Активные ингредиенты: Эзетимиб, Симвастатин.
ГОЛТОР 10 мг / 10 мг
ГОЛТОР 10 мг / 20 мг
ГОЛТОР 10 мг / 40 мг
ГОЛТОР 10 мг / 80 мг таблетки
Показания Почему применяется Голтор? Для чего это?
ГОЛТОР содержит активные вещества эзетемиб и симвастатин. ГОЛТОР - это лекарство, которое используется для снижения уровня общего холестерина, «плохого» холестерина (холестерина ЛПНП) и жирных веществ, называемых триглицеридами, в крови. Кроме того, GOLTOR увеличивает уровень «хорошего» холестерина (холестерина ЛПВП).
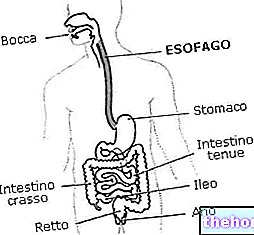
GOLTOR снижает уровень холестерина двумя способами. Действующее вещество эзетимиб снижает уровень холестерина, всасываемого в пищеварительном тракте. Активный ингредиент симвастатин, который принадлежит к классу «статинов», подавляет выработку холестерина, синтезируемого организмом.
Холестерин - одно из нескольких жирных веществ, обнаруженных в кровотоке. Общий холестерин в основном состоит из холестерина ЛПНП и холестерина ЛПВП. Холестерин ЛПНП часто называют «плохим» холестерином, потому что он может накапливаться в стенках артерий и образовывать бляшки. Со временем образование бляшек может привести к сужению артерий. Это сужение может замедлить или заблокировать приток крови к жизненно важным органам, таким как сердце и мозг. Эта блокировка кровотока может вызвать сердечный приступ или инсульт.
Холестерин ЛПВП часто называют «хорошим» холестерином, потому что он помогает предотвратить накопление плохого холестерина в артериях и защищает от сердечных заболеваний.
Триглицериды - это еще одна форма жира в крови, которая может увеличить риск сердечных заболеваний.
GOLTOR используется для пациентов, которые не могут контролировать свой уровень холестерина с помощью одной диеты. Принимая это лекарство, вы все равно должны соблюдать диету, снижающую уровень холестерина.
GOLTOR используется в качестве дополнения к вашему рациону для снижения уровня холестерина, если у вас есть:
- повышенный уровень холестерина в крови (первичная гиперхолестеринемия) [семейная и несемейная гетерозиготная] или повышенный уровень жира в крови (смешанная гиперлипидемия):
- кто плохо контролируется одним статином;
- для которых вы принимали статины и эзетимиб в виде отдельных таблеток;
- наследственное заболевание (гомозиготная семейная гиперхолестеринемия), повышающее уровень холестерина в крови. Возможно, вы лечитесь и другими методами лечения.
GOLTOR не помогает похудеть.
Противопоказания Когда не следует применять Голтор
Не принимайте ГОЛТОР, если:
- у вас аллергия (гиперчувствительность) на эзетимиб, симвастатин или любой другой ингредиент этого лекарства
- в настоящее время есть проблемы с печенью
- вы беременны или кормите грудью
- вы принимаете лекарства с одним или несколькими из следующих активных веществ:
- итраконазол, кетоконазол, позаконазол или вориконазол (используются для лечения грибковых инфекций)
- эритромицин, кларитромицин или телитромицин (используются для лечения инфекций)
- Ингибиторы протеазы ВИЧ, такие как индинавир, нелфинавир, ритонавир и саквинавир (ингибиторы протеазы ВИЧ используются для лечения ВИЧ-инфекций)
- боцепревир или телапревир (используются для лечения вирусных инфекций гепатита С)
- нефазодон (используется для лечения депрессии)
- кобицистат
- гемфиброзил (используется для снижения холестерина)
- циклоспорин (часто используется при трансплантации органов)
- даназол (искусственный гормон, используемый для лечения эндометриоза, состояния, при котором слизистая оболочка матки вырастает за пределы матки).
- вы принимаете или в последние 7 дней принимали или получали лекарство, называемое фузидиевой кислотой (используется для лечения бактериальной инфекции).
Не принимайте более 10 мг / 40 мг ГОЛТОРА, если вы принимаете ломитапид (используется для лечения серьезных и редких генетических холестериновых заболеваний).
Обратитесь за советом к своему врачу, если вы не уверены, что лекарство, которое вы принимаете, является одним из перечисленных выше.
Меры предосторожности при применении Что следует знать перед приемом Голтора
Сообщите своему врачу:
- всех ваших заболеваний, включая аллергию.
- если вы употребляете большое количество алкоголя или если у вас когда-либо было заболевание печени. В этом случае GOLTOR может вам не подойти.
- если вам предстоит операция. Возможно, вам придется на короткое время прекратить прием ГОЛТОРА.
- Если вы азиат, вам может подойти другая доза.
Ваш врач должен сдать анализ крови, прежде чем принимать ГОЛТОР, и если у вас есть симптомы проблем с печенью во время приема ГОЛТОРА. Этот анализ проводится для того, чтобы узнать, правильно ли функционирует печень.
Ваш врач может также назначить анализы крови для проверки функции печени после начала терапии ГОЛТОРОМ.
Пока вы лечитесь этим лекарством, ваш врач внимательно проверит, нет ли у вас диабета или вы не подвержены риску развития диабета. Вы рискуете заболеть диабетом, если у вас высокий уровень сахара и жира в крови, если у вас избыточный вес и высокое кровяное давление.
Сообщите своему врачу, если у вас тяжелое заболевание легких. Следует избегать применения ГОЛТОРА с фибратами (некоторые типы препаратов, снижающих уровень холестерина), поскольку использование ГОЛТОРА с фибратами не изучалось.
Немедленно обратитесь к врачу, если у вас есть боли в мышцах, мышечная болезненность и мышечная слабость по неустановленным причинам, поскольку мышечные проблемы могут, в редких случаях, быть серьезными и приводить к повреждению мышечной ткани, вызывающему повреждение почек, и очень редко наступает смерть. Риск повреждения мышц выше при более высоких дозах ГОЛТОРА, особенно при дозе 10 мг / 80 мг.
Риск мышечной травмы также выше у некоторых пациентов. Сообщите своему врачу, если к вам относится что-либо из следующего:
- есть проблемы с почками
- есть проблемы с щитовидной железой
- 65 лет и старше
- женщина
- когда-либо имели проблемы с мышцами во время лечения препаратами, снижающими уровень холестерина, называемыми статинами (такими как симвастатин, аторвастатин и розувастатин) или фибратами (такими как гемфиброзил и безафибрат)
- у вас или ваших ближайших родственников есть наследственное заболевание мышц.
Также сообщите своему врачу или фармацевту, если у вас постоянная мышечная слабость. Для диагностики и лечения этого состояния могут потребоваться дополнительные тесты и лекарства.
Дети и подростки
Применение ГОЛТОРА не рекомендуется детям младше 10 лет.
Взаимодействия Какие лекарства или продукты могут изменить действие Голтора
Сообщите своему врачу, если вы принимаете, недавно принимали или собираетесь принимать какие-либо другие лекарства с любым из следующих активных веществ. Прием GOLTOR с любым из следующих лекарств может увеличить риск мышечных проблем (некоторые из них уже упоминались выше в разделе «Не принимайте GOLTOR, если»):
- циклоспорин (часто используется у пациентов, получающих трансплантацию органов)
- даназол (искусственный гормон, используемый для лечения эндометриоза, состояния, при котором слизистая оболочка матки вырастает за пределы матки)
- лекарства с активными веществами, такими как итраконазол, кетоконазол, флуконазол, позаконазол или вориконазол (используются для лечения грибковых инфекций)
- фибраты с активными ингредиентами, такими как гемфиброзил и безафибрат (используются для снижения холестерина)
- эритромицин, кларитромицин, телитромицин или фузидовая кислота (используются для лечения бактериальных инфекций). Не принимайте фузидиевую кислоту, пока вы принимаете это лекарство. См. Также параграф 4 данной брошюры.
- Ингибиторы протеазы ВИЧ, такие как индинавир, нелфинавир, ритонавир и саквинавир (используются для лечения СПИДа)
- боцепревир или телапревир (используются для лечения вирусных инфекций гепатита С)
- нефазодон (используется для лечения депрессии)
- лекарства с активным веществом кобицистат
- амиодарон (используется для лечения нерегулярного сердцебиения)
- верапамил, дилтиазем или амлодипин (используются для лечения высокого кровяного давления, боли в груди, связанной с сердечными заболеваниями или другими сердечными заболеваниями)
- ломитапид (используется для лечения серьезных и редких генетических холестериновых заболеваний
- высокие дозы (1 г или более в день) ниацина или никотиновой кислоты (также используются для снижения холестерина)
- колхицин (используется для лечения подагры).
В дополнение к лекарствам, перечисленным выше, сообщите своему врачу или фармацевту, если вы принимаете или недавно принимали какие-либо другие лекарства, в том числе полученные без рецепта. В частности, сообщите своему врачу, если вы принимаете что-либо из следующего:
- лекарства с активным ингредиентом для предотвращения образования тромбов, такие как варфарин, флуиндион, фенпрокумон или аценокумарол (антикоагулянты)
- холестирамин (также используется для снижения холестерина), поскольку он влияет на работу ГОЛТОРА
- фенофибрат (также используется для снижения холестерина)
- рифампицин (применяется для лечения туберкулеза).
Вы также должны сообщить любому врачу, который прописывает новое лекарство, что вы принимаете ГОЛТОР.
ГОЛТОР с едой и питьем
Грейпфрутовый сок содержит одно или несколько веществ, которые изменяют метаболизм некоторых лекарств, в том числе GOLTOR. Следует избегать употребления грейпфрутового сока, так как он может увеличить риск мышечных проблем.
Предупреждения Важно знать, что:
Беременность и кормление грудью
Не используйте ГОЛТОР, если вы беременны, если вы собираетесь забеременеть или подозреваете беременность. Если вы забеременели во время приема ГОЛТОРА, немедленно прекратите его прием и обратитесь к врачу. GOLTOR не следует использовать во время грудного вскармливания, поскольку неизвестно, проникает ли лекарство в грудное молоко.
Прежде чем принимать какое-либо лекарство, посоветуйтесь со своим врачом или фармацевтом.
Вождение и использование машин
Ожидается, что GOLTOR не будет мешать вам управлять автомобилем или пользоваться механизмами. Однако следует учитывать, что некоторые люди испытывали головокружение после приема ГОЛТОРА.
ГОЛТОР содержит лактозу
Таблетки ГОЛТОР содержат сахар, лактозу. Если врач сказал вам, что у вас «непереносимость некоторых сахаров», обратитесь к врачу, прежде чем принимать это лекарство.
Дозировка и способ применения Как применять Голтор: Дозировка
Ваш врач определит, какая дозировка вам подходит, исходя из вашего текущего лечения и вашего профиля риска.
Таблетки не разбиты и не подлежат разделению.
Всегда принимайте это лекарство точно так, как вам объяснили врач или фармацевт. В случае сомнений проконсультируйтесь с врачом или фармацевтом.
- Прежде чем начать принимать GOLTOR, вы должны уже соблюдать диету для снижения уровня холестерина.
- Во время лечения GOLTOR вы должны продолжать соблюдать эту диету, чтобы снизить уровень холестерина.
Взрослые: доза составляет 1 таблетку ГОЛТОРА внутрь 1 раз в сутки.
Применение у подростков (от 10 до 17 лет): доза составляет 1 таблетку ГОЛТОРА перорально один раз в день (не следует превышать максимальную дозу 10 мг / 40 мг один раз в день).
Доза 10 мг / 80 мг GOLTOR рекомендуется только взрослым пациентам с очень высоким уровнем холестерина и высоким риском сердечных заболеваний, которые не достигли своего идеального уровня холестерина с помощью самых низких доз.
Вечером принимать ГОЛТОР. Вы можете принимать его с едой или без нее.
Если ваш врач прописал ГОЛТОР с другим лекарством, снижающим уровень холестерина, содержащим активное вещество холестирамин или любой другой агент, связывающий желчные кислоты, вы должны принять ГОЛТОР по крайней мере за 2 часа до или через 4 часа после приема агента, связывающего желчные кислоты.
Если вы забыли принять ГОЛТОР
- не принимайте двойную дозу, чтобы восполнить забытую таблетку, просто примите обычную дозу GOLTOR на следующий день в обычное время.
Если вы перестанете принимать ГОЛТОР
- поговорите со своим врачом или фармацевтом, поскольку ваш холестерин может снова подняться. Если у вас есть дополнительные вопросы по использованию этого лекарства, спросите своего врача или фармацевта.
Передозировка Что делать, если вы приняли слишком много Голтора
Если вы приняли больше GOLTOR, чем следует, обратитесь к врачу или фармацевту.
Побочные эффекты Каковы побочные эффекты Голтора
Как и все лекарства, GOLTOR может вызывать побочные эффекты, хотя они возникают не у всех (см. Раздел 2, что вам нужно знать перед приемом GOLTOR).
Сообщалось о следующих распространенных побочных эффектах (им может быть подвержено до 1 человека из 10):
- боль в мышцах
- увеличение значений лабораторных анализов крови для функции печени (трансаминаза) и / или мышц (CK)
Сообщалось о следующих необычных побочных эффектах (им может быть подвержено до 1 человека из 100):
- увеличение значений анализов крови, связанных с функцией печени; повышение уровня мочевой кислоты в крови; увеличение времени, необходимого для свертывания крови; присутствие белка в моче; снижение массы тела
- головокружение Головная боль; ощущение покалывания
- боль в животе; несварение желудка; метеоризм; тошнота; Его рвало; вздутие живота; понос; сухость во рту; боль в животе
- сыпь; зуд; крапивница
- боль в суставах; мышечная боль, чувствительность; слабость или судороги; боль в шее; боль в руках или ногах; боль в спине • необычная усталость или слабость; чувство усталости; грудная боль; отек, особенно рук и ног
- расстройство сна; трудности с засыпанием
Кроме того, у людей, принимающих ГОЛТОР или лекарства, содержащие активные вещества эзетимиб или симвастатин, были зарегистрированы следующие побочные эффекты:
- низкое количество эритроцитов (анемия); снижение количества клеток крови, что может вызвать синяки / кровотечение (тромбоцитопения)
- потеря чувствительности или слабость в руках и ногах; плохая память; потеря памяти; путаница
- проблемы с дыханием, включая постоянный кашель и / или одышку или лихорадку
- запор
- воспаление поджелудочной железы часто с сильной болью в животе
- воспаление печени со следующими симптомами: пожелтение кожи и глаз; зуд; темная моча или светлый стул; чувство усталости или слабости; потеря аппетита; печеночная недостаточность; камни желчного пузыря или воспаление желчного пузыря (которое может вызвать боль в животе, тошноту и рвоту)
- выпадение волос; выпуклая красная сыпь, иногда с поражениями формы мишени (мультиформная эритема)
- реакция гиперчувствительности, которая включает некоторые из следующих характеристик: гиперчувствительность (аллергические реакции, включая отек лица, губ, языка и / или горла, которые могут вызвать затруднение дыхания или глотания и требуют немедленного лечения, боль или воспаление суставов, воспаление крови сосуды, аномальные синяки, сыпь и отек, крапивница, чувствительность кожи к солнцу, лихорадка, гиперемия, одышка и плохое самочувствие, волчаночные симптомы (включая сыпь, кожные проблемы) суставов и влияние на лейкоциты).
- мышечная боль; чувствительность; мышечная слабость или судороги; травмы мышц; проблемы с сухожилиями, иногда осложняющиеся разрывом сухожилий.
- снижение аппетита
- приливы; высокое кровяное давление
- болеть
- Эректильная дисфункция
- депрессия
- изменения в некоторых значениях анализов крови, связанных с функцией печени
Дополнительные возможные побочные эффекты, о которых сообщают некоторые статины:
- нарушения сна, включая кошмары
- сексуальные трудности
- диабет. Это более вероятно, если у вас высокий уровень сахара и жира в крови, избыточный вес и высокое кровяное давление. Ваш врач будет наблюдать за вами во время лечения этим лекарством.
- постоянная боль в мышцах, болезненность или слабость, которые могут не исчезнуть после прекращения приема ГОЛТОРА (частота неизвестна).
Немедленно обратитесь к врачу, если у вас есть боли в мышцах, мышечная болезненность и мышечная слабость по неустановленным причинам, поскольку мышечные проблемы могут, в редких случаях, быть серьезными и приводить к повреждению мышечной ткани, вызывающему повреждение почек, и очень редко наступает смерть.
Сообщение о побочных эффектах
Если вы заметили какие-либо побочные эффекты, поговорите со своим врачом или фармацевтом, включая любые возможные побочные эффекты, не указанные в данном информационном листке. Вы также можете сообщить о побочных эффектах напрямую через национальную систему отчетности по адресу: www.agenziafarmaco.gov.it/it/responsabili Сообщив о побочных эффектах, вы поможете получить больше информации о безопасности этого лекарства.
Срок действия и удержание
Храните это лекарство в недоступном для детей месте.
Не используйте это лекарство по истечении срока годности, указанного на упаковке после «EXP».
Таблетки ГОЛТОР нельзя хранить при температуре выше 30 ° С.
Блистеры: Хранить в оригинальной упаковке для защиты лекарства от света и влаги.
Бутылки: Держите бутылки плотно закрытыми, чтобы защитить лекарство от света и влаги.
Не выбрасывайте лекарства в сточные воды или бытовые отходы. Спросите своего фармацевта, как утилизировать лекарства, которые вы больше не используете. Это поможет защитить окружающую среду.
Дополнительная информация
Что значит ГОЛТОР
Действующие вещества ГОЛТОРА - эзетимиб и симвастатин.
Каждая таблетка содержит 10 мг эзетимиба и 10 мг, 20 мг, 40 мг или 80 мг симвастатина.
Другие ингредиенты: бутилгидроксианизол, моногидрат лимонной кислоты, натрийкроскармеллоза, гипромеллоза, моногидрат лактозы, стеарат магния, микрокристаллическая целлюлоза, пропилгаллат.
Описание внешнего вида ГОЛТОР и содержимого упаковки
GOLTOR выпускается в виде таблеток в форме капсул от белого до кремового цвета с кодом «311», «312», «313» или «315» на одной стороне. Таблетки не разбиты и не подлежат разделению.
GOLTOR выпускается в упаковках по 7, 10, 14, 28, 30, 50, 56, 84, 90, 98, а также в групповых упаковках по 98 (2 упаковки по 49), 100 или 300 таблеток.
Не все размеры упаковки могут быть проданы.
Листовка с исходным кодом: AIFA (Итальянское агентство по лекарственным средствам). Контент опубликован в январе 2016 года. Представленная информация может быть устаревшей.
Чтобы иметь доступ к самой последней версии, рекомендуется зайти на сайт AIFA (Итальянское агентство по лекарственным средствам). Заявление об ограничении ответственности и полезная информация.
01.0 НАИМЕНОВАНИЕ ЛЕКАРСТВЕННОГО ПРЕПАРАТА
ГОЛЬТОР ПЛАНШЕТЫ
02.0 КАЧЕСТВЕННЫЙ И КОЛИЧЕСТВЕННЫЙ СОСТАВ
Каждая таблетка содержит 10 мг эзетимиба и 10, 20, 40 или 80 мг симвастатина.
Наполнитель (и):
Каждая таблетка 10 мг / 10 мг содержит 58,2 мг моногидрата лактозы.
Каждая таблетка 10 мг / 20 мг содержит 126,5 мг моногидрата лактозы.
Каждая таблетка 10 мг / 40 мг содержит 262,9 мг моногидрата лактозы.
Каждая таблетка 10 мг / 80 мг содержит 535,8 мг моногидрата лактозы.
Полный список вспомогательных веществ см. В разделе 6.1.
03.0 ФАРМАЦЕВТИЧЕСКАЯ ФОРМА
Таблетка.
Таблетки в форме капсул от белого до кремового цвета с кодом «311», «312», «313» или «315» на одной стороне.
04.0 КЛИНИЧЕСКАЯ ИНФОРМАЦИЯ
04.1 Терапевтические показания
Гиперхолестеринемия
GOLTOR показан в качестве дополнения к диете пациентам с первичной гиперхолестеринемией (семейной и несемейной гетерозиготной) или со смешанной гиперлипидемией, когда показано использование комбинированного продукта:
• пациенты, не получающие адекватного контроля только статинами;
• пациенты, которые уже получали статины и эзетимиб.
ГОЛТОР содержит эзетимиб и симвастатин. Симвастатин (20-40 мг) снижает частоту сердечно-сосудистых событий (см. Раздел 5.1). Благоприятный эффект эзетимиба на сердечно-сосудистую заболеваемость и смертность еще не продемонстрирован.
Гомозиготная семейная гиперхолестеринемия (гомозиготный IF)
ГОЛТОР показан в качестве дополнения к диете пациентам с гомозиготной семейной гиперхолестеринемией. Пациентам также могут быть назначены дополнительные терапевтические меры (например, аферез липопротеидов низкой плотности [ЛПНП]).
04.2 Дозировка и способ применения
Гиперхолестеринемия
Пациенту следует придерживаться адекватного режима питания с низким содержанием жиров и продолжать диету во время лечения препаратом ГОЛТОР.
Лекарство следует принимать внутрь. Диапазон доз GOLTOR составляет от 10 мг / 10 мг / день до 10 мг / 80 мг / день вечером. Не все дозировки доступны во всех государствах-членах. Обычная доза составляет 10 мг / 20 мг / день. O 10 мг / 40 мг / день назначают вечером в виде однократной дозы. Доза 10 мг / 80 мг рекомендуется только пациентам с тяжелой гиперхолестеринемией и высоким риском сердечно-сосудистых осложнений, которые не достигли терапевтических целей с помощью более низких доз, и когда ожидается, что преимущества перевешивают потенциальные риски (см. разделы 4.4 и 5.1).
В начале лечения или при изменении дозы следует учитывать уровень холестерина липопротеинов низкой плотности (ХС-ЛПНП), риск ишемической болезни сердца и реакцию пациента на текущую терапию, снижающую уровень холестерина.
Дозу GOLTOR следует подбирать индивидуально в зависимости от признанной эффективности различных сильных сторон GOLTOR (см. Раздел 5.1, таблица 1) и от реакции на продолжающуюся холестеринснижающую терапию. Корректировку дозы, если требуется, следует производить через определенные промежутки времени. Менее 4 недель ГОЛТОР можно вводить во время еды или без нее. Таблетку нельзя разделять.
Гомозиготная семейная гиперхолестеринемия
Рекомендуемая начальная доза для пациентов с гомозиготной семейной гиперхолестеринемией составляет 10 мг / 40 мг / сут в вечернее время. Доза 10 мг / 80 мг рекомендуется только в том случае, если ожидается, что польза превышает потенциальный риск (см. Выше; разделы 4.3 и 4.4). GOLTOR может использоваться у этих пациентов в качестве адъюванта к другим гиполипидемическим препаратам (например, аферез ЛПНП) или если такие методы лечения недоступны.
Одновременный прием с другими лекарственными средствами
Администрация GOLTOR должна происходить за ≥ 2 часа до или через ≥ 4 часов после введения агента, связывающего желчные кислоты.
У пациентов, принимающих амиодарон, амлодипин, верапамил или дилтиазем одновременно с GOLTOR, доза GOLTOR не должна превышать 10 мг / 20 мг / день (см. Разделы 4.4 и 4.5).
У пациентов, получающих гиполипидемические дозы ниацина (≥ 1 г / день) одновременно с GOLTOR, доза GOLTOR не должна превышать 10 мг / 20 мг / день (см. Разделы 4.4 и 4.5).
Использование у пожилых людей
У пожилых пациентов коррекции дозы не требуется (см. Раздел 5.2).
Использование у детей и подростков
Начало лечения необходимо проводить под наблюдением специалиста.
Подростки ≥ 10 лет (пубертатный статус: мальчики со стадией Таннера II и выше и девочки, у которых постменархе не менее одного года): клинический опыт у педиатрических пациентов и пациентов подросткового возраста (от 10 до 17 лет) ограничен. Обычно рекомендуется начинать доза составляет 10 мг / 10 мг один раз в день вечером. Рекомендуемый диапазон доз составляет от 10 мг / 10 мг до максимум 10 мг / 40 мг / день (см. разделы 4.4 и 5.2).
Дети
Использование при поражении печени
Коррекция дозы не требуется при легкой (оценка по шкале Чайлд-Пью от 5 до 6) печеночной недостаточности. Лечение препаратом GOLTOR не рекомендуется пациентам с умеренной (оценка по шкале Чайлд-Пью от 7 до 9) или тяжелой печеночной недостаточностью (оценка по шкале Чайлд-Пью> 9). ), (см. разделы 4.4 и 5.2).
Использование при поражении почек
У пациентов с почечной недостаточностью легкой степени (расчетная скорость клубочковой фильтрации ≥60 мл / мин / 1,73 м2) изменение дозы не требуется. У пациентов с хронической болезнью почек и предполагаемой скоростью клубочковой фильтрации 2 рекомендуемая доза GOLTOR составляет 10/20 мг один раз в день вечером (см. Разделы 4.4, 5.1 и 5.2). Более высокие дозы следует назначать с осторожностью.
04.3 Противопоказания
Повышенная чувствительность к эзетимибу, симвастатину или к любому из вспомогательных веществ.
Беременность и период лактации (см. Раздел 4.6).
Активное заболевание печени или повышенные, стойкие и неопределенные значения сывороточных трансаминаз.
Одновременное применение сильнодействующих ингибиторов CYP3A4 (агентов, которые увеличивают AUC примерно в 5 или более раз) (например, итраконазол, кетоконазол, позаконазол, вориконазол, эритромицин, кларитромицин, телитромицин, ингибиторы протеазы ВИЧ (например, нелфинавир) (неелфинавир), боцепревир), боцепревир см. разделы 4.4 и 4.5).
Одновременный прием гемфиброзила, циклоспорина или даназола (см. Разделы 4.4 и 4.5).
04.4 Особые предупреждения и соответствующие меры предосторожности при использовании
Миопатия / рабдомиолиз
В постмаркетинговом опыте применения эзетимиба сообщалось о случаях миопатии и рабдомиолиза. Большинство пациентов, у которых развился рабдомиолиз, получали сопутствующую терапию эзетимибом и статинами. Однако очень редко сообщалось о рабдомиолизе при применении эзетимиба и монотерапии. эзетимиб по сравнению с другими агентами, которые, как известно, связаны с повышенным риском рабдомиолиза.
ГОЛТОР содержит симвастатин. Симвастатин, как и другие ингибиторы ГМГ-КоА-редуктазы, иногда вызывает миопатию, проявляющуюся в виде мышечной боли, болезненности или слабости, связанных с повышением уровня креатинкиназы (КК) выше верхней границы нормы в 10 раз. Миопатия иногда проявляется как рабдомиолиз с или без острая почечная недостаточность, вторичная по отношению к миоглобинурии, и очень редко случаются летальные исходы. Риск миопатии увеличивается из-за высоких уровней ингибирующей активности HMG-CoA редуктазы в плазме.
Как и в случае с другими ингибиторами ГМГ-КоА-редуктазы, риск миопатии / рабдомиолиза зависит от дозы симвастатина. В базе данных клинических исследований, в которой 41413 пациентов лечили симвастатином, 24747 (примерно 60%) из них были включены в исследования со средним значением При последующем наблюдении не менее 4 лет частота миопатии составила примерно 0,03%, 0,08% и 0,61% при приеме 20, 40 и 80 мг / сут соответственно. В этих исследованиях за пациентами тщательно наблюдали, и некоторые взаимодействующие лекарства были исключены.
В клиническом исследовании, в котором пациенты с инфарктом миокарда в анамнезе получали симвастатин в дозе 80 мг / день (средний период наблюдения 6,7 лет), частота миопатии составляла примерно 1,0% по сравнению с частотой 0,02%, наблюдаемой у пациентов. лечился 20 мг / день. Примерно половина этих случаев миопатии произошла в течение первого года лечения. Частота миопатии в течение каждого последующего года лечения составляла приблизительно 0,1% (см. разделы 4.8 и 5.1).
Риск миопатии выше у пациентов, получавших GOLTOR 10/80 мг, чем у пациентов, принимающих другие статины с аналогичной эффективностью в снижении уровня холестерина ЛПНП. Следовательно, доза GOLTOR 10/80 мг должна использоваться только у пациентов с тяжелой гиперхолестеринемией и с высоким риском сердечно-сосудистых осложнений, которые не достигли целей лечения с помощью более низких доз, и когда ожидается, что польза превысит потенциальный риск. У пациентов, получавших GOLTOR 10/80 мг, которым требуется взаимодействующий агент, следует использовать более низкую дозу GOLTOR или альтернативную схему приема статинов с более низким потенциалом лекарственного взаимодействия (см. Ниже. Меры по снижению риска миопатии, вызванной лекарственными взаимодействиями и пункты 4.2, 4.3 и 4.5).
В клиническом исследовании, в котором более 9000 пациентов с хроническим заболеванием почек были рандомизированы для получения GOLTOR 10/20 мг в день (n = 4650) или плацебо (n = 4620) (средний период наблюдения 4,9 года), частота миопатии составила 1%. составлял 0,2% для GOLTOR и 0,1% для плацебо (см. раздел 4.8).
В клиническом исследовании, в котором пациенты с высоким риском сердечно-сосудистых заболеваний лечились симвастатином в дозе 40 мг / день (средний период наблюдения 3,9 года), частота миопатии у пациентов составила примерно 0,05%. Некитайские (n = 7367) против 0,24% для китайских пациентов (n = 5468). Хотя единственная азиатская популяция, оцениваемая в этом клиническом исследовании, была китайцами, следует проявлять осторожность при назначении ГОЛТОРА азиатским пациентам и обязательно использовать самую низкую дозу.
Сниженная функциональность транспортных белков
Снижение функции печеночных транспортных белков ОАТФ может увеличить системное воздействие симвастатиновой кислоты и увеличить риск миопатии и рабдомиолиза.Снижение функции может возникать как в результате ингибирования из-за взаимодействующих препаратов (например, циклоспорина), так и у пациентов с генотипом SLCO1B1 c.521T> C.
Пациенты, несущие аллель гена SLCO1B1 (c.521T> C), кодирующего менее активный белок OATP1B1, имеют повышенное системное воздействие симвастатиновой кислоты и больший риск миопатии. Риск миопатии, связанной с высокой дозой (80 мг) симвастатина, в целом составляет примерно 1% без генетического тестирования. Согласно результатам исследования SEARCH, гомозиготные носители C (также называемые CC), получавшие 80 мг, имеют 15% риск миопатии в течение одного года, в то время как риск у гетерозиготных носителей гетерозиготного аллеля C (CT) составляет 1,5%. Относительный риск составляет 0,3% у пациентов с наиболее распространенным генотипом (TT) (см. Раздел 5.2). Если возможно, генотипирование на наличие аллеля C следует рассматривать как часть оценки пользы и риска перед назначением симвастатина 80 мг отдельным пациентам, а пациентам с генотипом CC следует избегать высоких доз. этот ген при генотипировании не исключает возможности развития миопатии.
Измерение уровня креатинкиназы
Уровни КФК не следует измерять после интенсивных упражнений или при наличии какой-либо альтернативной причины повышения КК, так как это может затруднить интерпретацию данных. Если уровни КФК значительно повышены на исходном уровне (более чем в 5 раз превышают верхний предел нормы), их следует повторно измерить в течение 5-7 дней для подтверждения результатов.
До лечения
Все пациенты, начинающие терапию ГОЛТОРОМ или увеличивающие дозу ГОЛТОРА, должны быть проинформированы о риске миопатии и проинструктированы немедленно сообщать о любой необъяснимой мышечной боли, болезненности и слабости.
Следует проявлять осторожность у пациентов с предрасполагающими факторами к рабдомиолизу. Чтобы установить исходное референсное значение, уровень КФК следует измерить перед началом лечения в следующих случаях:
• пожилые (возраст ≥ 65 лет)
• женский пол
• поражение почек
• неконтролируемый гипотиреоз
• личный или семейный анамнез наследственных мышечных заболеваний
• история предыдущих эпизодов мышечной токсичности при приеме статинов или фибратов
• злоупотребление алкоголем.
В вышеупомянутых случаях риск, связанный с лечением, необходимо сопоставить с возможной пользой, и в случае лечения рекомендуется более тщательное наблюдение за пациентом. Если пациент ранее имел мышечные расстройства во время лечения фибратом или статином, лечение любым статинсодержащим продуктом (например, GOLTOR) следует начинать только с осторожностью. Если уровни КФК значительно повышены на исходном уровне (более чем в 5 раз превышают верхний предел нормы), лечение не следует начинать.
Во время лечения
Если пациент сообщает о мышечной боли, слабости или судорогах во время лечения препаратом ГОЛТОР, следует измерить уровень КФК. В случае значительного повышения уровня КФК (более чем в 5 раз выше верхней границы нормы) при отсутствии физических нагрузок терапию следует прекратить. Прекращение лечения может быть рассмотрено в случае серьезных мышечных симптомов, вызывающих ежедневный дискомфорт, даже если значения CK остаются ниже 5-кратного верхнего предела нормы. Лечение следует прекратить, если есть подозрение на миопатию по любой другой причине.
Если симптомы исчезнут и уровни КК вернутся к норме, можно рассмотреть возможность повторного введения GOLTOR или другого продукта, содержащего другой статин, в самой низкой дозе и под тщательным наблюдением.
Более высокая частота миопатии наблюдалась у пациентов, получавших симвастатин в дозе 80 мг (см. Раздел 5.1). Рекомендуется периодически измерять уровни КФК, поскольку они могут быть полезны для выявления субклинических случаев миопатии. Однако нет уверенности в том, что такой мониторинг предотвратит миопатию.
Терапию ГОЛТОРОМ следует временно прервать за несколько дней до серьезной плановой операции и в случае развития какого-либо серьезного медицинского или хирургического состояния.
Меры по снижению риска миопатии, вызванной лекарственными взаимодействиями (см. Также раздел 4.5)
Риск миопатии и рабдомиолиза значительно увеличивается при одновременном применении GOLTOR с мощными ингибиторами CYP3A4 (такими как итраконазол, кетоконазол, позаконазол, вориконазол, эритромицин, кларитромицин, телитромицин, ингибиторы протеазы ВИЧ, тельфапревир-вирон) (например, нелфапреавирон) (например, нелфецепревирвирон). ), как и циклоспорин, даназол и гемфиброзил. Использование этих лекарственных средств противопоказано (см. Раздел 4.3).
Из-за присутствия симвастатина в GOLTOR риск миопатии и рабдомиолиза также увеличивается при одновременном применении других фибратов, ниацина в гиполипидемических дозах (≥ 1 г / день) или при одновременном применении амиодарона, амлодипина, верапамила. или дилтиазем с некоторыми дозами ГОЛТОРА (см. разделы 4.2 и 4.5). Риск миопатии, в том числе рабдомиолиза, может увеличиваться при одновременном назначении ГОЛТОРА и фузидовой кислоты (см. Раздел 4.5).
Следовательно, что касается ингибиторов CYP3A4, одновременный прием GOLTOR с итраконазолом, кетоконазолом, позаконазолом, вориконазолом, ингибиторами протеазы ВИЧ (например, нелфинавиром), боцепревиром, телапревиром, эритромицином, кларитромицином, контра-телфитромом (см. Разделы 4.5 и 4.3). Если нельзя избежать терапии сильными ингибиторами CYP3A4 (агенты, которые увеличивают AUC примерно в 5 или более раз), лечение ГОЛТОРОМ следует прекратить (и рассмотреть возможность применения другого статина) во время. Кроме того, следует соблюдать осторожность при сочетании ГОЛТОРА с некоторые другие менее сильные ингибиторы CYP3A4: флуконазол, верапамил, дилтиазем (см. разделы 4.2 и 4.5). Следует избегать одновременного приема грейпфрутового сока и ГОЛТОРА.
Симвастатин не следует назначать одновременно с фузидиевой кислотой. Сообщалось о рабдомиолизе (включая некоторые летальные исходы) у пациентов, получавших эту комбинацию (см. Раздел 4.5). Пациентам, которым системное применение фузидиевой кислоты необходимо, лечение статинами следует прекратить на время лечения фузидиевой кислотой. Пациентам следует рекомендовать немедленно обратиться за медицинской помощью при появлении симптомов мышечной слабости, боли или болезненности.
Терапию статинами можно возобновить через семь дней после приема последней дозы фузидовой кислоты. В исключительных случаях, когда требуется длительное системное применение фузидиевой кислоты, например, для лечения тяжелых инфекций, необходимо только оценивать необходимость совместного введения GOLTOR и фузидиевой кислоты. в индивидуальном порядке под строгим медицинским наблюдением.
Следует избегать одновременного применения GOLTOR в дозах выше 10 мг / 20 мг в день и ниацина в дозах, снижающих уровень липидов (≥ 1 г / день), за исключением случаев, когда клиническая польза может перевешивать повышенный риск миопатии (см. Разделы 4.2 и 4.5. ).
Редкие случаи миопатии / рабдомиолиза были связаны с одновременным назначением ингибиторов HMG-CoA-редуктазы и липид-модифицирующих доз ниацина (никотиновой кислоты) (≥ 1 г / день), оба из которых могут вызвать миопатию при применении.
В клиническом исследовании (средний период наблюдения 3,9 года) с участием пациентов с высоким риском сердечно-сосудистых заболеваний и с хорошо контролируемыми уровнями ХС-ЛПНП, принимавших симвастатин 40 мг / день с эзетимибом 10 мг или без него, не было никаких дополнительных преимуществ для сердечно-сосудистые исходы при добавлении липид-модифицирующих доз ниацина (никотиновой кислоты) (≥1 г / день). Таким образом, врачи рассматривают возможность комбинированной терапии симвастатином и дозами липид-модифицирующего ниацина (никотиновой кислоты) (≥ 1 г / день) или Продукты, содержащие ниацин, должны тщательно взвешивать потенциальные преимущества и риски и должны внимательно следить за пациентами на предмет любых признаков или симптомов мышечной боли, чувствительности или слабости, особенно в первые месяцы терапии и при увеличении доз того или иного лекарства. .
Кроме того, в этом исследовании частота миопатии составляла приблизительно 0,24% для китайских пациентов, получавших симвастатин 40 мг или эзетимиб / симвастатин 10/40 мг, по сравнению с 1,24% для китайских пациентов, получавших симвастатин. 40 мг или эзетимиб / симвастатин 10 / 40 мг одновременно с никотиновой кислотой / ларопипрантом 2,000 мг / 40 мг с модифицированным высвобождением. Хотя единственной азиатской популяцией, оцениваемой в этом клиническом исследовании, была китайская популяция, поскольку частота миопатии у китайских пациентов выше, чем у некитайских пациентов, одновременное введение GOLTOR с дозами ниацина (никотиновой кислоты) может изменить липидный профиль ( ≥ 1 г / день) не рекомендуется пациентам из Азии.
Аципимокс структурно родственен ниацину. Хотя аципимокс не изучался, риск токсических эффектов, связанных с мышцами, может быть таким же, как у ниацина.
Следует избегать одновременного применения ГОЛТОРА в дозах выше 10 мг / 20 мг в день и амиодарона, амлодипина, верапамила или дилтиазема (см. Разделы 4.2 и 4.5).
Пациенты, принимающие другие лекарственные средства, которые, как известно, оказывают умеренное ингибирующее действие на CYP3A4 в терапевтических дозах при одновременном применении с GOLTOR, особенно с более высокими дозами GOLTOR, могут иметь повышенный риск миопатии. Если GOLTOR назначается одновременно с умеренным ингибитором CYP3A4 (агенты, увеличивающие AUC примерно в 2-5 раз), может потребоваться корректировка дозы. Для некоторых умеренных ингибиторов CYP3A4, например дилтиазема, рекомендуется максимальная доза 10/20 мг GOLTOR (см. Раздел 4.2).
Безопасность и эффективность ГОЛТОРА, вводимого с фибратами, не изучались. При одновременном применении симвастатина и фибратов (особенно гемфиброзила) повышается риск миопатии. Поэтому одновременное применение ГОЛТОРА и гемфиброзила противопоказано (см. Раздел 4.3) и одновременный прием с другими фибратами не рекомендуется (см. раздел 4.5).
Ферменты печени
В исследованиях контролируемого комбинированного дозирования, в которых пациенты лечились эзетимибом и симвастатином, наблюдались последовательные повышения уровня трансаминаз (≥3-кратный верхний предел нормы [ULN]) (см. Раздел 4.8).
В контролируемом клиническом исследовании, в котором более 9000 пациентов с хроническим заболеванием почек были рандомизированы для получения GOLTOR 10/20 мг в день (n = 4650) или плацебо (n = 4620) (средний период наблюдения 4,9 года), частота последовательные повышения уровня трансаминаз (> 3-кратного ULN) составили 0,7% для GOLTOR и 0,6% для плацебо (см. раздел 4.8).
Рекомендуется проводить функциональные пробы печени до начала лечения препаратом ГОЛТОР и после этого при наличии клинических показаний. Пациенты, титрованные до дозы 10 мг / 80 мг, должны пройти дополнительный тест перед титрованием, через 3 месяца после титрования до дозы 10 мг / 80 мг и периодически после этого (например, каждые шесть месяцев) в течение первого года лечения. Особое внимание следует уделять пациентам, у которых наблюдается повышение уровня трансаминаз в сыворотке крови, и у этих пациентов анализы крови следует незамедлительно повторять и в дальнейшем проводить чаще. Если уровни трансаминаз демонстрируют признаки прогрессирования, особенно если они повышаются в 3 раза по сравнению с ВГН и остаются устойчивыми, лечение препаратом следует прекратить. Обратите внимание, что АЛТ может возникать в мышцах, поэтому повышение АЛТ и КК может указывать на миопатию (см. Выше). Миопатия / рабдомиолиз).
Были редкие постмаркетинговые сообщения о летальной и нефатальной печеночной недостаточности у пациентов, принимавших статины, включая симвастатин. Если во время лечения препаратом ГОЛТОР возникает тяжелое поражение печени с клиническими симптомами и / или гипербилирубинемия или желтуха, немедленно прекратите терапию. Если альтернативной этиологии не обнаружено, не возобновляйте терапию ГОЛТОРОМ.
GOLTOR следует применять с осторожностью пациентам, употребляющим значительное количество алкоголя.
Печеночная недостаточность
Из-за неизвестных эффектов повышенного воздействия эзетимиба у пациентов с умеренной или тяжелой печеночной недостаточностью применение GOLTOR не рекомендуется (см. Раздел 5.2).
Сахарный диабет
Некоторые данные свидетельствуют о том, что статины, как классовый эффект, повышают уровень глюкозы в крови и у некоторых пациентов с высоким риском развития диабета могут вызывать такой уровень гипергликемии, что противодиабетическая терапия является подходящей.
Однако этот риск перевешивается снижением сосудистого риска при использовании статинов и, следовательно, не должен быть причиной для прекращения лечения статинами.
Пациенты из группы риска (уровень глюкозы натощак от 5,6 до 6,9 ммоль / л, ИМТ> 30 кг / м2, повышенный уровень триглицеридов, артериальная гипертензия) должны находиться под клиническим и биохимическим наблюдением в соответствии с национальными рекомендациями.
Педиатрические пациенты (от 10 до 17 лет)
Безопасность и эффективность эзетимиба, вводимого совместно с симвастатином у пациентов в возрасте от 10 до 17 лет с гетерозиготной семейной гиперхолестеринемией, оценивались в контролируемом клиническом исследовании у мальчиков-подростков (стадия Таннера II или выше) и у девочек. минимум год.
В этом ограниченном контролируемом исследовании, как правило, не наблюдалось влияния на половое созревание или половое созревание мальчиков и девочек-подростков, а также на продолжительность менструального цикла у девочек.Однако влияние эзетимиба в течение периода лечения> 33 недель на половой рост и созревание не изучалось (см. Разделы 4.2 и 4.8).
Безопасность и эффективность эзетимиба при одновременном применении с симвастатином в дозах более 40 мг в день не изучались у педиатрических пациентов в возрасте от 10 до 17 лет.
Эзетимиб не изучался у пациентов младше 10 лет или у девочек до менархе (см. Разделы 4.2 и 4.8).
Долгосрочная эффективность терапии эзетимибом у пациентов младше 17 лет для снижения заболеваемости и смертности среди взрослых не изучалась.
Связки
Безопасность и эффективность эзетимиба, вводимого с фибратами, не установлены (см. Выше и разделы 4.3 и 4.5).
Антикоагулянты
Если GOLTOR добавляется к варфарину, другому кумариновому антикоагулянту или флуиндиону, необходимо надлежащим образом контролировать международное нормализованное соотношение (см. Раздел 4.5).
Интерстициальное заболевание легких
Сообщалось о случаях интерстициального заболевания легких при приеме некоторых статинов, включая симвастатин, особенно при длительной терапии (см. Раздел 4.8). Симптомы могут включать одышку, непродуктивный кашель и ухудшение общего состояния здоровья (утомляемость, потеря веса и лихорадка). Если есть подозрение, что у пациента развилось интерстициальное заболевание легких, терапию ГОЛТОРОМ следует прекратить.
Вспомогательные вещества
Пациентам с редкими наследственными проблемами непереносимости галактозы, дефицитом лактазы Лаппа или мальабсорбцией глюкозы-галактозы не следует принимать это лекарство.
04.5 Взаимодействие с другими лекарственными средствами и другие формы взаимодействия
Фармакодинамические взаимодействия
Взаимодействие с гиполипидемическими препаратами, которые могут вызвать миопатию при приеме отдельно
Риск миопатии, в том числе рабдомиолиза, увеличивается при одновременном приеме симвастатина с фибратами. Кроме того, «фармакокинетическое взаимодействие симвастатина с гемфиброзилом вызывает повышение уровня симвастатина в плазме» (см. Ниже, Фармакокинетические взаимодействия и разделы 4.3 и 4.4). Редкие случаи миопатии / рабдомиолиза были связаны с одновременным назначением симвастатина и липид-модифицирующих доз ниацина (≥ 1 г / день) (см. Раздел 4.4).
Фибраты могут увеличивать выведение холестерина с желчью, что приводит к холелитиазу. В доклиническом исследовании на собаках эзетимиб повышал уровень холестерина в желчи желчного пузыря (см. Раздел 5.3). Хотя актуальность этих доклинических данных для людей неизвестна, одновременное применение GOLTOR с фибратами не рекомендуется (см. Раздел 4.4).
Фармакокинетические взаимодействия
Рекомендации по назначению взаимодействующих агентов приведены в следующей таблице (дополнительные подробности включены в текст; см. Также разделы 4.2, 4.3 и 4.4).
Влияние других лекарственных средств на ГОЛТОР
ГОЛТОР
Ниацин: В исследовании с участием 15 здоровых взрослых одновременный прием GOLTOR (10 мг / 20 мг в день в течение 7 дней) приводил к небольшому увеличению средних значений AUC ниацина (22%) и никотинуровой кислоты (19%), учитывая в виде таблеток с пролонгированным высвобождением НИАСПАН (1000 мг в течение 2 дней и 2000 мг в течение 5 дней, принимаемых после завтрака с низким содержанием жиров). В том же исследовании одновременное применение НИАСПАН привело к небольшому увеличению средних значений AUC эзетимиба (9%), общего эзетимиба (26%), симвастатина (20%) и симвастатиновой кислоты (35%) (см. разделы 4.2 и 4.4).
Исследования лекарственного взаимодействия с более высокими дозами симвастатина не проводились.
Эзетимиб
Антациды: Одновременный прием антацидов снижает скорость абсорбции эзетимиба, но не влияет на биодоступность эзетимиба. Это снижение скорости абсорбции не считается клинически значимым.
Холестирамин: одновременное введение холестирамина уменьшало среднюю площадь под кривой (AUC) общего эзетимиба (эзетимиб + эзетимиб-глюкуронид) примерно на 55%. Дальнейшее снижение холестерина липопротеинов низкой плотности (ХС-ЛПНП) из-за добавления GOLTOR к холестирамину может быть уменьшено этим взаимодействием (см. Раздел 4.2).
Циклоспорин: В исследовании восьми пациентов после трансплантации почки с клиренсом креатинина> 50 мл / мин при стабильных дозах циклоспорина введение однократной дозы 10 мг эзетимиба привело к увеличению в 3,4 раза (диапазон 2,3-7,9 раза) средняя AUC для общего эзетимиба по сравнению со здоровой контрольной популяцией из другого исследования, получавшего только эзетимиб (n = 17). В другом исследовании пациент с трансплантатом с тяжелой почечной недостаточностью, получавший циклоспорин и несколько других лекарственных препаратов, показал 12-кратное более высокая «общая экспозиция» эзетимиба по сравнению с контрольной группой, получавшей только эзетимиб. В двухпериодном перекрестном исследовании из двенадцати здоровых субъектов ежедневное введение 20 мг эзетимиба в течение 8 дней с однократной дозой 100 мг циклоспорина на 7-й день привело к среднее увеличение на 15% AUC циклоспорина (в диапазоне от одного Снижение на 10% и увеличение на 51%) по сравнению с однократной дозой 100 мг одного циклоспорина. Контролируемых исследований влияния одновременного приема эзетимиба на экспозицию циклоспорина у пациентов с трансплантатом почки не проводилось.Одновременное применение ГОЛТОРА и циклоспорина противопоказано (см. Раздел 4.3).
Связки: Одновременный прием фенофибрата или гемфиброзила увеличивал общую концентрацию эзетимиба примерно в 1,5 и 1,7 раза соответственно. Хотя это повышение не считается клинически значимым, одновременный прием GOLTOR с гемфиброзилом противопоказан, а с другими фибратами не рекомендуется (см. Разделы 4.3 и 4.4).
Симвастатин
Симвастатин является субстратом цитохрома P450 3A4. Мощные ингибиторы цитохрома P450 3A4 увеличивают риск миопатии и рабдомиолиза за счет увеличения концентрации ингибирующей активности HMG-CoA редуктазы в плазме во время терапии симвастатином. Такие ингибиторы включают итраконазол, кетоконазол, позаконазол, вориконазол, эритромицин, кларитромицин, телитромицин, ингибиторы протеазы ВИЧ (например, нелфинавир), боцепревир, телапревир и нефазодон. Телитромицин вызвал 11-кратное увеличение экспозиции симвастатиновой кислоты.
Комбинация с итраконазолом, кетоконазолом, позаконазолом, вориконазолом, ингибиторами протеазы ВИЧ (например, нелфинавиром), боцепревиром, телапревиром, эритромицином, кларитромицином, телитромицином и нефазодоном противопоказана, а также с гемклофиброзилом) и циклоспорозилом. Если лечение сильнодействующими ингибиторами CYP3A4 (агенты, увеличивающие AUC примерно в 5 или более раз) неизбежно, терапию ГОЛТОРОМ следует прекратить (и следует рассмотреть возможность применения другого статина) во время курса лечения. Следует проявлять осторожность при комбинировании ГОЛТОРА. с некоторыми другими менее мощными ингибиторами CYP3A4: флуконазолом, верапамилом или дилтиаземом (см. разделы 4.2 и 4.4).
Флуконазол: Сообщалось о редких случаях рабдомиолиза, связанного с одновременным назначением симвастатина и флуконазола. (см. раздел 4.4).
Циклоспорин: риск миопатии / рабдомиолиза увеличивается при одновременном применении циклоспорина с GOLTOR; поэтому использование циклоспорина противопоказано (см. разделы 4.3 и 4.4) .Хотя механизм действия до конца не изучен, циклоспорин, как было показано, увеличивает AUC ингибиторов HMG-CoA редуктазы. симвастатиновой кислоты предположительно частично объясняется ингибированием CYP3A4 и / или OATP1B1.
Даназол: риск миопатии и рабдомиолиза увеличивается при одновременном приеме даназола с ГОЛТОРОМ; поэтому использование с даназолом противопоказано (см. разделы 4.3 и 4.4).
Гемфиброзил: гемфиброзил увеличивает AUC кислотного метаболита симвастатина в 1,9 раза, возможно, из-за ингибирования глюкуронизации и / или OATP1B1 (см. разделы 4.3 и 4.4). Одновременный прием с гемфиброзилом противопоказан.
Фузидиевая кислота
Риск миопатии, включая рабдомиолиз, может повышаться при одновременном применении системной фузидовой кислоты со статинами. Совместное применение этой комбинации может вызвать повышение концентрации обоих агентов в плазме. Механизм этого взаимодействия (фармакодинамический или фармакокинетический, или и то, и другое) до сих пор неизвестен. Сообщалось о рабдомиолизе (в том числе о некоторых случаях смерти) у пациентов, получавших эту комбинацию. Если требуется лечение фузидиевой кислотой, лечение ГОЛТОРОМ следует прекратить на время лечения фузидиевой кислотой (см. Раздел 4.4).
Амиодарон: риск миопатии и рабдомиолиза увеличивается при одновременном назначении амиодарона с симвастатином (см. раздел 4.4). В клиническом исследовании миопатия наблюдалась у 6% пациентов, получавших симвастатин 80 мг и амиодарон. Таким образом, доза ГОЛТОРА не должна превышать 10 мг / 20 мг в сутки у пациентов, получающих сопутствующую терапию амиодароном.
Блокаторы кальциевых каналов
• Верапамил: Риск миопатии и рабдомиолиза увеличивается при одновременном приеме верапамила с симвастатином 40 или 80 мг (см. Раздел 4.4).
В фармакокинетическом исследовании одновременный прием симвастатина с верапамилом приводил к увеличению воздействия симвастатиновой кислоты в 2,3 раза, предположительно, частично из-за ингибирования CYP3A4. Поэтому доза ГОЛТОРА не должна превышать 10 мг / 20 мг в день у пациентов, получающих сопутствующую терапию верапамилом.
• Дилтиазем: Риск миопатии и рабдомиолиза увеличивается при одновременном назначении дилтиазема и симвастатина 80 мг (см. Раздел 4.4). В фармакокинетическом исследовании одновременный прием дилтиазема и симвастатина вызывал 2,7-кратное увеличение воздействия симвастатиновой кислоты, возможно, из-за ингибирования CYP3A4. Поэтому доза ГОЛТОРА не должна превышать 10 мг / 20 мг в день у пациентов, получающих сопутствующую терапию дилтиаземом.
• Амлодипин
Пациенты, получающие сопутствующую терапию амлодипином и симвастатином, имеют повышенный риск миопатии. В фармакокинетическом исследовании одновременный прием амлодипина вызывал увеличение экспозиции симвастатиновой кислоты в 1,6 раза. Следовательно, доза GOLTOR не должна превышать 10 мг / 20 мг в день у пациентов, одновременно получающих амлодипин.
Умеренные ингибиторы CYP3A4
Пациенты, принимающие другие лекарственные средства, которые, как известно, оказывают умеренное ингибирующее действие на CYP3A4 при одновременном применении с GOLTOR, особенно с более высокими дозами GOLTOR, могут иметь повышенный риск миопатии (см. Раздел 4.4).
Ингибиторы транспортного белка OATP1B1
Симвастатиновая кислота является субстратом транспортного белка OATP1B1. Одновременный прием лекарственных средств, которые являются ингибиторами транспортного белка OATP1B1, может привести к повышению концентрации симвастатиновой кислоты в плазме и повышенному риску миопатии (см. Разделы 4.3 и 4.4).
Грейпфрутовый сок: грейпфрутовый сок подавляет цитохром P450 3A4. Одновременный прием симвастатина и больших количеств (более одного литра в день) грейпфрутового сока приводил к 7-кратному увеличению воздействия симвастатиновой кислоты. Потребление 240 мл грейпфрутового сока утром и симвастатина вечером также привело к увеличению в 1,9 раза, поэтому следует избегать приема грейпфрутового сока во время лечения ГОЛТОРОМ.
Колхицин: Сообщалось о миопатии и рабдомиолизе при одновременном применении колхицина и симвастатина у пациентов с почечной недостаточностью. Рекомендуется тщательный клинический мониторинг таких пациентов, принимающих эту комбинацию.
Рифампицин: Поскольку рифампицин является мощным индуктором CYP3A4, пациенты, проходящие длительную терапию рифампицином (например, лечение туберкулеза), могут испытывать потерю эффективности симвастатина. В фармакокинетическом исследовании на здоровых добровольцах площадь под кривой концентрации в плазме (AUC) для симвастатиновой кислоты уменьшалась на 93% при одновременном введении рифампицина.
НиацинСлучаи миопатии / рабдомиолиза наблюдались при одновременном применении симвастатина с липид-модифицирующими дозами ниацина (≥ 1 г / день) (см. Раздел 4.4).
Влияние ГОЛТОРА на фармакокинетику других лекарственных средств
Эзетимиб
В доклинических исследованиях было показано, что эзетимиб не индуцирует ферменты цитохрома P450, участвующие в метаболизме лекарств.Не наблюдалось клинически значимых фармакокинетических взаимодействий между эзетимибом и лекарствами, метаболизируемыми цитохромами P450 1A2, 2D6, 2C8, 2C9 и 3A4 или N-ацетилтрансферазой.
Антикоагулянты: В исследовании с участием двенадцати здоровых взрослых мужчин одновременный прием эзетимиба (10 мг один раз в сутки) не оказал значительного влияния на биодоступность варфарина и протромбиновое время. Тем не менее, были постмаркетинговые сообщения об увеличении международного нормализованного отношения у пациентов, которые добавляли эзетимиб к варфарину или флуиндиону. Если GOLTOR добавлен к варфарину или другому антикоагулянту кумарина, или к флуиндиону, следует надлежащим образом контролировать МНО ( см. раздел 4.4).
Симвастатин
Симвастатин не оказывает ингибирующего действия на цитохром P450 3A4. Следовательно, действие симвастатина на плазменные концентрации веществ, метаболизируемых через цитохром P450 3A4, не ожидается.
Пероральные антикоагулянты: в двух клинических исследованиях, одно на здоровых добровольцах, а другое на пациентах с гиперхолестеринемией, симвастатин в дозе 20-40 мг / день умеренно усиливал эффект кумариновых антикоагулянтов; Протромбиновое время, представленное как Международное нормализованное отношение (МНО), увеличилось с исходного уровня 1,7 до 1,8 и с исходного уровня 2,6 до 3,4 у добровольцев и пациентов исследования, соответственно. Сообщалось об очень редких случаях повышенного МНО. У пациентов, принимающих кумариновые антикоагулянты, протромбиновое время следует определять до начала лечения GOLTOR и достаточно часто на ранних этапах терапии, чтобы гарантировать отсутствие значительного изменения протромбинового времени. После регистрации стабильного протромбинового времени можно отслеживать протромбиновое время с интервалами, которые обычно рекомендуются пациентам, принимающим кумариновые антикоагулянты. Если доза ГОЛТОРА изменена или введение прервано, ту же процедуру необходимо повторить. Лечение симвастатином не было связано с кровотечением или изменениями протромбинового времени у пациентов, не получающих антикоагулянтную терапию.
04.6 Беременность и кормление грудью
Беременность
Атеросклероз - это хронический процесс, и регулярное прекращение приема гиполипидемических препаратов во время беременности должно иметь незначительное влияние на долгосрочный риск, связанный с первичной гиперхолестеринемией.
ГОЛТОР
ГОЛТОР противопоказан при беременности. Клинические данные об использовании ГОЛТОРА во время беременности отсутствуют. Исследования на животных при комбинированной терапии показали репродуктивную токсичность (см. Раздел 5.3).
Симвастатин
Безопасность применения симвастатина беременным не установлена. Контролируемых клинических исследований симвастатина у беременных женщин не проводилось. Были редкие сообщения о врожденных аномалиях после внутриутробного воздействия ингибиторов HMG-CoA редуктазы. Однако при проспективном анализе примерно 200 беременностей, подвергшихся в течение первого триместра воздействию симвастатина или другого близкородственного ингибитора HMG-CoA редуктазы, частота врожденных аномалий была сопоставима с таковой в общей популяции. Это количество беременностей было статистически достаточным, чтобы исключить увеличение частоты врожденных аномалий в 2,5 или более раз по сравнению с исходным уровнем.
Хотя нет никаких доказательств того, что частота врожденных аномалий у потомков пациентов, получавших симвастатин или другие близкородственные ингибиторы HMG-CoA редуктазы, отличается от таковой в общей популяции, лечение матерей симвастатином может снизить уровень мевалоната у плода. предшественник биосинтеза холестерина. По этой причине GOLTOR не следует использовать беременным женщинам, желающим забеременеть или подозревающим, что они беременны. Лечение GOLTOR следует приостановить на время беременности или до тех пор, пока она не будет определена. что женщина не беременна (см. раздел 4.3).
Эзетимиб
Нет данных о применении эзетимиба при беременности.
Время кормления
ГОЛТОР противопоказан в период лактации. Исследования на крысах показали, что эзетимиб выделяется с молоком. Неизвестно, выделяются ли активные компоненты ГОЛТОРА с грудным молоком (см. Раздел 4.3).
04.7 Влияние на способность управлять автомобилем и работать с механизмами
Исследования влияния на способность управлять автомобилем и работать с механизмами не проводились, однако при вождении или использовании механизмов следует иметь в виду, что сообщалось о головокружении.
04.8 Побочные эффекты
Безопасность GOLTOR (или одновременного приема эзетимиба и симвастатина, эквивалентного GOLTOR) оценивалась примерно у 12000 пациентов в клинических исследованиях.
Частота нежелательных эффектов классифицируется следующим образом: очень часто (≥ 1/10), часто ≥ 1/100,
Следующие нежелательные эффекты наблюдались у пациентов, получавших GOLTOR (N = 2404), и с большей частотой, чем плацебо (N = 1340).
Следующие нежелательные эффекты наблюдались у пациентов, получавших GOLTOR (N = 9 595), с большей частотой, чем при однократном введении статинов (N = 8 883).
Педиатрические пациенты (от 10 до 17 лет)
В исследовании, проведенном с участием пациентов подросткового возраста (от 10 до 17 лет) с гетерозиготной семейной гиперхолестеринемией (n = 248), повышение АЛТ и / или АСТ (≥ 3 × ВГН последовательно) наблюдалось у 3% (4 пациента) пациенты в группе эзетимиб / симвастатин по сравнению с 2% (2 пациента) пациентов в группе монотерапии симвастатином; процент увеличения значений CPK (≥ 10 X ULN) составлял 2% (2 пациента) и 0%, соответственно. О случаях миопатии не сообщалось.
Это исследование не подходило для сравнения редких побочных реакций на лекарства.
Пациенты с хронической болезнью почек
В исследовании защиты сердца и почек (SHARP) (см. Раздел 5.1) с участием более 9000 пациентов, получавших GOLTOR 10/20 мг в день (n = 4650) или плацебо (n = 4620), профили безопасности были сопоставимы во время лечения. средний срок наблюдения 4,9 года. В этом исследовании были зарегистрированы только серьезные нежелательные явления и прекращение приема из-за каких-либо нежелательных явлений. Частота прекращения лечения из-за побочных эффектов была сопоставимой (10,4% у пациентов, получавших GOLTOR, 9,8% у пациентов, получавших плацебо). Частота миопатии / рабдомиолиза составляла 0,2% у пациентов, получавших GOLTOR, и 0,1% у пациентов, получавших плацебо. Последовательное повышение уровня трансаминаз (> 3x ULN) произошло у 0,7% пациентов. Пациенты, получавшие GOLTOR, по сравнению с 0,6% пациентов, получавших плацебо В этом исследовании не было статистически значимого увеличения частоты заранее определенных нежелательных явлений, включая рак (9,4% для GOLTOR, 9,5% для плацебо), гепатит, холецистэктомию или осложнения, связанные с камнями в желчном пузыре или панкреатит.
Диагностические исследования
В исследованиях комбинированного дозирования частота клинически значимых повышений сывороточных трансаминаз (ALT и / или AST ≥ 3 X ULN, последовательные значения) составляла 1,7% у пациентов, получавших GOLTOR. Эти повышения обычно были бессимптомными. Не были связаны с холестазом и вернулись. до исходного уровня после прекращения терапии или во время курса лечения (см. раздел 4.4).
Клинически значимое увеличение CK (≥ 10 X ULN) наблюдалось у 0,2% пациентов, получавших GOLTOR.
Постмаркетинговый опыт
О следующих дополнительных нежелательных эффектах сообщалось при постмаркетинговом использовании с GOLTOR или в клинических испытаниях, или во время постмаркетингового использования с одним из отдельных компонентов.
Нарушения со стороны крови и лимфатической системы: тромбоцитопения; анемия
Со стороны нервной системы: периферическая невропатия; нарушение памяти
Со стороны дыхательной системы, грудной клетки и средостения: кашель; одышка; интерстициальное заболевание легких (см. раздел 4.4)
Со стороны желудочно-кишечного тракта: запоры; панкреатит; гастрит
Со стороны кожи и подкожной клетчатки: алопеция; многоформная эритема; реакции гиперчувствительности, включая сыпь, крапивницу, анафилаксию, ангионевротический отек
Со стороны опорно-двигательного аппарата и соединительной ткани: мышечные спазмы; миопатия * (включая миозит); рабдомиолиз с острой почечной недостаточностью или без нее (см. раздел 4.4); тендинопатия, иногда осложняющаяся разрывом
* В клиническом исследовании миопатия чаще возникала у пациентов, получавших симвастатин в дозе 80 мг / день, по сравнению с пациентами, получавшими 20 мг / день (1,0% против 0,02%, соответственно) (см. Разделы 4.4 и 4.5).
Нарушения обмена веществ и питания: снижение аппетита.
Сосудистые расстройства: приливы; гипертония
Общие расстройства и состояния в месте введения: боль
Со стороны печени и желчевыводящих путей: гепатит / желтуха; фатальная и нефатальная печеночная недостаточность; желчекаменная болезнь; холецистит
Нарушения со стороны репродуктивной системы и груди: эректильная дисфункция
Психиатрические расстройства: депрессия, бессонница.
Редко сообщалось о явном синдроме гиперчувствительности, в том числе о некоторых из следующих: ангионевротический отек, волчаночный синдром, ревматическая полимиалгия, дерматомиозит, васкулит, тромбоцитопения, эозинофилия, повышенная скорость оседания эритроцитов, артрит и артралгия, гиперчувствительность, лихорадка, светочувствительность. хрипы и недомогание.
Исследования: повышенная щелочная фосфатаза; аномальный тест функции печени.
Сообщалось о повышении уровня HbA1c и уровня глюкозы в сыворотке крови натощак при приеме статинов, включая симвастатин.
Были редкие постмаркетинговые сообщения о когнитивных нарушениях (например, потеря памяти, забывчивость, амнезия, нарушение памяти, спутанность сознания), связанных с использованием статинов, включая симвастатин. Сообщения, как правило, были несерьезными и обратимыми после прекращения терапии статинами. с разным временем появления симптомов (от 1 дня до нескольких лет) и разрешением симптомов (в среднем 3 недели).
Сообщалось о следующих дополнительных побочных эффектах при приеме некоторых статинов:
• Нарушения сна, включая кошмары.
• Сексуальная дисфункция.
• Сахарный диабет: частота будет зависеть от наличия или отсутствия факторов риска (уровень глюкозы в крови натощак ≥ 5,6 ммоль / л, ИМТ> 30 кг / м2, повышенный уровень триглицеридов, гипертония в анамнезе).
04.9 Передозировка
ГОЛТОР
В случае передозировки следует применять симптоматические и поддерживающие меры. Одновременное введение эзетимиба (1000 мг / кг) и симвастатина (1000 мг / кг) хорошо переносилось в исследованиях острой пероральной токсичности на мышах и крысах. У этих животных не наблюдалось клинических признаков токсичности. Пероральная оценка LD50 для обоих видов: эзетимиб ≥ 1000 мг / кг / симвастатин ≥ 1000 мг / кг.
Эзетимиб
В клинических исследованиях введение эзетимиба в дозе 50 мг / день 15 здоровым предметам на срок до 14 дней или 40 мг / день 18 пациентам с первичной гиперхолестеринемией на срок до 56 дней, как правило, переносилось хорошо. Сообщалось о нескольких случаях передозировки; большинство из них не было связано с побочными эффектами. Сообщенные побочные эффекты не были серьезными. У животных не наблюдалось токсичности после приема однократных пероральных доз 5 000 мг / кг эзетимиба для крыс и мышей и 3 000 мг / кг для собак.
Симвастатин
Сообщалось о нескольких случаях передозировки; максимальная принятая доза составила 3,6 г. Все пациенты выздоровели без осложнений.
05.0 ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
05.1 Фармакодинамические свойства
Фармакотерапевтическая группа: ингибиторы HMG-CoA редуктазы в сочетании с другими фармакологическими агентами, которые изменяют липидный профиль.
Код УВД: C10BA02.
ГОЛТОР (эзетимиб / симвастатин) - это гиполипидемический продукт, который избирательно подавляет всасывание в кишечнике холестерина и родственных ему растительных стеролов и подавляет эндогенный синтез холестерина.
Механизм действия:
ГОЛТОР
Холестерин плазмы образуется в результате абсорбции в кишечнике и эндогенного синтеза. GOLTOR содержит эзетимиб и симвастатин, два гиполипидемических соединения с взаимодополняющими механизмами действия. GOLTOR снижает повышенный уровень общего холестерина (общий-C), LDL-C, аполипопротеина B (Apo B), триглицеридов (TG), холестерина липопротеинов невысокой плотности (C-non-HDL) и увеличивает холестерин высокой плотности. липопротеиды плотности (HDL-C) за счет двойного ингибирования абсорбции и синтеза холестерина.
Эзетимиб
Эзетимиб подавляет всасывание холестерина в кишечнике. Эзетимиб активен при пероральном приеме и имеет механизм действия, который отличается от других классов холестеринснижающих веществ (например, статинов, секвестрантов желчных кислот [смол], производных фиброевой кислоты и растительных станолов). Молекулярной мишенью эзетимиба является переносчик стеролов. , Niemann-Pick C1-Like 1 (NPC1L1), отвечает за поглощение в кишечнике холестерина и фитостеринов.
Эзетимиб локализуется на уровне щеточной каймы тонкого кишечника и тормозит всасывание холестерина, вызывая уменьшение пассажа кишечного холестерина в печень; статины снижают синтез холестерина в печени, и эти два различных механизма приводят к дополнительному снижению холестерина. В 2-недельном клиническом исследовании 18 пациентов с гиперхолестеринемией эзетимиб подавлял всасывание холестерина в кишечнике на 54% по сравнению с плацебо.
Был проведен ряд доклинических исследований для определения селективности эзетимиба в отношении ингибирования абсорбции холестерина. Эзетимиб ингибировал абсорбцию [14C] -холестерина, не влияя на абсорбцию триглицеридов, жирных кислот, желчных кислот, прогестерона, этинилэстрадиола и т. Д. или жирорастворимые витамины А и D.
Симвастатин
После перорального приема симвастатин, который представляет собой неактивный лактон, гидролизуется в печени до соответствующей активной формы бета-гидроксикислоты, которая обладает мощной ингибирующей активностью в отношении HMG-CoA-редуктазы (3-гидрокси-3-метилглутарил-КоА-редуктазы). Этот фермент катализирует превращение HMG-CoA в мевалонат, что является ранней и лимитирующей стадией биосинтеза холестерина.
Было показано, что симвастатин снижает как нормальную, так и повышенную концентрацию ХС-ЛПНП. ЛПНП формируется из липопротеинов очень низкой плотности (ЛПОНП) и в основном катаболизируется рецептором ЛПНП с высоким сродством (C-ЛПОНП) и индукцией рецептора ЛПНП, что приводит к снижению продукции и увеличению катаболизма Х-ЛПНП. Аполипопротеин B также существенно снижается во время лечения симвастатином. Симвастатин также умеренно повышает уровень ХС-ЛПВП и снижает уровень ТГ в плазме. В результате этих изменений соотношение между общим холестерином / ХС-ЛПВП и ХС-ЛПНП / Х-ЛПВП снижается.
КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
В контролируемых клинических испытаниях GOLTOR значительно снижал общий уровень холестерина, холестерина ЛПНП, апо B, триглицеридов и не-ЛПВП, а также повышал уровень холестерина ЛПВП у пациентов с гиперхолестеринемией.
Первичная гиперхолестеринемия
В 8-недельном двойном слепом плацебо-контролируемом исследовании 240 пациентов с гиперхолестеринемией, которые уже получали монотерапию симвастатином и не смогли достичь целевого уровня ХС-ЛПНП в соответствии с Национальной образовательной программой по холестерину (NCEP) (от 2, 6 до 4,1). ммоль / л [от 100 до 160 мг / дл в зависимости от исходных характеристик) были рандомизированы для приема 10 мг эзетимиба или плацебо в дополнение к уже существующей терапии симвастатином. не достигли исходного целевого уровня ХС-ЛПНП (~ 80%), значительно большее количество пациентов, рандомизированных в группу эзетимиба, получавшего симвастатин, достигли целевого уровня ХС-ЛПНП в конечной точке исследования по сравнению с пациентами, рандомизированными в группу плацебо, принимавшего одновременно с симвастатином, 76% и 21,5% соответственно.
Соответствующее снижение ХС-ЛПНП для эзетимиба или плацебо, вводимых одновременно с симвастатином, значительно различались (27% и 3% соответственно).
Кроме того, эзетимиб, вводимый одновременно с терапией симвастатином, значительно снижал общее количество C, Apo B, TG по сравнению с плацебо, вводимым одновременно с симвастатином.
В 24-недельном двойном слепом многоцентровом исследовании приняли участие 214 пациентов с сахарным диабетом 2 типа, получавших тиазолидиндионы (розиглитазон и пиоглитазон) минимум 3 месяца и симвастатин 20 мг минимум 6 недель со средним уровнем ХС ЛПНП 2,4. ммоль / л (93 мг / дл), были рандомизированы для приема либо симвастатина 40 мг, либо одновременного введения активных веществ, эквивалентных GOLTOR 10 мг / 20 мг. GOLTOR 10 мг / 20 мг был значительно более эффективным, чем удвоение дозы симвастатина до 40 мг в дальнейшем снижении ХС ЛПНП (-21% и 0%, соответственно), общего Х (-14% и -1%, соответственно), АпоВ (-14% и -2% соответственно) и C-не-ЛПВП (-20% и -2%, соответственно) по сравнению со снижением, наблюдаемым при приеме 20 мг симвастатина. Результаты для Х-ЛПВП и ТГ между двумя группы лечения существенно не различались, и на результаты не влиял тип лечения тиазолидиндионами.
Эффективность различных доз GOLTOR (от 10 мг / 10 мг до 10 мг / 80 мг / день) была продемонстрирована в 12-недельном двойном слепом плацебо-контролируемом многоцентровом исследовании, которое включало все доступные дозы GOLTOR и все связанные дозировки симвастатина.
При сравнении пациентов, получавших все дозы GOLTOR, с пациентами, получавшими все дозы симвастатина, GOLTOR значительно снизил общий-C, LDL-C и TG (см. Таблицу 1), а также Apo B (-42% и -29%, соответственно) , не-HDL-C (-49% и -34%, соответственно) и C-реактивный белок (-33% и -9%, соответственно). Эффекты GOLTOR на HDL-C были аналогичны эффектам, наблюдаемым при применении симвастатина. Дальнейший анализ показал, что GOLTOR значительно повысил уровень ХС-ЛПВП по сравнению с плацебо.
Таблица 1
Ответ на GOLTOR у пациентов с первичной гиперхолестеринемией
(среднее изменение% от исходного уровня при отсутствии леченияb)
a Для триглицеридов среднее отклонение в% от исходного уровня
b Базальный - не используется при лечении гиполипидемическими препаратами
c Комбинированные дозы GOLTOR (10 / 10-10 / 80) значительно снижали общий уровень C, LDL-C и TG по сравнению с симвастатином и значительно повышали уровень HDL-C по сравнению с плацебо.
В аналогичном исследовании результаты по всем липидным параметрам в целом согласовывались. В комбинированном анализе этих двух исследований липидный ответ на GOLTOR был сходным у пациентов с уровнем триглицеридов выше или ниже 200 мг / дл.
В многоцентровом двойном слепом контролируемом клиническом исследовании (ENHANCE) 720 пациентов с гетерозиготной семейной гиперхолестеринемией были рандомизированы для получения эзетимиба 10 мг в комбинации с 80 мг симвастатина (n = 357) или симвастатина 80 мг (n = 363) на двоих. годы. Основная цель исследования состояла в том, чтобы изучить влияние комбинированной терапии эзетимиб / симвастатин на толщину внутренней оболочки и среды (IMT) сонной артерии по сравнению с одним симвастатином. Влияние этого маркера еще не продемонстрировано. сердечно-сосудистой заболеваемости и смертности.
Первичная конечная точка, среднее изменение IMT всех шести сегментов сонной артерии, не различалась достоверно (p = 0,29) между двумя группами лечения на основе измерений ультразвука в B-режиме. При применении эзетимиба 10 мг в сочетании с 80 мг симвастатина или 80 мг только симвастатина толщина интимы и медиальной оболочки увеличивалась на 0,0111 мм и 0,0058 мм, соответственно, в течение 2-летнего периода исследования (на исходном уровне среднее значение ТИМ сонной артерии составляло 0,68 мм и 0,69 мм соответственно).
Эзетимиб 10 мг в комбинации с 80 мг симвастатина снижал уровень ХС-ЛПНП, общий -С, Апо В и ТГ значительно больше, чем 80 мг симвастатина. Для двух групп лечения процентное увеличение Х-ЛПВП было одинаковым. Нежелательные реакции, о которых сообщалось при приеме 10 мг эзетимиба в сочетании с 80 мг симвастатина, соответствовали его известному профилю безопасности.
ГОЛТОР содержит симвастатин. В двух крупных плацебо-контролируемых клинических испытаниях: Скандинавское исследование выживаемости с симвастатином (20-40 мг n = 4444 пациента) e Исследование защиты сердца (40 мг; N = 20 536 пациентов), эффект терапии симвастатином оценивался у пациентов с высоким риском коронарных событий из-за продолжающейся ишемической болезни сердца, диабета, заболевания периферических сосудов, инсульта в анамнезе или других цереброваскулярных заболеваний. Лечение симвастатином имеет было показано, что он снижает: риск общей смертности за счет снижения смертности от ИБС; риск нефатального инфаркта миокарда и инсульта; и необходимость хирургического вмешательства с процедурами коронарной и некоронарной реваскуляризации.
В исследовании эффективности дополнительного снижения уровня холестерина и гомоцистеина (ПОИСК) оценивалось влияние лечения симвастатином 80 мг по сравнению с 20 мг (средний период наблюдения 6,7 лет) на основные сосудистые события (MVE; определяемые как фатальная ишемия сердца. болезнь, нефатальный инфаркт миокарда, процедура коронарной реваскуляризации, нефатальный или смертельный инсульт или процедура периферической реваскуляризации) у 12064 пациентов с инфарктом миокарда в анамнезе. Существенной разницы в частоте МВЭ между 2 группами не было; симвастатин 20 мг (n = 1553; 25,7%) по сравнению с 80 мг симвастатина (n = 1477; 24,5%); ОР 0,94, 95% ДИ: 0,88: 1,01. Абсолютная разница в уровне ХС-ЛПНП между двумя группами по сравнению с курс исследования составлял 0,35 ± 0,01 ммоль / л. Профили безопасности были одинаковыми между двумя группами лечения, за исключением «частоты миопатии, которая составляла приблизительно 1,0% для пациентов, получавших симвастатин 80 мг по сравнению с 0,02% для пациентов, получавших 20 мг. Примерно половина этих случаев миопатии произошла в течение первого года лечения. Частота миопатии в течение каждого последующего года лечения составляла примерно 0,1%.
Было показано, что GOLTOR снижает количество серьезных сердечно-сосудистых событий у пациентов с хроническим заболеванием почек; тем не менее, увеличение эффективности GOLTOR в отношении сердечно-сосудистых заболеваний и смертности по сравнению с показателем для симвастатина окончательно не установлено.
Клинические исследования на педиатрических пациентах (от 10 до 17 лет)
В многоцентровом двойном слепом контролируемом исследовании участвовали 142 мальчика (стадия Таннера II и выше) и 106 девочек в постменархе в возрасте от 10 до 17 лет (средний возраст 14,2 года) с гетерозиготной семейной гиперхолестеринемией (гетерозиготная ПФ) с исходным уровнем ХС-ЛПНП. значения между 4,1 и 10,4 ммоль / л были рандомизированы для приема 10 мг эзетимиба одновременно с симвастатином (10, 20 или 40 мг) или симвастатином (10, 20 или 40 мг) отдельно в течение 6 недель, эзетимибом и 40 мг симвастатина одновременно. - вводили или вводили только симвастатин 40 мг в течение следующих 27 недель, а затем совместно вводили эзетимиб и симвастатин (10 мг, 20 мг или 40 мг) открыто в течение 20 недель.
На 6 неделе эзетимиб, вводимый совместно с симвастатином (все дозы), значительно снизил общий холестерин-C (38% против 26%), LDL-C (49% против 34%), Apo B (39% против 27%) и не- ХС-ЛПВП (47% против 33%) по сравнению с одним симвастатином (все дозы). Результаты были одинаковыми для двух групп лечения ТГ и ХС-ЛПВП (-17% против -12% и + 7% против + 6%, соответственно. На 33-й неделе результаты соответствовали результатам 6-й недели, и значительно большее количество пациентов, получавших эзетимиб и симвастатин в дозе 40 мг (62%), достигли «идеальной терапевтической цели в соответствии с NCEP AAP» (
Безопасность и эффективность эзетимиба, вводимого одновременно с симвастатином в дозах более 40 мг в день, не изучались у педиатрических пациентов в возрасте от 10 до 17 лет. Эффективность не изучалась у пациентов младше 17 лет. Длительная терапия эзетимибом в снижении заболеваемости и смертности в зрелом возрасте.
Гомозиготная семейная гиперхолестеринемия (гомозиготный IF)
Было проведено 12-недельное двойное слепое рандомизированное исследование с участием пациентов с клиническим и / или генотипическим диагнозом гомозиготного ИФ. Были проанализированы данные подгруппы пациентов (n = 14), получавших симвастатин в дозе 40 мг на исходном уровне. Увеличение дозировки симвастатина с 40 до 80 мг (n = 5) привело к снижению уровня ХС-ЛПНП на 13% по сравнению с исходным уровнем по сравнению с 40 мг симвастатина. Совместное введение эзетимиба и симвастатина, эквивалентного GOLTOR (10 мг / 40 мг и 10 мг. / 80 мг в сочетании, n = 9) привело к снижению уровня ХС-ЛПНП на 23% по сравнению с исходным уровнем по сравнению с 40 мг симвастатина. ), снижение уровня ХС-ЛПНП на 29% от исходного уровня было получено по сравнению с 40 мг симвастатина.
Профилактика серьезных сосудистых событий при хронической болезни почек (ХБП)
Исследование защиты сердца и почек (SHARP) было многонациональным рандомизированным плацебо-контролируемым двойным слепым исследованием с участием 9438 пациентов с хроническим заболеванием почек, одна треть из которых находилась на диализе в начале исследования. В общей сложности 4650 пациентов были отнесены к группе GOLTOR 10/20, а 4620 - к группе плацебо, а средний срок наблюдения составил 4,9 года.Средний возраст пациентов составлял 62 года, из них 63% составляли мужчины, 72% - европеоид, 23% - страдали диабетом, а для тех, кто не находился на диализе, средняя расчетная скорость клубочковой фильтрации (рСКФ) составляла 26,5 мл / мин / 1,73 м2. Отсутствие критерия включения в исследование на основе липидов. Среднее исходное значение ХС ЛПНП составляло 108 мг / дл. Через год, включая пациентов, больше не принимавших исследуемый препарат, ХС ЛПНП снизился на 26% по сравнению с плацебо при применении только симвастатина в дозе 20 мг и на 38%. % по GOLTOR 10/20 мг.
Первичное сравнение, указанное в протоколе SHARP, представляло собой «анализ намерения лечить« основные сосудистые события »(MVE; определяемый как нефатальный инфаркт миокарда или сердечная смерть, инсульт или любая процедура реваскуляризации) только у тех пациентов, которые первоначально были рандомизированы. в группы GOLTOR (n = 4 193) или плацебо (n = 4 191). Вторичный анализ включал тот же композит, проанализированный для всей рандомизированной когорты (исходный уровень исследования или 1 год) для GOLTOR (n = 4650) или плацебо (n = 4620), как а также компоненты этого композита.
Анализ первичных конечных точек показал, что GOLTOR значительно снизил риск серьезных сосудистых событий (749 пациентов в группе плацебо против 639 в группе GOLTOR) с относительным снижением риска на 16% (p = 0,001).
Однако дизайн этого исследования не учитывал отдельного вклада монокомпонентного эзетимиба в эффективность для значительного снижения риска серьезных сосудистых событий у пациентов с ХБП.
Отдельные компоненты MVE у всех рандомизированных пациентов показаны в таблице 2. GOLTOR значительно снизил риск инсульта и любой реваскуляризации без значительных численных различий в пользу GOLTOR для нефатального инфаркта миокарда и сердечной смерти.
Таблица 2
Основные сосудистые события по группам лечения у всех рандомизированных пациентов в SHARPa
a Анализ по намерению лечить всех пациентов SHARP, рандомизированных в GOLTOR или плацебо на исходном уровне или через 1 год
b MAE; определяется как совокупность нефатального инфаркта миокарда, коронарной смерти, негеморрагического инсульта или любой реваскуляризации
Абсолютное снижение холестерина ЛПНП, достигнутое с помощью GOLTOR, было ниже среди пациентов с более низким исходным уровнем ХС ЛПНП (
Стеноз аорты
Симвастатин и эзетимиб для лечения стеноза аорты (SEAS) было многоцентровым двойным слепым плацебо-контролируемым исследованием со средней продолжительностью 4,4 года с участием 1873 пациентов с бессимптомным стенозом аорты (СА), подтвержденным пиковой скоростью аортального кровотока, измеренной с помощью Доплеровский диапазон от 2,5 до 4,0 м / с. Были включены только пациенты, для которых лечение статинами не считалось необходимым для снижения риска атеросклеротического сердечно-сосудистого заболевания. Пациенты были рандомизированы в соотношении 1: 1 для одновременного приема 10 мг плацебо или эзетимиба и 40 мг симвастатина.
Первичной конечной точкой была совокупность основных сердечно-сосудистых событий (MCE), включая смерть от сердечно-сосудистых заболеваний, хирургическое протезирование аортального клапана (AVR), застойную сердечную недостаточность (CHF) в результате прогрессирования AS, нефатальный инфаркт миокарда, аортокоронарное шунтирование (CABG). )), чрескожное коронарное вмешательство (ЧКВ), госпитализация по поводу нестабильной стенокардии и негеморрагический инсульт. Ключевыми вторичными конечными точками были составные подмножества категорий событий первичной конечной точки.
По сравнению с плацебо, эзетимиб / симвастатин 10/40 мг существенно не снижал риск MCE. Первичный результат наступил у 333 пациентов (35,3%) в группе эзетимиба / симвастатина и у 355 пациентов (38,2%) в группе плацебо (отношение рисков в группе эзетимиб / симвастатин, 0,96; доверительный интервал 95%, 0,83–1,12; p = 0,59) Замена аортального клапана была выполнена 267 пациентам (28,3%) в группе эзетимиб / симвастатин и 278 пациентам (29,9%) в группе плацебо (отношение рисков 1,00; 95% ДИ 0,84–1,18; p = 0,97). В группе эзетимиба / симвастатина (n = 148) у меньшего числа пациентов были ишемические сердечно-сосудистые события (n = 148) по сравнению с группой плацебо (n = 187) (отношение рисков 0,78; 95% ДИ от 0,63 до 0,97; p = 0,02), в основном из-за меньшему количеству пациентов, которым было выполнено шунтирование коронарной артерии.
Рак чаще встречался в группе эзетимиба / симвастатина (105 против 70, p = 0,01). Клиническая значимость этого наблюдения сомнительна, поскольку в более крупном исследовании SHARP общее количество пациентов с любым типом рака (438 в группе эзетимиб / симвастатин по сравнению с 439 в группе плацебо) не отличалось, и, следовательно, результат SEAS исследование не может быть подтверждено SHARP.
05.2 Фармакокинетические свойства
При одновременном применении эзетимиба и симвастатина значительных фармакокинетических взаимодействий не наблюдалось.
Абсорбция :
ГОЛТОР
ГОЛТОР является биоэквивалентным одновременному применению эзетимиба и симвастатина.
Эзетимиб
После перорального приема эзетимиб быстро и интенсивно всасывается в сочетании с фармакологически активным фенольным глюкуронидом (эзетимиб-глюкуронид). Средние пиковые концентрации в плазме (Cmax) наблюдаются в течение 1-2 часов для эзетимиб-глюкуронида и 4-12 часов для эзетимиба. Абсолютная биодоступность эзетимиба не может быть определена, поскольку соединение практически нерастворимо в водной среде, подходящей для инъекций.
Одновременный прием пищи (с высоким содержанием жиров или обезжиренной пищи) не влиял на пероральную биодоступность эзетимиба в таблетках по 10 мг.
Симвастатин
Было обнаружено, что доступность активной α-гидроксикислоты в системный кровоток после перорального приема дозы симвастатина составляет менее 5% от дозы, что согласуется с экстенсивной экстракцией через печень. Основные метаболиты симвастатина, присутствующие в плазме крови человека: -гидроксикислота и четыре других активных метаболита.
Профили общих и активных ингибиторов в плазме не изменились при введении симвастатина непосредственно перед стандартным приемом пищи по сравнению с приемом натощак.
Распределение :
Эзетимиб
Эзетимиб и эзетимиб-глюкуронид связываются с белками плазмы человека на 99,7% и 88-92% соответственно.
Симвастатин
И симвастатин, и? -Гидроксикислота связываются с белками плазмы человека (95%).
Фармакокинетика однократного и многократного приема симвастатина не показала кумуляции препарата после многократного приема. Во всех вышеуказанных фармакокинетических исследованиях максимальная концентрация ингибиторов наблюдалась через 1,3–2,4 часа после приема дозы.
Биотрансформация :
Эзетимиб
Эзетимиб метаболизируется в основном в тонком кишечнике и печени посредством конъюгации глюкуронида (реакция фазы II) с последующей экскрецией с желчью. Минимальный окислительный метаболизм (реакция фазы I) наблюдался у всех оцениваемых видов. Эзетимиб и эзетимиб-глюкуронид являются основными производными лекарственного средства, обнаруженными в плазме крови, составляя примерно 10-20% и 80-90% от общего количества лекарственного средства, присутствующего в плазме, соответственно.Эзетимиб и эзетимиб-глюкуронид медленно выводятся из плазмы, что доказано значительного энтерогепатического цикла Период полувыведения эзетимиба и эзетимиб-глюкуронида составляет примерно 22 часа.
Симвастатин
Симвастатин - это неактивный лактон, который быстро гидролизуется. in vivo в соответствующей α-гидроксикислоте, сильном ингибиторе HMG-CoA редуктазы. Гидролиз происходит в основном в печени; скорость гидролиза в плазме человека очень низкая.
У людей симвастатин хорошо всасывается и быстро экстрагируется в печени. Экстракция в печени зависит от кровотока в печени. Печень является его основным местом действия с последующим выведением эквивалентных веществ с желчью. Поэтому доступность активного препарата в системном кровотоке низкая.
После внутривенного введения метаболита β-гидроксикислоты его средний период полувыведения составил 1,9 часа.
Устранение :
Эзетимиб
После перорального введения эзетимиба 14С (20 мг) людям общий эзетимиб составлял приблизительно 93% от общей радиоактивности плазмы. Приблизительно 78% и 11% введенной радиоактивности было извлечено с фекалиями и мочой, соответственно, в течение 10-дневного периода сбора образцов.После 48 часов не было обнаружено уровней радиоактивности в плазме.
Симвастатин
Симвастатиновая кислота активно транспортируется в гепатоциты через носитель OATP1B1.
После приема пероральной дозы симвастатина людям 13% радиоактивности выводилось с мочой и 60% с фекалиями в течение 96 ч. Количество, обнаруженное в фекалиях, представляет собой эквивалентные вещества, выделяемые с желчью, а также неабсорбированное лекарственное средство. После внутривенного введения метаболита β-гидроксикислоты только 0,3% внутривенной дозы выводилось с мочой в качестве ингибиторов.
Особые группы населения:
Педиатрические пациенты
Абсорбция и метаболизм эзетимиба у детей и подростков (от 10 до 18 лет) и взрослых одинаковы. На основании общего эзетимиба нет фармакокинетических различий между подростками и взрослыми.Фармакокинетические данные ситостеролемии в педиатрической популяции (см. Раздел 4.2).
Гериатрические пациенты
Концентрации общего эзетимиба в плазме крови примерно вдвое выше у пожилых людей (≥ 65 лет), чем у молодых (18-45 лет). Снижение уровня холестерина ЛПНП и профиль безопасности сопоставимы между пожилыми и более молодыми людьми, получавшими эзетимиб (см. Раздел 4.2. ).
Печеночная недостаточность
После введения однократной дозы эзетимиба 10 мг средняя площадь под кривой (AUC) для общего эзетимиба увеличилась примерно в 1,7 раза у пациентов с легким нарушением функции печени (5 или 6 баллов по шкале Чайлд-Пью) по сравнению со здоровыми субъектами. В 14-дневном исследовании с применением многократных доз (10 мг / день) у пациентов с умеренной печеночной недостаточностью (оценка по шкале Чайлд-Пью от 7 до 9) средняя AUC для общего эзетимиба увеличивалась примерно 4 раза в день 1 и на 14 день по сравнению со здоровыми субъектами. У пациентов с печеночной недостаточностью легкой степени коррекции дозы не требуется. Из-за неизвестных эффектов повышенного воздействия эзетимиба у пациентов с умеренной или тяжелой печеночной недостаточностью (оценка по шкале Чайлд-Пью> 9), эзетимиб не рекомендуется этим пациентам (см. Разделы 4.2 и 4.4).
Почечная недостаточность
Эзетимиб
После однократного приема 10 мг эзетимиба у пациентов с тяжелым заболеванием почек (n = 8; среднее значение CrCl ≤ 30 мл / мин) средняя AUC для общего эзетимиба увеличилась примерно в 1,5 раза по сравнению со здоровыми субъектами (n = 9). (см. раздел 4.2).
Еще один пациент в этом исследовании (после трансплантации почки и получавший несколько лекарственных препаратов, включая циклоспорин) имел 12-кратную «экспозицию» общего эзетимиба.
Симвастатин
В исследовании с участием пациентов с тяжелой почечной недостаточностью (клиренс креатинина
Секс
Концентрации общего эзетимиба в плазме крови у женщин несколько выше (примерно на 20%), чем у мужчин. Снижение уровня ХС-ЛПНП и профиль безопасности сопоставимы между мужчинами и женщинами, получавшими эзетимиб.
Полиморфизм SLCO1B1
Носители аллеля c.521T> C гена SLCO1B1 обладают пониженной активностью OATP1B1. Среднее воздействие (AUC) основного активного метаболита, симвастатиновой кислоты, составляет 120% у гетерозиготных носителей аллеля C (CT) и 221% у гомозиготные носители (CC) по сравнению с пациентами с наиболее распространенным генотипом (TT). Аллель C имеет частоту 18% в европейской популяции. Существует риск повышенного воздействия симвастатиновой кислоты у пациентов с полиморфизмом SLCO1B1, что может привести к повышенному риску рабдомиолиза (см. Раздел 4.4).
05.3 Доклинические данные по безопасности
ГОЛТОР
В исследованиях одновременного приема эзетимиба и симвастатина наблюдаемые токсические эффекты были в основном теми, которые обычно связаны со статинами. Некоторые из токсических эффектов были более выраженными, чем при лечении только статинами. Это связано с фармакокинетическими и / или фармакодинамическими взаимодействиями при одновременном применении. В клинических исследованиях такого рода взаимодействий не наблюдалось. Эпизоды миопатии возникали у крыс только после воздействия доз, в несколько раз превышающих терапевтическую дозу для людей (примерно в 20 раз выше уровня AUC для симвастатина и в 1800 раз выше уровня AUC для активного метаболита). Не было доказательств того, что сопутствующий прием эзетимиба каким-либо образом влиял на миотоксический потенциал симвастатина.
У собак совместно с эзетимибом и статинами при низких дозах (гиперплазия желчных протоков, накопление пигмента, инфильтрация мононуклеарных клеток и небольшие гепатоциты). Эти изменения не развивались при длительном воздействии доз до 14 месяцев. После прекращения воздействия наблюдалось общее восстановление результатов печеночных тестов. Эти данные согласуются с данными, описанными для ингибиторов HMG-CoA, или объясняются очень низким уровнем холестерина, достигнутым у исследуемых собак.
Одновременное введение эзетимиба и симвастатина не было тератогенным у крыс. У беременных самок кроликов наблюдалось ограниченное количество деформаций скелета (сращение хвостовых позвонков, уменьшение количества хвостовых позвонков).
В серии очерков in vivo А также in vitro Эзетимиб, вводимый отдельно или совместно с симвастатином, не проявлял генотоксического потенциала.
Эзетимиб
Исследования хронической токсичности эзетимиба на животных не выявили органы-мишени для токсических эффектов. У собак, получавших эзетимиб в течение 4 недель (≥ 0,03 мг / кг / день), концентрация холестерина в желчи увеличивалась в 2,5–3,5 раза. Однако в течение одного года исследования на собаках, получавших дозы до 300 мг / кг / день, не наблюдалось увеличения частоты холелитиаза или других гепатобилиарных эффектов. Клиническая ценность этих данных для людей неизвестна. Нельзя исключить риск литогенеза, связанный с терапевтическим применением эзетимиба.
Долгосрочные тесты на канцерогенность эзетимиба были отрицательными.
Эзетимиб не влиял на фертильность крыс обоих полов, тератогенность у крыс и кроликов не обнаруживалась, а также не изменялось пре- или постнатальное развитие. Эзетимиб преодолевал плацентарный барьер у самок крыс и беременных кроликов, получавших многократные дозы по 1000 мг / сут. кг / сут.
Симвастатин
Основываясь на традиционных исследованиях фармакодинамики, токсичности многократных доз, генотоксичности и канцерогенеза на животных, нет никаких рисков для пациента, кроме тех, которые ожидаются на основе фармакологического механизма. В максимально переносимых дозах как у крыс, так и у кроликов симвастатин не приводил к порокам развития плода и не влиял на фертильность, репродуктивную функцию или развитие новорожденных.
06.0 ФАРМАЦЕВТИЧЕСКАЯ ИНФОРМАЦИЯ
06.1 Вспомогательные вещества
Бутилгидроксианизол
Моногидрат лимонной кислоты
Кроскармеллоза натрия
Гипромеллоза
Моногидрат лактозы
Стеарат магния
Микрокристаллическая целлюлоза
Пропилгаллат
06.2 Несовместимость
Не имеет значения.
06.3 Срок действия
2 года.
06.4 Особые меры предосторожности при хранении
Не хранить при температуре выше 30 ° C.
Волдырь: Хранить в оригинальной упаковке для защиты от света и влаги.
Бутылки: Держите флакон плотно закрытым, чтобы защитить лекарство от света и влаги.
06.5 Характер непосредственной упаковки и содержимого упаковки
ГОЛТОР 10 мг / 10 мг, 10 мг / 20 мг и 10 мг / 40 мг
Белая бутылка из полиэтилена высокой плотности (HDPE) с закрывающейся крышкой из полипропилена с защитой от детей и осушающим силиконовым гелем, запечатанная специальной этикеткой, содержащая 100 таблеток.
ГОЛТОР 10 мг / 10 мг
Блистер из ПВХ / алюминиевого полиамида, приваренный к алюминиевой фольге с помощью виниловой смолы. Таблетки можно извлечь, нажав на пластиковый карман.Пакеты по 7, 10, 14, 28, 30, 50, 56, 84, 98, групповые упаковки по 98 (2 коробки по 49), 100 или 300 таблеток.
Блистер на одну дозу из ПВХ / алюминиевого полиамида, приваренного к алюминиевой фольге с использованием виниловой смолы. Таблетки можно извлечь, надавив на пластиковый карман в упаковке по 30, 50, 100 или 300 таблеток.
ГОЛТОР 10 мг / 20 мг, 10 мг / 40 мг
Непрозрачный блистер из полихлортрифторэтилена / ПВХ, запечатанный на алюминиевой фольге виниловой смолой. Таблетки можно извлечь, нажав на пластиковый карман. Упаковка из 90 таблеток.
ГОЛТОР 10 мг / 20 мг, 10 мг / 40 мг и 10 мг / 80 мг
Непрозрачный блистер из полихлортрифторэтилена / ПВХ, запечатанный на алюминиевой фольге виниловой смолой. Таблетки можно извлечь, нажав на пластиковый карман.Пакеты по 7, 10, 14, 28, 30, 50, 56, 84, 98, 100 или 300 таблеток.
Блистерная упаковка из полихлортрифторэтилена / ПВХ для однократной дозы, запаянная на алюминиевой фольге виниловой смолой. Таблетки можно извлечь, надавив на пластиковый карман в упаковке по 30, 50, 100 или 300 таблеток.
Не все размеры упаковки могут быть проданы.
06.6 Инструкции по эксплуатации и обращению
Никаких особых инструкций.
07.0 ДЕРЖАТЕЛЬ РАЗРЕШЕНИЯ НА МАРКЕТИНГ
ДОБАВИТЬ PHARMA Srl
Виале Шекспир, 47
00144 Рим
Дилер на продажу:
СИГМА-ТАУ Индустри Фармацевтика Риуните С.п.А.
Виа Понтина, км 30,400
00040 Помеция (РМ)
08.0 НОМЕР РАЗРЕШЕНИЯ НА МАРКЕТИНГ
100 таблеток во флаконе 10 мг / 10 мг АПК н. 036678011
7 таблеток в контурной ячейковой упаковке по 10 мг / 10 мг АПК н. 036678023
10 таблеток в контурной ячейковой упаковке по 10 мг / 10 мг АПК н. 036678035
14 таблеток в контурной ячейковой упаковке по 10 мг / 10 мг АПК н. 036678047
28 таблеток в контурной ячейковой упаковке по 10 мг / 10 мг АПК н. 036678050
30 таблеток в контурной ячейковой упаковке по 10 мг / 10 мг АПК н. 036678100
50 таблеток в контурной ячейковой упаковке по 10 мг / 10 мг АПК н. 036678062
56 таблеток в контурной ячейковой упаковке по 10 мг / 10 мг АПК н. 036678074
98 таблеток в контурной ячейковой упаковке по 10 мг / 10 мг АПК н. 036678086
2 х 49 таблеток в контурной ячейковой упаковке по 10 мг / 10 мг АПК н. 036678643
100 таблеток в блистерах по 10 мг / 10 мг АПК н. 036678098
300 таблеток в контурной ячейковой упаковке по 10 мг / 10 мг АПК н. 036678112
30 таблеток в блистерах для однократного приема 10 мг / 10 мг AIC n. 036678124
50 таблеток в блистерах для однократного приема 10 мг / 10 мг AIC n. 036678136
100 таблеток в блистерах для однократного приема по 10 мг / 10 мг AIC n. 036678148
300 таблеток в блистерах для однократного приема 10 мг / 10 мг AIC n. 036678163
100 таблеток во флаконе 10 мг / 20 мг АПК н. 036678151
7 таблеток в контурной ячейковой упаковке по 10 мг / 20 мг АПК н. 036678175
10 таблеток в контурной ячейковой упаковке по 10 мг / 20 мг АПК н. 036678187
14 таблеток в контурной ячейковой упаковке по 10 мг / 20 мг АПК н. 036678199
28 таблеток в контурной ячейковой упаковке по 10 мг / 20 мг АПК н. 036678201
30 таблеток в контурной ячейковой упаковке по 10 мг / 20 мг АПК н. 036678213
50 таблеток в контурной ячейковой упаковке по 10 мг / 20 мг АПК н. 036678225
56 таблеток в контурной ячейковой упаковке по 10 мг / 20 мг АПК н. 036678237
98 таблеток в контурной ячейковой упаковке по 10 мг / 20 мг АПК н. 036678249
100 таблеток в блистерах по 10 мг / 20 мг АПК н. 036678252
300 таблеток в контурной ячейковой упаковке по 10 мг / 20 мг АПК н. 036678264
30 таблеток в блистерах для однократного приема 10 мг / 20 мг AIC n. 036678276
50 таблеток в блистерах для однократного приема 10 мг / 20 мг AIC n. 036678288
100 таблеток в блистерах для однократного приема 10 мг / 20 мг AIC n. 036678290
300 таблеток в блистерах для однократного приема 10 мг / 20 мг AIC n. 036678302
100 таблеток во флаконе 10 мг / 40 мг AIC n. 036678314
7 таблеток в контурной ячейковой упаковке по 10 мг / 40 мг АПК н. 036678326
10 таблеток в контурной ячейковой упаковке по 10 мг / 40 мг АПК н. 036678338
14 таблеток в контурной ячейковой упаковке по 10 мг / 40 мг АПК н. 036678340
28 таблеток в контурной ячейковой упаковке по 10 мг / 40 мг АПК н. 036678353
30 таблеток в контурной ячейковой упаковке по 10 мг / 40 мг АПК н. 036678365
50 таблеток в контурной ячейковой упаковке по 10 мг / 40 мг АПК н. 036678377
56 таблеток в контурной ячейковой упаковке по 10 мг / 40 мг АПК н. 036678389
98 таблеток в контурной ячейковой упаковке по 10 мг / 40 мг АПК н. 036678391
100 таблеток в блистерах по 10 мг / 40 мг АПК н. 036678403
300 таблеток в контурной ячейковой упаковке по 10 мг / 40 мг АПК н. 036678415
30 таблеток в блистерах для однократного приема 10 мг / 40 мг AIC n. 036678427
50 таблеток в блистерах для однократного приема по 10 мг / 40 мг AIC n. 036678439
100 таблеток в блистерах для однократного приема по 10 мг / 40 мг AIC n. 036678441
300 таблеток в блистерах для однократного приема по 10 мг / 40 мг AIC n. 036678454
7 таблеток в контурной ячейковой упаковке по 10 мг / 80 мг АПК н. 036678466
10 таблеток в контурной ячейковой упаковке по 10 мг / 80 мг АПК н. 036678478
14 таблеток в контурной ячейковой упаковке по 10 мг / 80 мг АПК н. 036678480
28 таблеток в блистерах по 10 мг / 80 мг АПК н. 036678492
30 таблеток в контурной ячейковой упаковке по 10 мг / 80 мг АПК н. 036678504
50 таблеток в блистерах по 10 мг / 80 мг АПК н. 036678516
56 таблеток в контурной ячейковой упаковке по 10 мг / 80 мг АПК н. 036678528
98 таблеток в контурной ячейковой упаковке по 10 мг / 80 мг АПК н. 036678530
100 таблеток в контурной ячейковой упаковке по 10 мг / 80 мг АПК н. 036678542
300 таблеток в блистерах по 10 мг / 80 мг АПК н. 036678555
30 таблеток в блистерах для однократного приема по 10 мг / 80 мг AIC n. 036678567
50 таблеток в блистерах для однократного приема по 10 мг / 80 мг AIC n. 036678579
100 таблеток в блистерах для однократного приема по 10 мг / 80 мг AIC n. 036678581
300 таблеток в блистерах для однократного приема по 10 мг / 80 мг AIC n. 036678593
09.0 ДАТА ПЕРВОГО РАЗРЕШЕНИЯ ИЛИ ПРОДЛЕНИЯ РАЗРЕШЕНИЯ
Дата первого разрешения: август 2005 г.
Дата последнего обновления: февраль 2010 г.
10.0 ДАТА ПЕРЕСМОТРА ТЕКСТА
Март 2015 г.