Активные ингредиенты: Ритуксимаб.
Концентрат Мабтера 500 мг для приготовления раствора для инфузий
Пакеты-вкладыши Mabthera доступны для размеров упаковки:- Концентрат Мабтера 100 мг для приготовления раствора для инфузий
- Концентрат Мабтера 500 мг для приготовления раствора для инфузий
- Мабтера 1400 мг раствор для подкожного введения
Показания Почему применяется Мабтера? Для чего это?
Что такое Мабтера
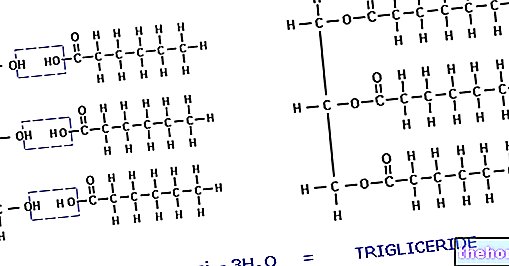
Мабтера содержит активное вещество «ритуксимаб», тип белка, называемого «моноклональным антителом», который связывается с поверхностью определенных белых кровяных телец, называемых В-лимфоцитами. Когда ритуксимаб связывается с поверхностью этих клеток, он их убивает.
Для чего применяется Мабтера
Мабтера можно использовать для лечения многих заболеваний у взрослых. Ваш врач может назначить Мабтеру для лечения:
а) Неходжкинская лимфома
Неходжкинская лимфома - это заболевание лимфатической ткани (части иммунной системы), в которое вовлечены В-лимфоциты, особый тип белых кровяных телец.
Мабтеру можно назначать в виде монотерапии (отдельно) или с другими лекарствами, которые собирательно называются «химиотерапией».
У пациентов, лечение которых оказалось эффективным, Мабтера можно использовать в качестве поддерживающей терапии в течение 2 лет после завершения первоначального лечения.
б) Хронический лимфолейкоз
Хронический лимфолейкоз (ХЛЛ) является наиболее распространенной формой лейкемии взрослых. ХЛЛ включает особый лимфоцит, В-клетку, которая возникает в костном мозге и созревает в лимфатических узлах. У пациентов с ХЛЛ слишком много аномальных лимфоцитов, которые становятся ими. накапливаются в основном в костном мозге и в крови. Разрастание этих аномальных В-лимфоцитов является причиной симптомов, которые могут возникнуть у вас. Мабтера в сочетании с химиотерапией разрушает эти клетки, которые постепенно выводятся из организма биологическими процессами.
в) ревматоидный артрит
Мабтера используется для лечения ревматоидного артрита. Ревматоидный артрит - это заболевание, поражающее суставы. В-лимфоциты ответственны за некоторые из ваших симптомов. Мабтера используется для лечения ревматоидного артрита у людей, которые пробовали другие лекарства, но перестали работать, не работали достаточно хорошо или вызывали побочные эффекты. Мабтера обычно принимается с другим лекарством, называемым метотрексатом. Мабтера замедляет повреждение суставов, вызванное ревматоидным артритом. и увеличивает способность выполнять обычные повседневные дела.
Лучший ответ на Мабтеру наблюдался у тех, у кого был положительный анализ крови на ревматоидный фактор (РФ) и / или антициклический цитруллинированный пептид (анти-ЦЦП). Оба теста обычно положительны при ревматоидном артрите и помогают подтвердить диагноз.
г) Гранулематоз с полиангиитом и микроскопическим полиангиитом
Мабтера используется для индукции ремиссии гранулематоза с полиангиитом (формально называемого болезнью Вегенера) или микроскопического полиангиита в сочетании с глюкокортикоидами. Гранулематоз с полиангиитом и микроскопический полиангиит - это две формы воспаления кровеносных сосудов, которые в основном поражают легкие и почки. но может поражать и другие органы. Лимфоциты участвуют в возникновении этих состояний.
Противопоказания Когда нельзя применять Мабтеру
Не принимайте Мабтеру:
- если у вас аллергия на ритуксимаб, другие белки, аналогичные ритуксимабу, или любые другие ингредиенты этого лекарства (перечислены в разделе 6);
- если у вас в настоящее время «тяжелая активная инфекция»;
- если ваша иммунная система слабая;
- если у вас тяжелая сердечная недостаточность или тяжелое неконтролируемое заболевание сердца и ревматоидный артрит, гранулематоз с полиангиитом или микроскопический полиангиит.
Не принимайте Мабтеру, если к вам относится что-либо из вышеперечисленного. Если вы не уверены, проконсультируйтесь с врачом, фармацевтом или медсестрой, прежде чем принимать Мабтеру.
Меры предосторожности при применении Что следует знать перед приемом Мабтеры
Перед приемом мабтеры проконсультируйтесь со своим врачом, фармацевтом или медсестрой:
- если у вас была инфекция гепатита в прошлом или она может быть сейчас, так как в небольшом количестве случаев Мабтера может вызвать реактивацию гепатита B, что в очень редких случаях может быть фатальным. Пациенты с историей инфицирования гепатитом B будут находиться под пристальным наблюдением врача на предмет любых признаков этой инфекции;
- если вы когда-либо страдали сердечными заболеваниями (такими как стенокардия, учащенное сердцебиение или сердечная недостаточность) или имели проблемы с дыханием.
Если что-либо из вышеперечисленного относится к вам (или если вы не уверены), проконсультируйтесь со своим врачом, фармацевтом или медсестрой, прежде чем принимать Мабтеру. Возможно, вашему врачу потребуется уделять вам особое внимание во время приема Мабтеры.
Если у вас ревматоидный артрит, гранулематоз с полиангиитом или микроскопический полиангиит, поговорите со своим врачом.
- если вы подозреваете, что у вас есть инфекция, даже легкая, например, простуда. Клетки, на которые воздействует мабтера, используются для борьбы с инфекциями, и вы должны подождать, пока инфекция исчезнет, прежде чем принимать мабтеру. Также сообщите своему врачу, если у вас в прошлом были многочисленные инфекции или если вы страдаете от тяжелых инфекций;
- если вы считаете, что в ближайшем будущем вам потребуются какие-либо прививки, включая прививки, необходимые для поездки в другие страны. Некоторые вакцины не следует вводить одновременно с Мабтерой или в течение нескольких месяцев после приема Мабтеры. Ваш врач рассмотрит возможность вакцинации перед приемом Мабтеры.
Дети и подростки
Поговорите со своим врачом, фармацевтом или медсестрой, прежде чем давать это лекарство, если вам или вашему ребенку меньше 18 лет, поскольку в настоящее время имеется мало информации о применении Мабтеры у детей и подростков.
Взаимодействие Какие лекарства или продукты могут изменить действие Мабтеры
Сообщите своему врачу, фармацевту или медсестре, если вы принимаете, недавно принимали или собираетесь принимать любые другие лекарства, в том числе лекарства, отпускаемые без рецепта, и лекарства на травах, поскольку Мабтера может повлиять на действие некоторых лекарств и наоборот.
В частности, сообщите своему врачу:
- если вы принимаете лекарства от гипертонии, вас могут попросить прекратить прием этих лекарств за 12 часов до приема Мабтеры, поскольку у некоторых людей при приеме Мабтеры наблюдается снижение артериального давления;
- если в прошлом вы принимали лекарства, влияющие на иммунную систему, например химиотерапию или иммунодепрессанты.
Если что-либо из вышеперечисленного относится к вам (или если вы не уверены), поговорите со своим врачом, фармацевтом или медсестрой, прежде чем принимать Мабтеру.
Предупреждения Важно знать, что:
Беременность, кормление грудью и фертильность
Вы должны сообщить своему врачу или медсестре, если вы беременны, подозреваете или планируете забеременеть, поскольку Мабтера может проникать через плаценту и повлиять на ребенка.
Если есть вероятность того, что вы можете забеременеть, вам и вашему партнеру необходимо будет использовать эффективные средства контрацепции во время терапии Мабтерой и в течение 12 месяцев после последнего курса лечения Мабтерой.
Мабтера может проникать в грудное молоко, поэтому вы не должны кормить грудью во время терапии этим лекарством или в течение 12 месяцев после вашего последнего лечения Мабтерой.
Вождение и использование машин
Неизвестно, влияет ли Мабтера на способность управлять автомобилем и использовать инструменты или механизмы.
Дозировка и способ применения Как применять Мабтера: Дозировка
Администрация
Мабтера будет назначена вам врачом или медсестрой, имеющей опыт применения этого лекарства. Они будут внимательно следить за вами во время приема этого лекарства, чтобы обнаружить любые побочные эффекты.
Мабтера всегда вводится капельно в вену (внутривенная инфузия).
Лекарства, назначаемые перед каждой инфузией Мабтеры
Перед инфузией Мабтеры вам будут назначены другие лекарства (премедикация), чтобы избежать или уменьшить возникновение возможных побочных эффектов.
Сколько и как часто вы будете получать терапию
а) Если вы лечитесь от неходжкинской лимфомы
- Если вам дается только Мабтера
Мабтера будет вводиться один раз в неделю в течение 4 недель. Возможны повторные курсы лечения Мабтерой.
- Если вам назначают Мабтеру в сочетании с химиотерапией
Вы получите Мабтеру в день химиотерапии; их введение обычно происходит каждые 3 недели максимум 8 раз
- Если вы хорошо отреагируете на лечение, Мабтера может назначаться вам в качестве поддерживающей терапии каждые 2–3 месяца в течение двух лет. В зависимости от вашей реакции на лекарство ваш врач может изменить режим приема.
б) Если вы лечитесь от хронического лимфолейкоза
Если вы лечитесь Мабтерой в сочетании с химиотерапией, вы будете получать инфузии Мабтеры в день 0 цикла 1, затем в день 1 каждого цикла, всего 6 циклов. Каждый цикл длится 28 дней. После инфузии Мабтеры следует назначить химиотерапию. Ваш врач решит, следует ли вам получать сопутствующую поддерживающую терапию.
в) Если вы лечитесь от ревматоидного артрита
Каждый цикл лечения состоит из двух отдельных инфузий, вводимых с интервалом в 2 недели. Возможны повторные курсы лечения Мабтерой. В зависимости от признаков и симптомов вашего заболевания врач решит, когда назначить вам дальнейшие курсы. Это могло произойти через несколько месяцев.
г) Если вы лечитесь от гранулематоза с полиангиитом или микроскопическим полиангиитом.
Лечение Мабтерой включает четыре отдельных инфузии с недельными интервалами. Кортикостероиды будут вводиться в виде инъекций перед началом лечения Мабтерой. Пероральный прием кортикостероидов может быть начат вашим врачом в любое время для лечения вашего состояния.
Побочные эффекты Каковы побочные эффекты Мабтеры
Как и все лекарства, это лекарство может вызывать побочные эффекты, хотя они возникают не у всех.
Большинство побочных эффектов легкие или умеренные, но в некоторых случаях они могут быть серьезными и требовать лечения. В редких случаях некоторые из этих реакций заканчивались летальным исходом.
Инфузионные реакции
Во время или в течение первых 2 часов после первой инфузии у вас могут развиться жар, озноб и тремор. Реже у некоторых пациентов может быть боль в месте инфузии, образование волдырей, кожный зуд, недомогание, усталость, головная боль, затрудненное дыхание, опухший язык или горло, раздражение или насморк, рвота, ощущение тепла или тепла. Сердцебиение, сердечный приступ или уменьшение количество тромбоцитов. Если у вас болезнь сердца или стенокардия, эти реакции могут усугубиться. Если вы испытываете какие-либо из этих симптомов, немедленно сообщите об этом человеку, который вводит вам инфузию, так как скорость инфузии, возможно, необходимо замедлить или остановить. Может потребоваться дополнительное лечение, например, антигистаминным препаратом или парацетамолом. Когда эти симптомы проявляются разрешился или улучшился, инфузию можно возобновить. Эти реакции реже возникают после второй инфузии. Ваш врач может принять решение о прекращении лечения Мабтерой, если эти реакции носят тяжелый характер.
Инфекции
Немедленно сообщите своему врачу, если у вас есть какие-либо признаки инфекции, в том числе:
- лихорадка, кашель, боль в горле, жжение при мочеиспускании, слабость или общее недомогание;
- потеря памяти, беспокойное мышление, трудности при ходьбе или потеря зрения - это может быть связано с очень редкой «серьезной инфекцией, которая закончилась летальным исходом (прогрессирующая мультифокальная лейкоэнцефалопатия или ПМЛ). Во время лечения с помощью Мабтеры могут легче развиться инфекции.
- Часто это простуда, но были случаи пневмонии или инфекций мочевыводящих путей. Эти условия перечислены в «списке в разделе« Другие нежелательные эффекты »ниже.
Если вы лечитесь от ревматоидного артрита, вы также найдете эту информацию в карточке предупреждения пациента, которую вам выдаст врач. Важно, чтобы вы носили эту карточку с предупреждением и показывали ее члену семьи или кому-либо еще. иначе позаботьтесь о ней.
Кожные реакции
В очень редких случаях могут возникнуть серьезные кожные реакции с образованием волдырей, которые могут быть опасными для жизни. Покраснение, часто связанное с волдырями, может появиться на коже или слизистых оболочках, например во рту, на гениталиях или веках, а также может присутствовать лихорадка. Немедленно сообщите своему врачу, если у вас появятся какие-либо из этих симптомов.
Другие побочные эффекты
а) Если вы лечитесь от неходжкинской лимфомы или хронического лимфолейкоза
Очень частые побочные эффекты (им может быть подвержено более 1 человека из 10):
- бактериальные или вирусные инфекции, бронхит
- низкое количество лейкоцитов, с лихорадкой или без нее, или тромбоцитов (клеток крови)
- тошнота
- участки облысения на коже головы, озноб, головная боль
- снижение иммунной системы - из-за уменьшения количества определенных антител, называемых «иммуноглобулинами» (IgG), в крови, которые помогают организму защитить себя от инфекций.
Общие побочные эффекты (им может быть подвержено до 1 человека из 10):
- инфекции крови (сепсис), пневмония, опоясывающий лишай, простуда, бронхиальная инфекция, грибковые инфекции, инфекции неизвестного происхождения, синусит, гепатит В
- низкое количество эритроцитов (анемия), низкое количество всех клеток крови
- аллергические реакции (гиперчувствительность)
- высокий уровень сахара в крови, потеря веса, отек лица и тела, высокий уровень «фермента« ЛДГ »в крови, низкий уровень кальция в крови
- ненормальные ощущения в коже - такие как онемение, покалывание, покалывание, жжение, ощущение растянутой кожи, снижение осязания
- чувство беспокойства, трудности с засыпанием
- выраженное покраснение лица и других участков кожи вследствие расширения кровеносных сосудов
- головокружение или беспокойство
- усиление слезотечения, проблемы со слезоточивым протоком, воспаление глаз (конъюнктивит)
- постоянный звон в ушах, боль в ушах
- проблемы с сердцем - например, сердечный приступ, нерегулярное или учащенное сердцебиение
- высокое или низкое кровяное давление (снижение кровяного давления, особенно в положении стоя)
- сокращение мышц дыхательных путей, вызывающее хрипы (бронхоспазм), воспаление, раздражение в легких, горле и носовых пазухах, одышку, насморк
- рвота, диарея, боль в желудке, раздражение или изъязвление горла и рта, проблемы с глотанием, запор, несварение желудка
- расстройства пищевого поведения: недостаточное потребление пищи, приводящее к потере веса
- крапивница, повышенное потоотделение, ночная потливость
- мышечные проблемы, такие как жесткость мышц, боль в суставах или мышцах, боль в спине и шее
- общее недомогание, беспокойство или усталость, тремор, признаки гриппа
- полиорганная недостаточность.
Необычные побочные эффекты (им может быть подвержено до 1 человека из 100):
- проблемы с кровотечением, снижение выработки эритроцитов и повышенное разрушение эритроцитов (гемолитическая и апластическая анемия), отек или увеличение лимфатических узлов
- плохое настроение и потеря интереса или удовольствия от занятий, нервозность
- проблемы, связанные со вкусом - например, изменения вкусовых ощущений
- проблемы с сердцем - например, медленное сердцебиение или боль в груди (стенокардия)
- астма, недостаточное количество кислорода, поступающего в органы тела
- вздутие живота.
Очень редкие побочные эффекты (им может быть подвержено до 1 человека из 10000):
- кратковременное увеличение количества определенных типов антител (иммуноглобулины - IgM) в крови, химические изменения в крови из-за распада умирающих раковых клеток
- повреждение нервов рук и ног, паралич лица
- сердечная недостаточность
- воспаление кровеносных сосудов, в том числе вызывающих кожные симптомы
- нарушение дыхания
- повреждение стенки кишечника (перфорация)
- серьезные проблемы с кожей с образованием пузырей, потенциально смертельный исход. Покраснение, часто связанное с волдырями, может появиться на коже или слизистых оболочках, например во рту, на гениталиях или веках, а также может присутствовать лихорадка.
- почечная недостаточность
- тяжелая потеря зрения.
Неизвестно (частота, с которой возникают эти побочные эффекты, неизвестна):
- немедленное снижение лейкоцитов
- снижение количества тромбоцитов вскоре после инфузии - состояние обратимое, но в редких случаях потенциально смертельное
- потеря слуха, потеря других чувств.
б) Если вы лечитесь от ревматоидного артрита
Очень частые побочные эффекты (им может быть подвержено более 1 человека из 10):
- инфекции, такие как пневмония (бактериальная)
- боль при мочеиспускании (инфекция мочевыводящих путей)
- аллергические реакции, которые могут возникнуть во время инфузии, но могут возникнуть в течение 24 часов после инфузии
- изменения артериального давления, тошнота, сыпь, лихорадка, чувство зуда, насморк или заложенность носа, чихание, дрожь, учащенное сердцебиение и усталость
- Головная боль
- изменения в лабораторных исследованиях, требуемые врачом. К ним относятся снижение количества определенных специфических белков в крови (иммуноглобулинов), которые помогают защитить от инфекции.
Общие побочные эффекты (им может быть подвержено до 1 человека из 10):
- инфекции, такие как воспаление бронхов (бронхит)
- ощущение боли и распирания за носом, щеками и глазами (синусит), боль в животе, рвота и диарея, затрудненное дыхание
- грибковая инфекция стопы (стопа спортсмена)
- высокий уровень холестерина в крови
- ненормальные ощущения на коже, такие как онемение, покалывание, покалывание или жжение, радикулит, мигрень, головокружение
- выпадение волос
- тревога, депрессия
- расстройство желудка, диарея, кислотный рефлюкс, раздражение и / или изъязвление горла и рта
- боль в животе, спине, мышцах и / или суставах.
Необычные побочные эффекты (им может быть подвержено до 1 человека из 100):
- избыточная задержка жидкости на лице и теле
- воспаление, раздражение и / или напряжение в легких, горле, кашель
- кожные реакции, включая крапивницу, зуд, сыпь
- аллергические реакции, включая хрипы или одышку, отек лица и языка, коллапс.
Очень редкие побочные эффекты (им может быть подвержено до 1 человека из 10000):
- комплекс симптомов, возникающих в течение нескольких недель после инфузии Мабтеры, включая реакции аллергического типа, такие как сыпь, зуд, болезненность суставов, увеличение лимфатических узлов и лихорадка
- серьезные кожные реакции с образованием пузырей, которые могут быть опасными для жизни. Покраснение, часто связанное с волдырями, может появиться на коже или слизистых оболочках, например во рту, на гениталиях или веках, а также может присутствовать лихорадка.
Другие редко сообщаемые побочные эффекты от лечения Мабтерой включают снижение количества лейкоцитов (нейтрофилов), которые используются для борьбы с инфекциями. Некоторые инфекции могут быть серьезными (см. Информацию о инфекциях в этом разделе).
в) Если вы лечитесь от гранулематоза с полиангиитом или от микроскопического полиангиита.
Очень частые побочные эффекты (им может быть подвержено более 1 человека из 10):
- инфекции, такие как инфекции легких, инфекции мочевыводящих путей (болезненное мочеиспускание), простуды и инфекции герпеса.
- аллергические реакции, которые могут возникнуть во время инфузии, но могут возникнуть в течение 24 часов после инфузии
- понос
- кашель или одышка
- носовое кровотечение
- повышенное кровяное давление
- боль в суставах или спине
- мышечные подергивания или тряски
- чувство головокружения
- тремор (тремор, часто в руках)
- нарушения сна (бессонница)
- отек рук и лодыжек.
Общие побочные эффекты (им может быть подвержено до 1 человека из 10):
- несварение желудка
- запор
- кожные высыпания, включая прыщи или прыщи
- покраснение или покраснение кожи
- заложенность носа
- жесткость мышц или мышечные боли
- боль в мышцах или руках или ногах
- низкое количество эритроцитов (анемия)
- низкое количество тромбоцитов в крови увеличение количества калия в крови
- изменения сердечного ритма или частоты сердечных сокращений быстрее, чем обычно.
Очень редкие побочные эффекты (им может быть подвержено до 1 человека из 10000):
- серьезные кожные реакции с образованием пузырей, которые могут быть опасными для жизни. Покраснение, часто связанное с волдырями, может появиться на коже или слизистых оболочках, например во рту, на гениталиях или веках, а также может присутствовать лихорадка.
- рецидив перенесенной ранее инфекции гепатита В.
Мабтера также может вызывать изменения в лабораторных исследованиях, требуемых вашим врачом.
Если вы принимаете Мабтеру в сочетании с другими лекарствами, некоторые из побочных эффектов, которые вы испытываете, могут быть связаны с другими лекарствами.
Сообщение о побочных эффектах
Если у вас появятся какие-либо побочные эффекты, поговорите со своим врачом, фармацевтом или медсестрой. Это включает в себя любые возможные побочные эффекты, не указанные в этой брошюре. Вы также можете сообщить о побочных эффектах напрямую через национальную систему отчетности, перечисленную в Приложении V. Побочные эффекты, которым вы можете помочь предоставьте дополнительную информацию о безопасности этого лекарства.
Срок действия и удержание
Храните это лекарство в недоступном для детей месте.
Не используйте это лекарство после истечения срока годности, указанного на упаковке после EXP. Срок годности относится к последнему дню месяца.
Хранить в холодильнике (2-8 ° C). Храните контейнер во внешней упаковке, чтобы защитить его от света.
Не выбрасывайте лекарства в сточные воды или бытовые отходы. Спросите своего фармацевта, как утилизировать лекарства, которые вы больше не используете. Это поможет защитить окружающую среду.
Что содержит Мабтера
- Действующее вещество в Мабтере - ритуксимаб. Во флаконе содержится 500 мг ритуксимаба (10 мг / мл).
- Другие ингредиенты: цитрат натрия, полисорбат 80, хлорид натрия, гидроксид натрия, соляная кислота и вода для инъекций.
Как выглядит Мабтера и что содержится в упаковке
Мабтера - это прозрачный бесцветный раствор, поставляемый в виде концентрата для приготовления раствора для инфузий. В пачках по 1 флакону.
Листовка с исходным кодом: AIFA (Итальянское агентство по лекарственным средствам). Контент опубликован в январе 2016 года. Представленная информация может быть устаревшей.
Чтобы иметь доступ к самой последней версии, рекомендуется зайти на сайт AIFA (Итальянское агентство по лекарственным средствам). Заявление об ограничении ответственности и полезная информация.
01.0 НАИМЕНОВАНИЕ ЛЕКАРСТВЕННОГО ПРЕПАРАТА
MABTHERA 500 MG КОНЦЕНТРАТ ДЛЯ РАСТВОРА ДЛЯ ИНФУЗИИ
02.0 КАЧЕСТВЕННЫЙ И КОЛИЧЕСТВЕННЫЙ СОСТАВ
Каждый мл содержит 10 мг ритуксимаба.
Каждый флакон содержит 500 мг ритуксимаба.
Ритуксимаб представляет собой генетически созданное химерное моноклональное антитело мыши / человека, состоящее из гликозилированного иммуноглобулина с константными областями человеческого IgG1 и последовательностями вариабельных областей легкой цепи мыши. Антитело получают с использованием суспензионной культуры клеток млекопитающих (яичник китайского хомячка) и очищают с помощью аффинной хроматографии и ионного обмена, включая специальные процедуры инактивации и удаления вирусов.
Полный список вспомогательных веществ см. В разделе 6.1.
03.0 ФАРМАЦЕВТИЧЕСКАЯ ФОРМА
Концентрат для приготовления раствора для инфузий.
Прозрачная бесцветная жидкость.
04.0 КЛИНИЧЕСКАЯ ИНФОРМАЦИЯ
04.1 Терапевтические показания
Мабтера назначается взрослым по следующим показаниям:
Неходжкинская лимфома (НХЛ)
Мабтера показана для лечения ранее нелеченных пациентов с фолликулярной лимфомой III-IV стадии в сочетании с химиотерапией.
Поддерживающая терапия Мабтерой показана для лечения пациентов с фолликулярной лимфомой, отвечающих на индукционную терапию.
Монотерапия Мабтерой показана для лечения пациентов с фолликулярной лимфомой III-IV стадии, которые являются химиорезистентными или имеют второй или последующий рецидив после химиотерапии.
Мабтера показана для лечения пациентов с CD20-положительной диффузной крупноклеточной неходжкинской лимфомой в сочетании с химиотерапией CHOP (циклофосфамид, доксорубицин, винкристин, преднизолон).
Хронический лимфолейкоз (ХЛЛ)
Мабтера в сочетании с химиотерапией показана для лечения пациентов с ранее нелеченым и рецидивирующим / рефрактерным хроническим лимфолейкозом. Доступны лишь ограниченные данные об эффективности и безопасности для пациентов, ранее получавших моноклональные антитела, включая Мабтеру, или для пациентов, резистентных к предыдущему лечению химиотерапией Мабтера плюс.
См. Раздел 5.1 для получения дополнительной информации.
Ревматоидный артрит
Мабтера в комбинации с метотрексатом показана для лечения тяжелого активного ревматоидного артрита у взрослых пациентов, у которых проявился «неадекватный ответ или» непереносимость других модифицирующих заболевание противоревматических препаратов (БПВП), включая один или несколько ингибиторов фактора некроза опухоли. (TNF).
Было показано, что Мабтера снижает скорость прогрессирования повреждений суставов по данным рентгенологического исследования и улучшает физическую функцию при приеме в сочетании с метотрексатом.
Гранулематоз с полиангиитом и микроскопическим полиангиитом
Мабтера в сочетании с глюкокортикоидами показана для индукции ремиссии у взрослых пациентов с гранулематозом с полиангиитом (Вегенера) (ГПА) и тяжелым активным микроскопическим полиангиитом (МПА).
04.2 Дозировка и способ применения
Мабтеру следует вводить под тщательным наблюдением опытного медицинского работника и в среде, где имеется немедленное наличие реанимационного оборудования (см. Раздел 4.4).
Перед каждым приемом Мабтеры всегда следует проводить премедикацию жаропонижающими препаратами и антигистаминными препаратами, например парацетамолом и дифенгидрамином.
У пациентов с неходжкинской лимфомой и хроническим лимфолейкозом (ХЛЛ) следует рассмотреть возможность премедикации глюкокортикоидами, если Мабтера не назначается в сочетании с химиотерапией, содержащей глюкокортикоиды.
У пациентов с ревматоидным артритом премедикация метилпреднизолоном 100 мг внутривенно должна быть завершена за 30 минут до инфузии Мабтеры, чтобы снизить частоту и тяжесть инфузионных реакций (IRR).
Пациентам с гранулематозом с полиангиитом (Вегенера) или микроскопическим полиангиитом рекомендуется внутривенное введение метилпреднизолона в дозе 1000 мг / сут за 1-3 дня до первой инфузии Мабтеры (последняя доза метилпреднизолона может быть введена в тот же день, что и после первой инфузии Мабтеры), после чего следует пероральный прием преднизона в дозе 1 мг / кг / день (не следует превышать 80 мг / день, а дозу следует постепенно снижать. как можно быстрее в зависимости от клиническое состояние) во время и после лечения Мабтерой.
Дозировка
Важно проверить этикетку лекарства, чтобы убедиться, что пациенту вводится соответствующий препарат (внутривенно или подкожно) в соответствии с предписаниями.
Неходжкинской лимфомы
Фолликулярная неходжкинская лимфома
Ассоциативная терапия
Рекомендуемая доза Мабтеры в сочетании с химиотерапией для индукционного лечения ранее нелеченых или рецидивирующих / рефрактерных пациентов с фолликулярной лимфомой составляет 375 мг / м2 площади поверхности тела за цикл, до 8 циклов.
Мабтеру следует вводить в первый день каждого цикла химиотерапии после в / в. глюкокортикоидный компонент химиотерапии, если применимо.
Поддерживающая терапия
• Ранее нелеченая фолликулярная лимфома.
Рекомендуемая доза Мабтеры, используемой в качестве поддерживающей терапии для ранее нелеченых пациентов с фолликулярной лимфомой, которые ответили на индукционное лечение, составляет: 375 мг / м2 площади поверхности тела один раз в два месяца (начиная через 2 месяца после последней дозы терапии). Индукция) до заболевания прогрессии или максимум на два года.
• Рецидивирующая / рефрактерная фолликулярная лимфома.
Рекомендуемая доза Мабтеры, используемой в качестве поддерживающей терапии для пациентов с рецидивирующей / резистентной фолликулярной лимфомой, которые ответили на индукционное лечение, составляет 375 мг / м2 площади поверхности тела один раз в 3 месяца (начиная с 3 месяцев после последней дозы терапии). Индукция) до прогрессирование заболевания или максимум на два года.
Монотерапия
• Рецидивирующая / рефрактерная фолликулярная лимфома.
Рекомендуемая доза монотерапии Мабтерой, используемой в качестве индукционного лечения для взрослых пациентов с фолликулярной лимфомой III-IV стадии, которые являются химиорезистентными или находятся в их втором или последующем рецидиве после химиотерапии, составляет 375 мг / м2 площади поверхности тела, вводимых в виде внутривенной инфузии. раз в неделю в течение четырех недель.
Для повторного лечения монотерапией Мабтерой для пациентов, которые отреагировали на предыдущее лечение Мабтерой при рецидивной / рефрактерной фолликулярной лимфоме, рекомендуемая доза составляет 375 мг / м2 площади поверхности тела, вводимая в виде внутривенной инфузии один раз в неделю в течение четырех недель (см. Раздел 5.1. ).
Диффузная крупноклеточная неходжкинская лимфома
Мабтера необходимо применять в сочетании с химиотерапией CHOP. Рекомендуемая доза составляет 375 мг / м2 площади поверхности тела, вводимая в первый день каждого цикла химиотерапии в течение 8 циклов после внутривенной инфузии глюкокортикоидного компонента CHOP. Безопасность и эффективность Мабтеры в сочетании с другими химиотерапевтическими препаратами при диффузной крупноклеточной неходжкинской лимфоме еще не установлены.
Корректировка дозировки во время лечения
Снижение дозы Мабтеры не рекомендуется. Когда Мабтера назначается в сочетании с химиотерапией, следует применять стандартные снижения дозы химиотерапевтических препаратов.
Хронический лимфолейкоз
Пациентам с ХЛЛ рекомендуется проводить профилактику с адекватной гидратацией и назначением урикостатов за 48 часов до начала терапии, чтобы снизить риск синдрома лизиса опухоли. Пациентам с ХЛЛ с количеством лимфоцитов> 25 x 109 / л рекомендуется вводить преднизон / преднизолон 100 мг внутривенно непосредственно перед инфузией Мабтеры для уменьшения скорости и тяжести острых инфузионных реакций и / или синдрома высвобождения цитокинов.
Рекомендуемая доза Мабтеры в сочетании с химиотерапией для ранее нелеченых и рецидивирующих / рефрактерных пациентов составляет 375 мг / м2 площади поверхности тела, вводимой в день 0 первого цикла лечения, с последующим введением 500 мг / м2 площади поверхности тела в первый день каждого последующего. цикл для 6 полных циклов. После инфузии Мабтеры следует проводить химиотерапию.
Ревматоидный артрит
Пациентам, получающим Мабтеру, следует выдавать карточку с предупреждением пациента при каждой инфузии.
Курс Мабтеры состоит из двух внутривенных инфузий по 1000 мг каждая. Рекомендуемая дозировка Мабтеры составляет 1000 мг внутривенно с последующей второй внутривенной инфузией 1000 мг через две недели.
Необходимость дальнейшего лечения следует оценить через 24 недели после предыдущего цикла. Повторное лечение должно быть выполнено в это время, если остаточная активность болезни сохраняется, в противном случае повторное лечение следует отложить до тех пор, пока остаточная активность болезни не появится снова.
Имеющиеся данные предполагают, что клинический ответ обычно достигается в течение 16–24 недель после начального курса лечения. У пациентов, которые не видят терапевтического эффекта в течение этого периода времени, следует внимательно рассмотреть вопрос о продолжении терапии.
Гранулематоз с полиангиитом и микроскопическим полиангиитом
Пациентам, принимающим Мабтера, следует выдавать карточку с предупреждением пациента при каждой инфузии.
Рекомендуемая дозировка Мабтеры для индукционной терапии ремиссии гранулематоза с полиангиитом и микроскопическим полиангиитом составляет 375 мг / м2 площади поверхности тела, вводимая внутривенно один раз в неделю в течение 4 недель (всего 4 инфузии).
Пациентам с гранулематозом с полиангиитом и микроскопическим полиангиитом во время и после лечения Мабтерой рекомендуется профилактика пневмонии. Pneumocystis jiroveci, (PCP), в зависимости от ситуации.
Особые группы населения
Педиатрическая популяция
Безопасность и эффективность Мабтеры у детей и подростков до 18 лет еще не установлены.
Пожилые пациенты
У пожилых пациентов (в возрасте> 65 лет) корректировка дозировки не требуется.
Способ применения
Приготовленный раствор Мабтеры следует вводить путем внутривенной инфузии через выделенную линию. Его не следует вводить внутривенно или болюсно. Следует тщательно наблюдать за пациентами на предмет появления синдрома высвобождения цитокинов (см. Раздел 4.4). Пациентам, у которых развиваются тяжелые реакции, особенно тяжелая одышка, бронхоспазм или гипоксия, следует немедленно прекратить инфузию. Пациенты с неходжкинской лимфомой должны быть затем обследованы на предмет наличия синдрома лизиса опухоли путем проведения соответствующих лабораторных тестов и на наличие легочной инфильтрации с помощью рентгенографии грудной клетки. Всем пациентам инфузию не следует возобновлять до полного исчезновения всех симптомов. Симптомы и нормализация лабораторных показателей и рентгенографии грудной клетки. Только после этого инфузию можно возобновить с начальной скоростью, сниженной наполовину по сравнению с предыдущей. Если такие же серьезные побочные реакции возникнут снова, решение о прекращении лечения следует тщательно рассматривать в каждом конкретном случае.
Легкие или умеренные IRR (см. Раздел 4.8) обычно отвечают за снижение скорости инфузии. По мере улучшения симптомов скорость инфузии можно увеличивать.
Первый настой
Рекомендуемая начальная скорость инфузии составляет 50 мг / ч; после первых 30 минут его можно увеличивать с шагом 50 мг / ч каждые 30 минут, максимум до 400 мг / ч.
Последующие инфузии
По всем показаниям
Последующие дозы Мабтеры можно вводить с начальной скоростью 100 мг / ч и увеличивать на 100 мг / ч с 30-минутными интервалами до максимальной 400 мг / ч.
Только при ревматоидном артрите
Альтернативная схема для более быстрого введения последующих инфузий
Если при первой или последующих инфузиях, введенных в дозе 1000 мг Мабтеры в соответствии со стандартным графиком инфузий, пациенты не испытали тяжелой реакции, связанной с инфузией, вторую и последующие инфузии можно проводить с большей скоростью, с той же скоростью. ..концентрация предыдущих инфузий (4 мг / мл на объем 250 мл).
Начните инфузию со скоростью 250 мг / ч в течение первых 30 минут, а затем со скоростью 600 мг / ч в течение следующих 90 минут. Если более быстрая инфузия хорошо переносится, тот же график инфузии можно использовать для введения последующих инфузий. .
Более быстрая инфузия не следует назначать пациентам с клинически значимым сердечно-сосудистым заболеванием, включая аритмии, или у которых в прошлом возникли тяжелые реакции на инфузию ритуксимаба или любую предшествующую биологическую терапию.
04.3 Противопоказания
Противопоказания к применению при неходжкинской лимфоме и хроническом лимфолейкозе
Повышенная чувствительность к действующему веществу, мышиному белку или любому другому вспомогательному веществу, перечисленному в разделе 6.1.
Активные тяжелые инфекции (см. Раздел 4.4).
Пациенты с тяжелым иммунодефицитом.
Противопоказания к применению при ревматоидном артрите, гранулематозе с полиангиитом и микроскопическом полиангиите
Повышенная чувствительность к активному веществу, мышиному белку или любому другому вспомогательному веществу, перечисленному в разделе 6.1.
Активные тяжелые инфекции (см. Раздел 4.4).
Пациенты с тяжелым иммунодефицитом.
Тяжелая сердечная недостаточность (класс IV по кардиологической ассоциации Нью-Йорка) или тяжелая неконтролируемая болезнь сердца (другие сердечные заболевания см. В разделе 4.4).
04.4 Особые предупреждения и соответствующие меры предосторожности при использовании
Чтобы улучшить отслеживаемость биологических лекарственных препаратов, название продукта Мабтера должно быть четко указано в истории болезни пациента.
Прогрессирующая мультифокальная лейкоэнцефалопатия
Всем пациентам, принимающим Мабтера при ревматоидном артрите, гранулематозе с полиангиитом и микроскопическом полиангиите, при каждой инфузии должна выдаваться карточка с предупреждением. Карточка с предупреждением содержит важную информацию о безопасности для пациентов, касающуюся потенциально серьезных инфекций, включая прогрессирующую мультифокальную лейкоэнцефалопатию (ПМЛ).
Сообщалось об очень редких случаях летального исхода ПМЛ после применения Мабтеры. Пациентов следует регулярно обследовать на предмет любых новых или ухудшающихся неврологических симптомов или признаков, указывающих на ПМЛ. При подозрении на ПМЛ дальнейшее введение следует приостановить. диагноз ПМЛ был исключен. Врач должен осмотреть пациента, чтобы определить, указывают ли симптомы на неврологическую дисфункцию и, если да, могут ли эти симптомы наводить на мысль о ПМЛ. При наличии клинических показаний следует обратиться за консультацией к неврологу.
В случае сомнений следует рассмотреть возможность дальнейшего обследования, включая такие тесты, как МРТ, желательно с контрастированием, анализ спинномозговой жидкости (ЦСЖ) для оценки ДНК вируса JC и повторные неврологические обследования.
Врачи должны быть особенно внимательны к симптомам, указывающим на ПМЛ, которые пациент может не заметить (например, когнитивным, неврологическим или психиатрическим симптомам). Пациенту также следует посоветовать сообщить своему партнеру или опекуну о лечении, поскольку они могут заметить симптомы, о которых пациент не подозревает.
Если у пациента развивается ПМЛ, прием Мабтеры необходимо полностью прекратить.
После восстановления иммунной системы у пациентов с ослабленным иммунитетом и ПМЛ отмечалась стабилизация или улучшение. Неизвестно, приведет ли раннее выявление ПМЛ и прекращение терапии Мабтерой к аналогичной стабилизации или улучшению.
Неходжкинская лимфома и хронический лимфолейкоз
Связанные инфузионные реакции
Мабтера связана с реакциями, связанными с инфузией (IRR), которые потенциально связаны с высвобождением цитокинов и / или других химических медиаторов. Синдром высвобождения цитокинов может быть клинически неотличим от реакций острой гиперчувствительности.
Этот набор реакций, который включает синдром высвобождения цитокинов, синдром лизиса опухоли, анафилактические реакции и реакции гиперчувствительности, описан ниже. Эти реакции не связаны конкретно со способом введения Мабтеры и могут наблюдаться с обоими препаратами.
Сообщалось о серьезных и фатальных реакциях, связанных с инфузией, во время постмаркетингового применения внутривенного препарата Мабтеры, которые начинались в пределах от 30 минут до 2 часов после начала первой внутривенной инфузии Мабтеры. Эти реакции характеризовались легочными явлениями, а в некоторых случаях случаи включали быстрый лизис опухоли и симптомы синдрома лизиса опухоли, а также лихорадку, озноб, дрожь, гипотонию, крапивницу, ангионевротический отек и другие симптомы (см. раздел 4.8).
Синдром тяжелого выброса цитокинов характеризуется тяжелой одышкой, часто сопровождающейся бронхоспазмом и гипоксией, а также лихорадкой, ознобом, дрожью, крапивницей и ангионевротическим отеком. Этот синдром может быть связан с некоторыми особенностями синдрома лизиса опухоли, такими как гиперурикемия, гиперкалиемия, гипокальциемия, гиперфосфатемия, острая почечная недостаточность, повышенная концентрация лактатдегидрогеназы (ЛДГ), и может быть связан с острой дыхательной недостаточностью и смертью. Острая дыхательная недостаточность может сопровождаться такими явлениями, как интерстициальная инфильтрация легких или отек легких, которые видны на рентгенограмме грудной клетки. Синдром часто возникает в течение одного-двух часов после начала первой инфузии. Пациенты с легочной недостаточностью или инфильтрацией опухоли легких в анамнезе могут подвергаться повышенному риску неблагоприятных исходов, и к ним следует относиться с большей осторожностью. Пациентам, у которых развивается тяжелый синдром высвобождения цитокинов, следует немедленно прекратить инфузию (см. Раздел 4.2) и назначить агрессивное симптоматическое лечение. Поскольку за первоначальным улучшением клинических симптомов может последовать их ухудшение, за этими пациентами следует тщательно наблюдать до разрешения или исключения опухоли. синдром лизиса и легочная инфильтрация. Дальнейшее лечение пациентов после полного исчезновения симптомов и признаков редко приводило к рецидиву тяжелого синдрома высвобождения цитокинов.
С особой осторожностью следует лечить пациентов с высокой опухолевой нагрузкой или с большим количеством (≥ 25 x 109 / л) циркулирующих неопластических клеток, таких как пациенты с ХЛЛ, которые могут иметь повышенный риск особенно тяжелого синдрома высвобождения цитокинов. За этими пациентами следует очень внимательно наблюдать на протяжении всего курса первой инфузии. Следует рассмотреть возможность использования уменьшенной скорости инфузии для первой инфузии у таких пациентов или разделенной дозы в течение двух дней в течение первого цикла и каждого последующего цикла, если количество лимфоцитов все еще превышает 25 x 109 / л.
Связанные с инфузией побочные реакции всех видов (включая синдром высвобождения цитокинов, сопровождающийся гипотонией и бронхоспазмом у 10% пациентов) наблюдались у 77% пациентов, принимавших Мабтера (см. Раздел 4.8). Эти симптомы обычно обратимы. инфузии Мабтеры и с назначением жаропонижающих препаратов, антигистаминных препаратов и, иногда, кислорода, внутривенного введения физиологического раствора или бронхолитических препаратов и, при необходимости, глюкокортикоидов. Для тяжелых реакций см. описанный выше синдром высвобождения цитокинов.
Сообщалось об анафилактических и других реакциях гиперчувствительности у пациентов после внутривенного введения белков. В отличие от синдрома высвобождения цитокинов, реакции гиперчувствительности обычно возникают в течение нескольких минут после начала инфузии. В случае возникновения аллергической реакции во время приема Мабтеры, лекарственных средств для лечения реакций гиперчувствительности, например. Адреналин (адреналин), антигистаминные препараты и глюкокортикоиды должны быть доступны для немедленного применения.Клинические проявления анафилаксии могут быть похожи на клинические проявления синдрома высвобождения цитокинов (описанного выше). О реакциях, связанных с гиперчувствительностью, сообщалось реже, чем о реакциях, связанных с высвобождением цитокинов.
В некоторых случаях сообщалось о дополнительных реакциях: инфаркт миокарда, фибрилляция предсердий, отек легких и острая обратимая тромбоцитопения.
Во время приема Мабтеры может возникнуть артериальная гипотензия, поэтому следует рассмотреть возможность прекращения приема антигипертензивных препаратов за 12 часов до инфузии Мабтеры.
Сердечные расстройства
У пациентов, получавших Мабтера, наблюдались случаи стенокардии, сердечных аритмий, таких как трепетание и фибрилляция предсердий, сердечная недостаточность и / или инфаркт миокарда. Поэтому следует тщательно контролировать пациентов с сердечными заболеваниями и / или кардиотоксической химиотерапией в анамнезе.
Гематологическая токсичность
Хотя сама по себе Мабтера не оказывает миелосупрессивного действия, следует соблюдать особую осторожность при рассмотрении возможности лечения пациентов с аутологичными нейтрофилами тромбоцитов костного мозга и других групп риска с предположительно нарушенной функцией костного мозга без индукции миелотоксичности.
Во время терапии Мабтерой следует регулярно проводить общий анализ крови, включая количество нейтрофилов и тромбоцитов.
Инфекции
Во время терапии Мабтерой могут возникнуть серьезные инфекции, в том числе со смертельным исходом (см. Раздел 4.8).
Мабтеру нельзя применять у пациентов с тяжелыми активными инфекциями (например, туберкулезом, сепсисом и оппортунистическими инфекциями, см. Раздел 4.3).
Врачи должны с осторожностью подходить к применению Мабтеры у пациентов с рецидивирующими или хроническими инфекциями в анамнезе или с сопутствующими заболеваниями, которые могут еще больше предрасполагать пациентов к серьезным инфекциям (см. Раздел 4.8).
Сообщалось о случаях реактивации гепатита В у субъектов, получавших Мабтеру, включая сообщения о фульминантном гепатите со смертельным исходом. Большинство этих субъектов также получали цитотоксическую химиотерапию. Ограниченная информация, полученная в результате исследования пациентов с рецидивирующим / рефрактерным ХЛЛ, позволяет предположить, что лечение Мабтерой может также ухудшить исход первичных инфекций гепатита В. Скрининг на вирус гепатита В (ВГВ) должен проводиться у всех пациентов перед началом лечения Мабтерой и должен как минимум включать дозирование HBsAg и HBcAb. Затем эти тесты могут быть дополнены другими подходящими маркерами в соответствии с местными правилами. Пациентам с активной инфекцией гепатита В нельзя принимать Мабтера. Пациенты с положительной серологией на гепатит В (как на HBsAg, так и на HBcAb) должны быть обследованы врачом-гепатологом до начала лечения и должны находиться под наблюдением и наблюдением в соответствии с местными клиническими стандартами для предотвращения реактивации гепатита В.
Сообщалось об очень редких случаях прогрессирующей мультифокальной лейкоэнцефалопатии (ПМЛ) во время постмаркетингового использования Мабтеры при НХЛ и ХЛЛ (см. Раздел 4.8). Большинство пациентов получали Мабтеру в сочетании с химиотерапией или в рамках программы трансплантации гемопоэтических стволовых клеток.
Иммунизация
Безопасность иммунизации живыми вирусными вакцинами после терапии Мабтерой не изучалась для пациентов с НХЛ и ХЛЛ, и вакцинация живыми вирусными вакцинами не рекомендуется. Пациенты, принимающие Мабтера, могут получать невирусные вакцинации. Однако процент ответа на неживой вирус вакцины могут быть уменьшены. В нерандомизированном исследовании пациенты с рецидивом НХЛ низкой степени злокачественности, получавшие монотерапию Мабтерой, по сравнению с контрольными здоровыми добровольцами, не получавшими лечения, имели более низкий уровень ответов на вакцинацию бустерными антигенами столбняка (16% против 81%) и Неоантигены гемоцианина лимфы улитки (KLH) (4% против 76% при оценке более чем в 2 раза при увеличении титра антител). Ожидается, что ХЛЛ даст аналогичные результаты, учитывая сходство между двумя заболеваниями, однако это не было оценено в клинических исследованиях . предварительные терапевтические антитела против панели антигенов (Пневмококк, грипп A, эпидемический паротит, краснуха, ветряная оспа) сохранялась не менее 6 месяцев после лечения Мабтерой.
Кожные реакции
Сообщалось о серьезных кожных реакциях, таких как токсический эпидермальный некролиз (синдром Лайелла) и синдром Стивенса-Джонсона, некоторые со смертельным исходом (см. Раздел 4.8). В случае возникновения таких событий, если есть подозрение на связь с Мабтерой, лечение следует окончательно прекратить.
Ревматоидный артрит, гранулематоз с полиангиитом и микроскопический полиангиит
Группы населения с ревматоидным артритом, не принимавшие метотрексат (метотрексат)
Применение Мабтеры не рекомендуется пациентам, ранее не получавшим метотрексат, поскольку не установлено благоприятное соотношение польза / риск.
Связанные инфузионные реакции
Мабтера связана с реакциями, связанными с инфузией (ВСН), которые могут быть связаны с высвобождением цитокинов и / или других химических медиаторов. Премедикация обезболивающими / жаропонижающими и антигистаминными препаратами всегда должна проводиться перед каждой инфузией Мабтеры пациентам. При ревматоидном артрите премедикацию глюкокортикоидами следует проводить перед каждой инфузией Мабтеры, чтобы снизить частоту и тяжесть ВСД (см. разделы 4.2 и 4.8).
Сообщалось о серьезных случаях ВСД с летальным исходом у пациентов с ревматоидным артритом в условиях постмаркетинга.
При лечении ревматоидного артрита большинство реакций, связанных с инфузией, в клинических испытаниях были от легкой до умеренной по интенсивности. Наиболее частыми симптомами были аллергические реакции, такие как головная боль, зуд, раздражение горла, покраснение, сыпь, крапивница, гипертония и гипертермия. В целом доля пациентов, у которых наблюдалась некоторая инфузионная реакция, была выше после первой инфузии, чем после второй в любом цикле лечения. Частота ВСД снижалась в последующих курсах (см. Раздел 4.8). Сообщенные реакции, как правило, были обратимыми при снижении скорости инфузии или прекращении приема Мабтеры и приеме жаропонижающих, антигистаминных средств и, иногда, кислорода, внутривенного введения физиологического раствора или бронходилататоров и глюкокортикоидов, если необходимо. Внимательно наблюдайте за пациентами с ранее существовавшими сердечными заболеваниями. состояния и те, у кого ранее были сердечно-легочные побочные реакции.В зависимости от тяжести ВСД и необходимого вмешательства временно или навсегда прекратить прием Мабтеры. В большинстве случаев инфузию можно возобновить, снизив скорость до 50% (например, со 100 мг / ч до 50 мг / ч), когда симптомы полностью исчезнут.
Лекарства для лечения реакций гиперчувствительности, например. Адреналин (адреналин), антигистаминные препараты и глюкокортикоиды должны быть доступны для немедленного применения в случае возникновения аллергических реакций во время приема Мабтеры.
Нет данных о безопасности применения Мабтеры у пациентов с сердечной недостаточностью средней степени тяжести (класс III по NYHA) или тяжелым неконтролируемым заболеванием сердца. У пациентов, получавших Мабтеру, ранее существовавшие состояния сердечной ишемии, такие как стенокардия, становились симптоматическими, как и фибрилляция и трепетание предсердий. предыдущие реакции; сердечно-легочные нежелательные явления, риск сердечно-сосудистых осложнений, возникающих в результате инфузионных реакций, следует учитывать до начала лечения Мабтерой, и пациенты должны находиться под тщательным наблюдением во время приема. Во время инфузии Мабтеры может возникнуть гипотензия, поэтому отмена гипотензивных препаратов за 12 часов до начала лечения. Настой Мабтеры.
IRR для пациентов с гранулематозом с полиангиитом и микроскопическим полиангиитом были аналогичны тем, которые наблюдались в клинических исследованиях, проведенных у пациентов с ревматоидным артритом (см. Раздел 4.8).
Сердечные расстройства
У пациентов, получавших Мабтера, наблюдались случаи стенокардии, сердечной аритмии, такой как трепетание и фибрилляция предсердий, сердечная недостаточность и / или инфаркт миокарда. Таким образом, пациенты с сердечными заболеваниями в анамнезе должны находиться под тщательным наблюдением (см. Выше «Реакции, связанные с инфузией»).
Инфекции
Основываясь на механизме действия Мабтеры и знании того, что В-клетки играют важную роль в поддержании нормального иммунного ответа, пациенты имеют повышенный риск инфекций после терапии Мабтерой (см. Раздел 5.1). Во время лечения могут возникать серьезные инфекции, включая смертельные исходы. терапию Мабтерой (см. раздел 4.8). Мабтеру нельзя назначать пациентам с тяжелой активной инфекцией (например, туберкулезом, сепсисом и оппортунистическими инфекциями, см. раздел 4.3) или пациентам с тяжелым иммунодефицитом (например, у которых уровни CD4 или CD8 очень низкие. Врачи должны проявлять осторожность при рассмотрении возможности применения Мабтеры у пациентов с рецидивирующими или хроническими инфекциями в анамнезе или с сопутствующими заболеваниями, которые могут еще больше предрасполагать пациентов к тяжелым инфекциям, таким как ex. гипогаммаглобулинемия (см. раздел 4.8). Рекомендуется определять уровень иммуноглобулинов до начала лечения Мабтерой.
Пациенты, у которых наблюдаются признаки и симптомы инфекции после лечения Мабтерой, должны быть незамедлительно обследованы и должным образом пролечены. Перед началом последующего курса лечения Мабтерой следует повторно обследовать пациентов на предмет любого потенциального риска инфекций.
Сообщалось об очень редких случаях фатальной прогрессирующей мультифокальной лейкоэнцефалопатии (ПМЛ) после применения Мабтеры для лечения ревматоидного артрита и аутоиммунных заболеваний, включая системную красную волчанку (СКВ) и васкулит.
Инфекция гепатита B
Сообщалось о случаях реактивации гепатита В, в том числе с летальным исходом, у пациентов с ревматоидным артритом, гранулематозом с полиангиитом и микроскопическим полиангиитом, получавших Мабтеру.
Скрининг на вирус гепатита В (HBV) должен проводиться у всех пациентов до начала лечения Мабтерой и должен включать, по крайней мере, тестирование на HBsAg и HBcAb. Затем эти тесты могут быть дополнены другими подходящими маркерами в соответствии с местными правилами. Пациентам с активной инфекцией гепатита В нельзя принимать Мабтера.Пациенты с положительной серологией на гепатит В (как на HBsAg, так и на HBcAb) должны быть обследованы врачом-гепатологом, а также под наблюдением и наблюдением в соответствии с местными клиническими стандартами для предотвращения реактивации гепатита В.
Поздняя нейтропения
Измеряйте нейтрофилы перед каждым курсом Мабтеры и через регулярные интервалы до 6 месяцев после прекращения лечения и в случае появления признаков или симптомов инфекции (см. Раздел 4.8).
Кожные реакции
Сообщалось о серьезных кожных реакциях, таких как токсический эпидермальный некролиз (синдром Лайелла) и синдром Стивенса-Джонсона, некоторые со смертельным исходом (см. Раздел 4.8). В случае возникновения таких событий, если есть подозрение на связь с Мабтерой, лечение следует окончательно прекратить.
Иммунизация
Перед началом терапии Мабтерой врачи должны проверить вакцинационный статус пациента и следовать текущим рекомендациям по иммунизации.Вакцинация должна быть завершена как минимум за 4 недели до первого введения Мабтеры.
Безопасность иммунизации живыми вирусными вакцинами после терапии Мабтерой не изучалась, поэтому вакцинация живыми вирусными вакцинами не рекомендуется во время терапии Мабтерой или в период истощения периферических В-клеток.
Пациенты, принимающие Мабтера, могут получать вакцины против неживых вирусов. Однако частота ответа на вакцины с неживыми вирусами может быть снижена. В рандомизированном исследовании пациенты с ревматоидным артритом, получавшие Мабтера и метотрексат, имели те же показатели ответа, что и пациенты, получавшие только метотрексат на бустерные антигены столбняка (39% против 42%), сниженные показатели на полисахаридную вакцину. Pneumococcus (43% против 82% по крайней мере к 2 серотипам антипневмококковых антител) и неоантигенам KLH (47% против 93%) при назначении через 6 месяцев после Мабтеры. Если во время терапии Мабтерой требуется вакцинация против неживых вирусов, она должна быть завершена как минимум за 4 недели до начала следующего курса Мабтеры.
В «общемировом опыте повторных курсов лечения Мабтерой в течение одного года в условиях ревматоидного артрита» процент пациентов с положительными титрами антител против S. pneumoniae, грипп, эпидемический паротит, краснуха, ветряная оспа и столбнячный токсин в целом были аналогичны исходным показателям.
Сопутствующее / последовательное использование других DMARD при лечении ревматоидного артрита
Не рекомендуется одновременное применение Мабтеры и противоревматической терапии, кроме тех, которые указаны в показаниях и дозировках для ревматоидного артрита.
Имеются ограниченные данные клинических испытаний, позволяющие полностью оценить безопасность последовательного применения после Мабтеры других БПВП (включая ингибиторы ФНО и другие биопрепараты) (см. Раздел 4.5). Имеющиеся данные указывают на то, что частота клинически значимых инфекций остается неизменной при применении таких методов лечения. используется у пациентов, ранее леченных Мабтерой; тем не менее, пациенты должны тщательно наблюдаться на предмет признаков инфекции, если биологические агенты и / или БПВП используются после терапии Мабтерой.
Новообразования
Иммуномодулирующие препараты могут увеличить риск рака. Основываясь на ограниченном опыте применения Мабтеры у пациентов с ревматоидным артритом (см. Раздел 4.8), текущие данные не предполагают повышенного риска злокачественных новообразований, однако в настоящее время нельзя исключать возможный риск развития солидных опухолей.
04.5 Взаимодействие с другими лекарственными средствами и другие формы взаимодействия
В настоящее время имеются ограниченные данные о возможных лекарственных взаимодействиях с Мабтерой.
У пациентов с ХЛЛ совместный прием с Мабтерой, по-видимому, не влияет на фармакокинетику флударабина или циклофосфамида. Кроме того, нет явного влияния флударабина и циклофосфамида на фармакокинетику Мабтеры.
Совместное применение с метотрексатом не влияло на фармакокинетику Мабтеры у пациентов с ревматоидным артритом.
Пациенты, у которых развились антимышиные или антихимерные антитела (HAMA / HACA), могут иметь аллергические реакции или реакции гиперчувствительности при лечении другими диагностическими или терапевтическими моноклональными антителами.
У пациентов с ревматоидным артритом 283 пациента впоследствии получали биологическую терапию БПВП после введения Мабтеры. У этих пациентов частота клинически значимых инфекций во время терапии Мабтерой составляла 6,01 на 100 пациенто-лет по сравнению с 4,97 на 100 пациенто-лет после биологического лечения БПВП.
04.6 Беременность и кормление грудью
Контрацепция у мужчин и женщин
Поскольку ритуксимаб имеет длительное время удерживания у пациентов с истощением B-клеток, женщинам детородного возраста следует использовать эффективные методы контрацепции во время лечения и в течение 12 месяцев после завершения терапии Мабтерой.
Беременность
Известно, что иммуноглобулины IgG проникают через плацентарный барьер.
Уровни В-клеток у детей грудного возраста после воздействия мабтеры на мать не оценивались в клинических испытаниях. Нет адекватных и хорошо контролируемых данных исследований с участием беременных женщин, однако сообщалось о временном истощении В-клеток и лимфоцитопении у младенцев, рожденных от матерей, подвергшихся воздействию Мабтеры во время беременности. Подобные эффекты наблюдались в исследованиях на животных (см. Раздел 5.3). По этой причине Мабтера не следует назначать беременным женщинам, если возможная польза не превышает потенциальный риск.
Грудное вскармливание
Неизвестно, выделяется ли ритуксимаб с грудным молоком. Однако, поскольку материнский IgG выделяется с грудным молоком, а ритуксимаб был обнаружен в молоке кормящих обезьян, женщинам не следует кормить грудью во время лечения Мабтерой и в течение 12 месяцев после лечения Мабтерой.
Плодородие
Исследования на животных не выявили вредного воздействия ритуксимаба на репродуктивные органы.
04.7 Влияние на способность управлять автомобилем и работать с механизмами
Исследования влияния Мабтеры на способность управлять транспортными средствами и механизмами не проводились, хотя фармакологическая активность и побочные реакции, о которых сообщалось на сегодняшний день, позволяют предположить, что Мабтера не оказывает или оказывает незначительное влияние на способность управлять автомобилем или управлять транспортными средствами.
04.8 Побочные эффекты
Опыт лечения неходжкинской лимфомы и хронического лимфолейкоза
Резюме профиля безопасности
Общий профиль безопасности Мабтеры при неходжкинской лимфоме и хроническом лимфолейкозе основан на данных пациентов, участвовавших в клинических испытаниях и постмаркетинговом наблюдении. Эти пациенты получали лечение Мабтерой в виде монотерапии (в качестве индукционной терапии или в качестве поддерживающей терапии после индукции) или в сочетании с химиотерапией.
Наиболее часто наблюдаемыми нежелательными лекарственными реакциями (НЛР) у пациентов, получавших Мабтеру, были ВСН, которые наблюдались у большинства пациентов во время первой инфузии. Частота возникновения симптомов, связанных с инфузией, значительно снижается при последующих инфузиях и составляет менее 1% после восьми доз Мабтеры.
Инфекционные события (в основном бактериальные и вирусные) произошли примерно у 30-55% пациентов с НХЛ, получавших лечение в клинических испытаниях, и примерно у 30-50% пациентов с ХЛЛ, получавших лечение в клинических испытаниях. Наиболее частыми или наблюдаемыми серьезными побочными реакциями на лекарства были:
• ВСД (включая синдром высвобождения цитокинов и синдром лизиса опухоли), см. Раздел 4.4.
• Инфекции, см. Раздел 4.4.
• Сердечно-сосудистые события, см. Раздел 4.4.
Другие серьезные нежелательные реакции, о которых сообщалось, включают реактивацию гепатита В и ПМЛ (см. Раздел 4.4).
Список побочных реакций в виде таблицы
Частота нежелательных реакций, о которых сообщалось при применении монотерапии Мабтерой или в сочетании с химиотерапией, сведена в Таблицу 1. В рамках каждого класса частоты нежелательные эффекты перечислены в порядке уменьшения степени тяжести. Частота определяется как очень часто (≥ 1/10), часто ( ≥ 1/100 до
Нежелательные реакции, выявленные только в ходе постмаркетингового наблюдения и частота которых не может быть оценена, перечислены в графе «неизвестно».
Таблица 1 Нежелательные реакции, зарегистрированные в клинических испытаниях или во время постмаркетингового наблюдения у пациентов с НХЛ и ХЛЛ, получавших Мабтера в качестве монотерапии / поддерживающей терапии или в сочетании с химиотерапией.
Следующие термины были зарегистрированы как нежелательные явления во время клинических испытаний; однако гематологическая токсичность, нейтропеническая инфекция, инфекция мочевыводящих путей, сенсорные нарушения, гипертермия наблюдались с аналогичной или меньшей частотой в группах Мабтеры по сравнению с контрольными группами.
Характерные признаки и симптомы ВСД были зарегистрированы более чем у 50% пациентов в ходе клинических исследований и наблюдались в основном во время первой инфузии, обычно в первые два часа. Эти симптомы в основном включают жар, озноб и скованность. Другие симптомы включают покраснение кожи, ангионевротический отек, бронхоспазм, рвоту, тошноту, крапивницу / сыпь, усталость, головную боль, раздражение горла, ринит, зуд, боль, тахикардию, гипертензию, гипотензию, одышку, диспепсию, астению и симптомы синдрома лизиса опухоли. Тяжелые ИР (такие как бронхоспазм, гипотензия) наблюдались в 12% случаев. В некоторых случаях сообщалось о дополнительных реакциях: инфаркт миокарда, фибрилляция предсердий, отек легких и острая обратимая тромбоцитопения. Обострение ранее существовавших сердечных заболеваний, таких как стенокардия или застойная сердечная недостаточность, или тяжелые сердечные заболевания (сердечная недостаточность, инфаркт миокарда, фибрилляция предсердий), отек легких, полиорганная недостаточность, синдром лизиса опухоли, синдром высвобождения цитокинов, почечная и респираторная недостаточность об отказе сообщалось с более низкой или неизвестной частотой.Частота симптомов, связанных с инфузией, значительно снизилась при последующих инфузиях и
Описание ряда побочных реакций
Инфекции
Мабтера вызывает истощение В-клеток примерно у 70-80% пациентов, но это событие было связано со снижением сывороточного иммуноглобулина только у меньшинства пациентов.
Локализованные кандидозные инфекции, такие как опоясывающий герпес, чаще регистрировались в группе Мабтеры в рандомизированных исследованиях. О серьезных инфекциях сообщалось примерно у 4% пациентов, получавших монотерапию Мабтерой. Во время двухлетнего поддерживающего лечения Мабтерой наблюдались более высокие показатели всех инфекций, включая инфекции 3-й или 4-й степени, по сравнению с наблюдением. Кумулятивной токсичности в отношении инфекций, зарегистрированных в течение двухлетнего периода лечения, не было. Сообщалось о других серьезных вирусных инфекциях, новых, реактивных или обостренных, во время лечения Мабтерой, некоторые из которых закончились смертельным исходом. Большинство пациентов получали Мабтеру в сочетании с химиотерапией или как часть трансплантации гемопоэтических стволовых клеток. Примеры этих серьезных вирусных инфекций - инфекции, вызываемые герпетическими вирусами (цитомегаловирус, вирус ветряной оспы и простой герпес), вирусом JC (прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ)) и вирусным гепатитом С. Случаи смертельного ПМЛ также были зарегистрированы во время клинических испытаний и имели место. ti после прогрессирования заболевания и повторного лечения. Сообщалось о случаях реактивации гепатита В, большинство из которых произошло у пациентов, получавших Мабтеру в сочетании с цитотоксической химиотерапией. У пациентов с рецидивирующим / рефрактерным ХЛЛ частота инфицирования гепатитом В 3/4 степени (реактивация и первичная инфекция) составляла 2% в группе R-FC по сравнению с 0% в группе FC. Наблюдалось прогрессирование саркомы Капоши. ранее существовавшая саркома Капоши. Эти случаи имели место по неутвержденным показаниям, и большинство пациентов были ВИЧ-положительными.
Гематологические побочные реакции
В клинических испытаниях с использованием Мабтеры в качестве монотерапии в течение 4 недель гематологические отклонения наблюдались у меньшинства пациентов и, как правило, были легкими и обратимыми. Тяжелая нейтропения (степень 3/4) наблюдалась у 4,2% пациентов, анемия - у 1,1% и тромбоцитопения - у 1,7% пациентов. На фоне двухлетнего поддерживающего лечения Мабтерой лейкопения (5% против 2%, степень 3/4) и нейтропения (10% против 4%, степень 3/4) были зарегистрированы с более высокой частотой по сравнению с наблюдением. Частота тромбоцитопении была низкой (
Во время лечения в исследованиях Мабтерой в сочетании с химиотерапией лейкопения 3/4 степени (R-CHOP 88% против CHOP 79%, R-FC 23% против HR 12%), нейтропения (R-CVP 24% против CVP 14%; R-CHOP 97% против CHOP 88%, R-FC 30% против HR 19% при ранее нелеченом CLL), панцитопения (R-FC 3% против CF 1% в ранее нелеченых CLL), как правило, сообщалось с более высокой частотой по сравнению с одной химиотерапией.
Однако более высокая частота нейтропении у пациентов, получавших Мабтера и химиотерапию, не была связана с более высокой частотой инфекций и инвазий по сравнению с пациентами, получавшими только химиотерапию. Ранее нелеченные и рецидивирующие / рефрактерные исследования ХЛЛ установили, что у 25% пациентов, получавших лечение с R-FC нейтропения была продолжительной (определялась как количество нейтрофильных гранулоцитов менее 1x109 / л между 24-м и 42-м днями после последней дозы) или имела место с поздним началом (определяемое как количество нейтрофильных гранулоцитов менее 1x109 / л после 42-го дня. после последней дозы у пациентов, у которых не было пролонгированной нейтропении в прошлом или которые выздоровели до 42 дня) после лечения Мабтерой и CF. Различия в частоте анемии не выявлены. Сообщалось о некоторых случаях поздней нейтропении, возникающей более чем через четыре недели после последней инфузии Мабтеры. В исследовании первой линии ХЛЛ пациенты со стадией С по Бине испытали больше нежелательных явлений в группе R-FC, чем в группе HR ( R-FC 83% против HR 71%). В исследовании рецидивирующего / рефрактерного ХЛЛ тромбоцитопения 3/4 степени была зарегистрирована у 11% пациентов в группе RFC по сравнению с 9% пациентов в группе CF.
В исследованиях с применением Мабтеры у пациентов с макроглобулинемией Вальдестрома после начала лечения наблюдалось временное повышение уровня сывороточного IgM, которое может быть связано с повышенной вязкостью и связанными с ним симптомами. Временное повышение уровня IgM обычно возвращается как минимум к исходному уровню. месяцы.
Сердечно-сосудистые побочные реакции
В клинических испытаниях с применением только одной Мабтеры сердечно-сосудистые реакции были зарегистрированы у 18,8% пациентов с гипотензией и гипертензией как наиболее часто встречающиеся события. Сообщалось о случаях аритмий 3 или 4 степени (включая желудочковую и наджелудочковую тахикардию) и стенокардии во время инфузии. Во время поддерживающего лечения частота сердечных нарушений 3/4 степени была сопоставима среди пациентов, получавших лечение Мабтерой и наблюдением. Сердечные события были Сообщалось о серьезных нежелательных явлениях (включая фибрилляцию предсердий, инфаркт миокарда, левожелудочковую недостаточность, ишемию миокарда) у 3% пациентов, получавших Мабтера, по сравнению с сердечными аритмиями 3 и 4 степени, особенно наджелудочковыми аритмиями, такими как тахикардия и трепетание / фибрилляция предсердий. выше в группе RCHOP (14 пациентов, 6,9%) по сравнению с группой CHOP (3 пациента, 1,5%). Все эти аритмии возникли в контексте инфузии Мабтеры или были связаны с предрасполагающими состояниями, такими как лихорадка, инфекция, острый инфаркт миокарда или ранее существовавшие респираторные и сердечно-сосудистые заболевания. Никаких различий между группами R-CHOP и CHOP с точки зрения не наблюдалось. частоты других сердечных приступов 3 и 4 степени, включая сердечную недостаточность, заболевание миокарда и проявления ишемической болезни сердца. При ХЛЛ общая частота сердечных расстройств 3 или 4 степени была низкой как в исследовании первой линии (4% R-FC, 3% FC), так и в исследовании с рецидивами / рефрактерными (4% R-FC, 4% FC). .
Дыхательная система
Сообщалось о случаях интерстициального заболевания легких, некоторые со смертельным исходом.
Неврологические патологии
В течение периода лечения (фаза индукционной терапии, состоящей из R-CHOP до восьми циклов) четыре пациента (2%), получавших R-CHOP, все с факторами риска сердечно-сосудистых заболеваний, испытали цереброваскулярные тромбоэмболические нарушения во время первого цикла лечения. Не было различий между группами лечения с точки зрения частоты других тромбоэмболических событий. Напротив, у трех пациентов (1,5%) были цереброваскулярные события в группе CHOP, все из которых произошли в течение периода наблюдения. ХЛЛ, общая частота расстройств нервной системы 3 или 4 степени была низкой как в исследовании первой линии (4% R-FC, 4% FC), так и в исследовании рецидива / рефрактерности (3% R-FC, 3% FC). .
Сообщалось о случаях синдрома задней обратимой энцефалопатии (PRES) / синдрома задней обратимой лейкоэнцефалопатии (RPLS). Признаки и симптомы включали нарушения зрения, головную боль, судороги и изменения психического статуса с гипертонией или без нее. Диагноз PRES / RPLS требует подтверждения визуализация церебральный. В зарегистрированных случаях выявлены факторы риска PRES / RPLS, включая статус сопутствующего заболевания пациента, артериальную гипертензию, иммуносупрессивную терапию и / или химиотерапию.
Желудочно-кишечные расстройства
Перфорация желудочно-кишечного тракта, в некоторых случаях приводившая к летальному исходу, наблюдалась у пациентов, получавших Мабтеру для лечения неходжкинской лимфомы. В большинстве этих случаев Мабтера применялась с химиотерапией.
Уровни IgG
В клиническом исследовании, посвященном оценке Мабтеры в качестве поддерживающей терапии при рецидивирующей / рефрактерной фолликулярной лимфоме, медианные уровни IgG были ниже нижнего предела нормы (LLN) (
Небольшое количество спонтанных и литературных случаев, связанных с гипогаммаглобулинемией, в некоторых случаях тяжелой и требующей длительной заместительной иммуноглобулиновой терапии, наблюдалось у педиатрических пациентов, получавших Мабтера. Последствия длительного истощения В-клеток у педиатрических пациентов неизвестны.
Заболевания кожи и подкожной клетчатки:
О случаях токсического эпидермального некролиза (синдром Лайелла) и синдрома Стивенса-Джонсона, некоторые со смертельным исходом, сообщалось очень редко.
Субпопуляции пациентов - монотерапия Мабтерой
Пожилые пациенты (≥ 65 лет):
Частота нежелательных реакций всех степеней и 3/4 степени была сходной у пожилых и более молодых пациентов (
Объемное заболевание
У пациентов с объемным заболеванием частота нежелательных реакций 3/4 степени была выше, чем у пациентов без объемного заболевания (25,6%). против 15,4%). Частота нежелательных реакций всех степеней в этих двух группах была одинаковой.
Повторное лечение
Доля пациентов, сообщивших о нежелательных реакциях во время повторного лечения с последующими курсами Мабтеры, была аналогична доле пациентов, сообщивших о нежелательных реакциях на лечение во время первоначального воздействия (нежелательные реакции всех степеней и 3/4 степени).
Субпопуляции пациентов - комбинированная терапия с Мабтерой
Пожилые пациенты (≥ 65 лет)
Частота нежелательных явлений 3/4 степени со стороны крови и лимфатической системы была выше у пожилых пациентов по сравнению с более молодыми пациентами (
Опыт лечения ревматоидного артрита
Резюме профиля безопасности
Общий профиль безопасности Мабтеры при ревматоидном артрите основан на данных пациентов, пролеченных в ходе клинических исследований, и на данных постмаркетингового наблюдения.
Профиль безопасности Мабтеры у пациентов с ревматоидным артритом средней и тяжелой степени тяжести кратко изложен в следующих разделах. В клинических исследованиях более 3100 пациентов прошли по крайней мере один курс лечения и наблюдались в течение периода от 6 месяцев до более 5 лет; примерно 2400 пациентов прошли два или более курсов лечения, более 1000 пациентов прошли 5 и более курсов. Информация о безопасности, полученная в результате постмаркетингового опыта, отражает профиль ожидаемых побочных реакций, уже наблюдаемых в клинических исследованиях Мабтеры (см. Раздел 4.4).
Пациенты получали 2 дозы Мабтеры по 1000 мг с интервалом в две недели в комбинации с метотрексатом (10-25 мг / неделя). Инфузии Мабтеры вводились после внутривенной инфузии 100 мг метилпреднизолона; пациенты также получали пероральное лечение преднизоном в течение 15 дней.
Список побочных реакций в виде таблицы
Побочные реакции перечислены в таблице 2. Частота определяется как очень часто (≥ 1/10), часто (≥1 / 100 до
Наиболее частыми побочными реакциями, вызванными приемом Мабтеры, были ВНД.
Общая частота ВСД в клинических испытаниях составила 23% при первой инфузии и снизилась при последующих инфузиях. Серьезные ВСД были редкостью (0,5% пациентов) и возникали преимущественно во время начального цикла. В дополнение к побочным реакциям, наблюдаемым при клиническом ревматоидном артрите Сообщалось об исследованиях, проведенных с Мабтерой, прогрессирующей мультифокальной лейкоэнцефалопатией (ПМЛ) и реакциями, подобными сывороточной болезни, во время постмаркетингового опыта.
Таблица 2 Сводная информация о побочных реакциях на лекарства, о которых сообщалось в клинических испытаниях или во время постмаркетингового наблюдения, которые имели место у пациентов с ревматоидным артритом, получавших Мабтеру
Повторные циклы
Повторные курсы лечения связаны с профилем побочных реакций, аналогичным тому, который наблюдается после первого воздействия. Частота всех побочных реакций после первого приема Мабтеры была максимальной в течение первых 6 месяцев и впоследствии снизилась. В основном это касается ВСД (чаще всего во время первого лечения), обострения ревматоидного артрита и инфекций; все они были более частыми в первые 6 месяцев лечения.
Реакции, связанные с инфузией
В клинических исследованиях наиболее частыми побочными реакциями (НЛР) после лечения Мабтерой были ВНД (см. Таблицу 2). Среди 3189 пациентов, получавших MabThera, 1135 (36%) имели по крайней мере один IRR, при этом 733/3189 (23%) пациентов испытали IRR после первой инфузии первого лечения MabThera. Частота ВСД снижается при последующих инфузиях. В клинических исследованиях менее 1% (17/3 189) пациентов испытали тяжелую ВСД. В клинических испытаниях не было ВС 4 степени по Общим критериям токсичности (CTC) и не было случаев смерти из-за ВС. Доля событий CTC степени 3 и IRR, приводящих к прекращению лечения, уменьшалась в течение курса лечения и становилась редкостью, начиная с цикла 3 и далее. Внутривенная премедикация глюкокортикоидами значительно снизила частоту и тяжесть ВСД (см. Разделы 4.2 и 4.4). В постмаркетинговых условиях сообщалось о тяжелых случаях ВСД с летальным исходом.
В исследовании, предназначенном для оценки безопасности «более быстрой инфузии Мабтеры у пациентов с ревматоидным артритом, пациентам с активным ревматоидным артритом от умеренной до тяжелой степени, у которых не было тяжелого ИР в течение или в течение 24 часов после первой исследуемой инфузии, было разрешено пройти 2-часовую внутривенную инфузию Мабтеры. Пациенты с тяжелой инфузионной реакцией на биологическую терапию ревматоидного артрита в анамнезе не включались в исследование. Частота, типы и тяжесть ВСД соответствовали историческим данным. Серьезных ВСД не наблюдалось.
Описание ряда побочных реакций
Инфекции
Общая частота инфекций составляла примерно 94 на 100 пациенто-лет в группе Мабтеры. Инфекции были в основном легкой и средней степени тяжести и включали в основном инфекции верхних дыхательных путей и мочевыводящих путей. Им потребовалось внутривенное введение антибиотиков. это было около 4 из 100 пациенто-лет. Частота серьезных инфекций не показала значительного увеличения после повторных курсов с Мабтерой. Инфекции нижних дыхательных путей (включая пневмонию) были зарегистрированы в клинических испытаниях, с аналогичной частотой в группах Мабтеры по сравнению с группами Мабтеры.
Сообщалось о случаях прогрессирующей мультифокальной лейкоэнцефалопатии с летальным исходом после применения Мабтеры для лечения аутоиммунных состояний. К ним относятся ревматоидный артрит и аутоиммунные состояния, не имеющие показаний, такие как системная красная волчанка (СКВ) и васкулит.
Сообщалось о случаях реактивации гепатита В у пациентов с неходжкинской лимфомой, получавших Мабтеру в сочетании с цитотоксической химиотерапией (см. Неходжкинская лимфома). О реактивации инфекции гепатита B также сообщалось очень редко у пациентов с РА, получавших Мабтеру (см. Раздел 4.4).
Сердечно-сосудистые побочные реакции
Серьезные сердечные реакции наблюдались с частотой 1,3 на 100 пациенто-лет среди тех, кто лечился Мабтерой, и 1,3 на 100 пациенто-лет у пациентов, получавших плацебо. Доля пациентов с сердечными реакциями (полными или тяжелыми) не увеличивалась в различные циклы.
Неврологические события
Сообщалось о случаях заднего обратимого энцефалопатического синдрома (PRES) / синдрома задней обратимой лейкоэнцефалопатии (RPLS). Признаки и симптомы включали нарушения зрения, головные боли, судороги и измененное психическое состояние с гипертонией или без нее. Диагноз PRES / RPLS требует подтверждения с помощью изображения головного мозга. В описанных случаях были известны факторы риска PRES / RPLS, включая основное заболевание пациентов, артериальную гипертензию, иммуносупрессивную терапию и / или химиотерапию.
Нейтропения
После лечения Мабтерой наблюдались случаи нейтропении, большинство из которых были преходящими, легкой или средней степени тяжести. Нейтропения может возникнуть через несколько месяцев после приема Мабтеры (см. Раздел 4.4).
В плацебо-контролируемых клинических исследованиях тяжелая нейтропения развивалась у 0,94% (13/382) пациентов, получавших Мабтера, и у 0,27% (2/731) пациентов, получавших плацебо.
Нейтропенические события, включая тяжелую и стойкую нейтропению с поздним началом, некоторые из которых были связаны со смертельными инфекциями, редко регистрировались в постмаркетинговом опыте.
Заболевания кожи и подкожной клетчатки
О случаях токсического эпидермального некролиза (синдром Лайелла) и синдрома Стивенса-Джонсона, некоторые со смертельным исходом, сообщалось очень редко.
Лабораторные аномалии
Гипогаммаглобулинемия (IgG или IgM ниже нижней границы нормы) наблюдалась у пациентов с ревматоидным артритом, получавших Мабтера. Не наблюдалось увеличения частоты общих или тяжелых инфекций после низкого уровня IgG или IgM (см. Раздел 4.4).
Небольшое количество спонтанных и литературных случаев, связанных с гипогаммаглобулинемией, в некоторых случаях тяжелой и требующей длительной заместительной иммуноглобулиновой терапии, наблюдалось у педиатрических пациентов, получавших Мабтера. Последствия длительного истощения В-клеток у педиатрических пациентов неизвестны.
Опыт лечения гранулематоза с полиангиитом и микроскопическим полиангиитом.
В клиническом исследовании гранулематоза с полиангиитом и микроскопическим полиангиитом 99 пациентов лечились Мабтерой (375 мг / м2 один раз в неделю в течение 4 недель) и глюкокортикоидами (см. Раздел 5.1).
Список побочных реакций в виде таблицы
ADR, перечисленные в таблице 3, представляют все нежелательные явления, которые произошли с частотой ≥ 5% в группе Мабтера.
Таблица 3: Побочные реакции на лекарства, возникающие у ≥ 5% пациентов, получавших Мабтеру с более высокой частотой, чем в группе сравнения, в 6-месячном базовом клиническом исследовании.
Подбор побочных реакций на лекарства
Реакции, связанные с инфузией
IRR в клинических исследованиях, относящихся к гранулематозу с полиангиитом и микроскопическому полиангииту, определяли как любое нежелательное явление, происходящее в течение 24 часов после инфузии, и считали инфузию связанным исследователем в популяции безопасности. 99 пациентов лечились Мабтерой, и у 12% наблюдалось хотя бы одно ВСД. Все IRR были 1 или 2 степени согласно CTC. Наиболее частые ВСД включали синдром высвобождения цитокинов, приливы, раздражение и тремор в горле. Мабтера вводили в комбинации с внутривенными глюкокортикоидами, что может снизить частоту и тяжесть этих явлений.
Инфекции
У 99 пациентов, получавших Мабтеру, общая частота инфекций составляла примерно 237 на 100 пациенто-лет (95% ДИ 197–285) на 6-месячной первичной конечной точке. Инфекции были преимущественно легкими или умеренными и состояли в основном из инфекций. инфекции мочевыводящих путей, опоясывающего лишая и мочевыводящих путей. Частота серьезных инфекций составляла примерно 25 на 100 пациенто-лет. Наиболее частой серьезной инфекцией в группе Мабтеры была пневмония с частотой 4%.
Новообразования
Частота злокачественных новообразований у пациентов, получавших Мабтера, в клинических исследованиях, касающихся гранулематоза с полиангиитом и микроскопическим полиангиитом, составила 2,00 на 100 пациенто-лет на дату окончания совместного исследования (когда последний пациент завершил период наблюдения). Основываясь на стандартизированном соотношении заболеваемости, частота злокачественных новообразований, по-видимому, аналогична той, о которой ранее сообщалось у пациентов с ANCA-ассоциированным васкулитом.
Сердечно-сосудистые побочные реакции
Частота сердечных событий составляла примерно 273 на 100 пациенто-лет (95% ДИ 149–470) на 6-месячной первичной конечной точке. Частота серьезных сердечных событий составляла 2,2 на 100 пациенто-лет (95% ДИ 3-15). Наиболее частыми нежелательными явлениями были тахикардия (4%) и фибрилляция предсердий (3%) (см. Раздел 4.4).
Реактивация гепатита В
Сообщалось о небольшом количестве случаев реактивации гепатита В, некоторые со смертельным исходом, у пациентов с гранулематозом с полиангиитом и микроскопическим полиангиитом, получавших Мабтера в постмаркетинговых условиях.
Неврологические события
Сообщалось о случаях заднего обратимого энцефалопатического синдрома (PRES) / синдрома задней обратимой лейкоэнцефалопатии (RPLS). Признаки и симптомы включали нарушения зрения, головные боли, судороги и измененное психическое состояние с гипертонией или без нее. Диагноз PRES / RPLS требует подтверждения с помощью изображения головного мозга. В описанных случаях были известны факторы риска PRES / RPLS, включая основное заболевание пациента, гипертонию, иммуносупрессивную терапию и / или химиотерапию.
Гипогаммаглобулинемия
Гипогаммаглобулинемия (IgA, IgG или IgM ниже нижней границы нормы) наблюдалась у пациентов с гранулематозом с полиангиитом и микроскопическим полиангиитом, получавших Мабтера. В 6-месячном многоцентровом рандомизированном двойном слепом исследовании не меньшей эффективности с активным контролем в группе Мабтеры у 27%, 58% и 51% пациентов с нормальным исходным уровнем иммуноглобулина были низкие уровни IgA. IgG и IgM, соответственно, по сравнению с 25%, 50% и 46% группы циклофосфамида. Повышенного уровня общих инфекций или серьезных инфекций не наблюдалось у пациентов с низким уровнем IgA, IgG или IgM.
Нейтропения
В многоцентровом рандомизированном двойном слепом активно-контролируемом исследовании не меньшей эффективности Мабтеры при гранулематозе с полиангиитом и микроскопическим полиангиитом участвовали 24% пациентов в группе Мабтеры (один цикл) и 23% пациентов в группе циклофосфамида. развилась нейтропения 3 степени или выше. Нейтропения не была связана с наблюдаемым увеличением числа серьезных инфекций у пациентов, получавших Мабтера. Влияние многократных курсов Мабтеры на развитие нейтропении у пациентов с гранулематозом с полиангиитом и микроскопическим полиангиитом в клинических исследованиях не изучалось.
Заболевания кожи и подкожной клетчатки
Очень редко сообщалось об эпизодах токсического эпидермального некролиза (синдром Лайелла) и синдрома Стивенса-Джонсона, некоторые со смертельным исходом.
Сообщение о предполагаемых побочных реакциях
Отчетность о предполагаемых побочных реакциях, возникающих после получения разрешения на лекарственный препарат, важна, поскольку позволяет осуществлять непрерывный мониторинг баланса пользы и риска лекарственного средства. Медицинских работников просят сообщать о любых предполагаемых побочных реакциях через национальную систему отчетности.
04.9 Передозировка
Имеется ограниченный опыт клинических испытаний на людях с дозами выше, чем одобренные для внутривенного введения Мабтеры. Самая высокая внутривенная доза Мабтеры, испытанная на людях на сегодняшний день, составляет 5000 мг (2250 мг / м2), что было протестировано в исследовании повышения дозы в пациенты с хроническим лимфолейкозом. Других знаков безопасности обнаружено не было.
Пациенты, которые столкнулись с передозировкой, должны немедленно прекратить инфузию и находиться под тщательным наблюдением. Постмаркетинговые сообщения о пяти случаях передозировки Мабтеры. В трех из этих случаев не было зарегистрировано нежелательных явлений. Два сообщенных нежелательных явления были схожими симптомами. - грипп с Доза 1,8 г ритуксимаба и респираторная недостаточность со смертельным исходом при дозе 2 г ритуксимаба.
05.0 ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
05.1 Фармакодинамические свойства
Фармакотерапевтическая группа: противоопухолевые средства, моноклональные антитела, код ATC: L01X C02 Ритуксимаб специфически связывается с трансмембранным антигеном CD20, негликозилированным фосфопротеином, обнаруженным на пре-B и зрелых B-клетках. Антиген экспрессируется более чем на 95% всех B. -клеточные неходжкинские лимфомы (НХЛ).
CD20 обнаруживается в нормальных и неопластических В-клетках, но не в гемопоэтических стволовых клетках, про-В-клетках, нормальных плазматических клетках или других нормальных тканях. Антиген не интернализуется после связывания антитела и не распространяется с поверхности клетки. CD20 не циркулирует в крови в качестве свободного антигена и, следовательно, не конкурирует со связыванием антител. Fab-домен ритуксимаба связывается с антигеном CD20 на В-лимфоцитах. ..и домен Fc может активировать эффекторные функции иммунной системы с целью вызвать лизис В-клеток.Возможные механизмы эффекторно-опосредованного лизиса клеток включают комплемент-зависимую цитотоксичность (CDC) через связывание C1q и антителозависимую клеточную цитотоксичность (ADCC), опосредованную одним или несколькими рецепторами Fcγ на поверхности гранулоцитов, макрофагов и NK-клеток. Связывание ритуксимаба с Антиген CD20 на В-лимфоцитах также вызывает гибель клеток в результате апоптоза.
Количество периферических В-клеток упало ниже нормы после приема первой дозы Мабтеры. У пациентов, получающих лечение по поводу гематологического рака, восстановление В-клеток начинается в течение 6 месяцев после лечения и обычно возвращается к нормальному уровню в течение 12 месяцев после завершения терапии, хотя у некоторых пациентов выздоровление может длиться дольше (в среднем выздоровление составляет 23 месяца после индукции. терапия). У пациентов с ревматоидным артритом наблюдалось немедленное истощение В-клеток периферической крови после двух инфузий Мабтеры по 1000 мг каждая с интервалом в 14 дней. Количество периферических В-клеток начинает увеличиваться с 24-й недели, а признаки выздоровления у большинства пациентов появляются с 40-й недели, как при приеме Мабтеры.
назначают отдельно и при приеме в сочетании с метотрексатом. У небольшого процента пациентов наблюдалось длительное истощение периферических В-клеток в течение 2 лет или более после приема последней дозы Мабтеры. У пациентов с гранулематозом с полиангиитом или микроскопическим полиангиитом количество В-клеток периферической крови снизилось до 2 и оставалось на этом уровне в большинство пациентов до момент времени 6 месяцев. У большинства пациентов (81%) наблюдались признаки восстановления В-клеток с количеством> 10 клеток / мкл в течение 12 месяцев, достигая 87% пациентов к 18 месяцу.
Клинический опыт лечения неходжкинской лимфомы и хронического лимфолейкоза.
Фолликулярная лимфома
Монотерапия
Начальное лечение, еженедельно, 4 дозы
В опорном исследовании 166 пациентов с рецидивом или химиорезистентной низкосортной или фолликулярной B-клеточной НХЛ получали 375 мг / м2 Мабтеры в виде внутривенной инфузии один раз в неделю в течение четырех недель. Процент общих ответов (ЧОО) в популяции, оцененных в соответствии с "намерение лечить анализ (ITT) составлял 48% (95% ДИ 41% - 56%) с 6% полными ответами (CR) и 42% частичными ответами (PR). Среднее время до прогрессирования (ВДП) для пациентов, ответивших на лечение, составило 13,0 месяцев. В анализе подгрупп, ЧОО была выше у пациентов с гистологическими подтипами B, C и D IWF по сравнению с пациентами с гистологическими подтипами A IWF (58% против 12%), у пациентов с большим диаметром поражения 7 см (53% против 38%). ) и у пациентов с химиочувствительным рецидивом по сравнению с пациентами с химиорезистентным рецидивом (определяется как продолжительность ответа
ЧОО у пациентов, ранее получавших аутологичную трансплантацию костного мозга (ABMT), составляла 78% по сравнению с 43% у пациентов, ранее не получавших ABMT. Возраст, пол, степень лимфомы, первоначальный диагноз, наличие или отсутствие объемного заболевания, нормальный или повышенный уровень ЛДГ , наличие экстранодального заболевания не оказало статистически значимого влияния (точный критерий Фишера) на ответ на Мабтеру. Статистически значимая корреляция была выявлена между частотой ответа и поражением костного мозга. 40% пациентов с поражением костного мозга ответили на лечение по сравнению с 59% пациентов. без вовлечения костного мозга (p = 0,0186). Этот результат не был подтвержден анализом так называемой «пошаговой логистической регрессии», в котором следующие факторы были определены как прогностические факторы: гистологический тип, исходная положительность bcl-2, устойчивость к последней химиотерапии и объемное заболевание.
Начальное лечение, еженедельно, 8 доз
В многоцентровом исследовании с участием одной группы 37 пациентов с рецидивом или химиорезистентной, низкосортной или фолликулярной B-клеточной НХЛ получали Мабтера 375 мг / м2 в виде еженедельной внутривенной инфузии восьми доз. ЧОО составила 57% (95% доверительный интервал (ДИ): 41–73%; CR 14%, PR 43%) со средним прогнозом ВДП для респондентов 19,4 месяца (диапазон от 5,3 до 38,9 месяцев).
Начальное лечение, тяжелое заболевание, еженедельно по 4 дозы
В пуле данных из 3 исследований 39 пациентов с рецидивом или химиорезистентной НХЛ, объемным заболеванием (единичное поражение ≥ 10 см в диаметре), низкосортной или фолликулярной В-клеточной болезнью получали Мабтера 375 мг / м2 в виде еженедельной внутривенной инфузии для четырех человек. дозы. ЧОО составляла 36% (95% ДИ 21% - 51%; CR 3%, PR 33%) со средней ВДП для ответивших пациентов 9,6 месяцев (диапазон 4,5 - 26,8 месяцев).
Повторное лечение, еженедельно на 4 приема
В многоцентровом исследовании с одной группой 58 пациентов с рецидивом или химиорезистентной низкосортной или фолликулярной B-клеточной НХЛ, у которых был достигнут объективный клинический ответ на предыдущий курс лечения Мабтерой, были повторно пролечены Мабтерой в дозе 375 мг / м2 в качестве препарата. еженедельная внутривенная инфузия за четыре приема. Трое из этих пациентов получили два курса Мабтеры до включения в исследование и, таким образом, получили третий курс в исследовании. Двое пациентов в исследовании дважды были подвергнуты повторному лечению. Для 60 повторных курсов в исследовании ЧОО составила 38% (95% ДИ 26% - 51%; 10% ПО, 28% ЧО) со средним прогнозом ВДП для ответивших пациентов 17,8 месяцев (диапазон 5, 4-26,6). . Эти данные лучше, чем ТТП, полученная после первого курса Мабтеры (12,4 мес).
Первоначальное лечение в сочетании с химиотерапией
В рандомизированном открытом клиническом исследовании 322 ранее не леченных пациента с фолликулярной лимфомой были рандомизированы для получения химиотерапии ЦВД (циклофосфамид 750 мг / м2, винкристин 1,4 мг / м2 до максимальной дозы 2 мг в день 1 и преднизолон. 40 мг / м2 / день в дни 1-5) каждые 3 недели в течение 8 циклов или Мабтера 375 мг / м2 в сочетании с CVP (R-CVP).
Мабтера вводили в первый день каждого цикла лечения. Всего 321 пациент (162 R-CVP, 159 CVP) получил терапию и был проанализирован на эффективность. Среднее время наблюдения за пациентами составило 53 месяца. R-CVP привел к значительному преимуществу по сравнению с CVP для первичной конечной точки, то есть времени до неэффективности лечения (27 месяцев по сравнению с 6,6 месяцами, p
Разница между группами лечения в общей выживаемости показала значительную клиническую разницу (p = 0,029, лог-ранговый тест, стратифицированный по центру): 53-месячная выживаемость составила 80,9% для пациентов в группе R. ЦВД по сравнению с 71,1% для пациентов в группе CVP.
Результаты трех других рандомизированных исследований с использованием Мабтеры в сочетании с режимами химиотерапии без ЦВД (CHOP, MCP, CHVP / Интерферон-α) также продемонстрировали значительное улучшение показателей ответа, параметров, зависящих от времени, и общей выживаемости. Наиболее важные результаты всех четырех исследований представлены в таблице 4.
Таблица 4 Краткое изложение основных результатов четырех рандомизированных исследований фазы III, оценивающих эффективность Мабтеры при различных режимах химиотерапии при фолликулярной лимфоме.
EFS - Выживание без событий
ВДП - Время прогрессировать или умереть
PFS - Выживание без прогрессирования
TTF - Время до неэффективности лечения
OS проценты - выживаемость на момент анализа
Поддерживающая терапия
Ранее нелеченая фолликулярная лимфома
В проспективном открытом международном многоцентровом исследовании III фазы 1193 пациента с ранее нелеченой распространенной фолликулярной лимфомой получали индукционную терапию R-CHOP (n = 881), R-CVP (n = 268) или R-FCM (n). = 44), по выбору исследователя. В общей сложности 1078 пациентов ответили на индукционную терапию, из которых 1018 были рандомизированы для получения поддерживающей терапии Мабтерой (n = 505) или наблюдения (n = 513). Две группы лечения были хорошо сбалансированы в отношении исходных характеристик и статуса заболевания. Поддерживающая терапия Мабтерой состояла из однократной инфузии Мабтеры в дозе 375 мг / м2 поверхности тела каждые 2 месяца до прогрессирования заболевания или на срок до 2 лет.
Через 25 месяцев после рандомизации поддерживающая терапия Мабтерой вызвала клинически значимое и статистически значимое улучшение оцениваемой исследователем первичной конечной точки выживаемости без прогрессирования (ВБП) по сравнению с наблюдением за пациентами с ранее нелеченной фолликулярной лимфомой. (таблица 5).
Значительное преимущество поддерживающего лечения Мабтерой также наблюдалось в отношении вторичных конечных точек: бессобытийная выживаемость (EFS), время до следующего лечения лимфомой (TNLT), время до следующей химиотерапии (TNCT) и общая частота ответа (ORR) (таблица 5). . Результаты первичного анализа были подтверждены более длительным периодом наблюдения (среднее время наблюдения: 48 месяцев и 73 месяца), и обновленные результаты были добавлены в Таблицу 5, чтобы проиллюстрировать сравнение между периодами наблюдения 25, 48 и 73 месяца.
Таблица 5 Поддерживающая фаза: сводка результатов эффективности Мабтеры по сравнению с наблюдение через 73 месяца среднего времени наблюдения (по сравнению с результатами первичного анализа, основанного на среднем времени наблюдения 25 месяцев, и обновленного анализа, основанного на среднем времени наблюдения 48 месяцев)
* По окончании обслуживания / наблюдения; # p-значения из теста хи-квадрат.
Основные значения соответствуют среднему сроку наблюдения 73 месяца, значения, выделенные курсивом в скобках, соответствуют 48 месяцам медианного времени наблюдения, а значения в скобках соответствуют среднему сроку наблюдения 25 месяцев (первичный анализ).
ВБП: выживаемость без прогрессирования заболевания; EFS: выживание без событий; ОС: общая выживаемость; TNLT: время до следующего курса лечения лимфомой; TNCT: время до следующего курса химиотерапии; ЧОО: общая частота ответа: НР: недоступность в момент клинического прекращения: ИЛИ: отношение шансов.
Поддерживающая терапия Мабтерой обеспечила стабильную пользу во всех протестированных подгруппах: пол (мужчины, женщины), возраст (= 60 лет), оценка FLIPI (= 3), индукционная терапия (R-CHOP, R-CVP или R-FCM) и независимо качества ответа на индукционную терапию (CR, CRu или PR). Исследовательский анализ преимуществ поддерживающего лечения показал менее выраженный эффект у пожилых пациентов (> 70 лет), однако размер выборки был небольшим.
Рецидивирующая / рефрактерная фолликулярная лимфома
В проспективном открытом международном многоцентровом исследовании III фазы 465 пациентов с рецидивирующей / резистентной фолликулярной лимфомой были рандомизированы на первом этапе для индукционной терапии CHOP (циклофосфамид, доксорубицин, винкристин и преднизолон; n = 231) или MabThera плюс CHOP (R-CHOP, n = 234). Две группы лечения были хорошо сбалансированы в отношении исходных характеристик и статуса заболевания. Всего 334 пациента, достигших полной или частичной ремиссии после индукционной терапии, были рандомизированы во вторую фазу поддерживающей терапии Мабтерой (n = 167) или наблюдения (n = 167). Поддерживающая терапия Мабтерой состояла из однократной инфузии Мабтеры в дозе 375 мг / м2 поверхности тела каждые 3 месяца до прогрессирования заболевания или в течение двух лет.
Окончательный анализ эффективности включал всех пациентов, рандомизированных в обе части исследования.После среднего времени наблюдения 31 месяц для пациентов, рандомизированных в фазу индукции, R-CHOP значительно улучшил прогноз пациентов с лимфомой. Фолликулярный рецидив / резистентность по сравнению с CHOP (см. Таблицу 6).
Таблица 6 Фаза индукции: список результатов эффективности CHOP по сравнению с R-CHOP (среднее время наблюдения 31 месяц).
1) Оценка была рассчитана с учетом относительного риска.
2) Последний ответ опухоли, оцененный исследователем. «Первичным» статистическим тестом для «ответа» был тест тенденции CR по сравнению с PR по сравнению с отсутствием ответа (p
Сокращения: нет данных; ORR: процент глобальных ответов; CR: полный ответ; PR: частичный ответ.
Для пациентов, рандомизированных на поддерживающую фазу исследования, среднее время наблюдения составило 28 месяцев от рандомизации до поддерживающей фазы. Поддерживающая терапия Мабтерой привела к клинически значимому и статистически значимому улучшению первичной конечной точки, ВБП (время от рандомизации для поддерживающей терапии до рецидива, прогрессирования заболевания или смерти) по сравнению с одним наблюдением (p
Таблица 7 Поддерживающая фаза: список результатов эффективности Мабтеры с учетом наблюдения (среднее время наблюдения 28 месяцев).
NR: не достигнуто; a: Применимо только к пациентам, достигшим полного ответа.
Польза поддерживающего лечения Мабтерой была подтверждена во всех проанализированных подгруппах, независимо от режима индукции (CHOP или R-CHOP) или качества ответа на индукционное лечение (CR или PR) (таблица 7). Поддерживающая терапия Мабтерой значительно увеличивала медианное значение ВБП у пациентов, ответивших на индукционную терапию СНОР (медиана ВБП 37,5 месяцев против 11,6 месяцев, p
Диффузная крупноклеточная неходжкинская лимфома
В рандомизированном открытом исследовании 399 ранее не леченных пожилых пациентов (в возрасте от 60 до 80 лет) с диффузной крупноклеточной В-клеточной лимфомой прошли стандартные курсы химиотерапии CHOP (циклофосфамид 750 мг / м2, доксорубицин 50 мг / м2, винкристин от 1,4 мг / м2 до максимум 2 мг в день 1, и преднизолон 40 мг / м2 / день в дни 1-5) каждые 3 недели в течение восьми циклов, или Мабтера 375 мг / м2 в сочетании с CHOP (R -НАРЕЗАТЬ).
Мабтера вводили в первый день лечебного цикла.
Окончательный анализ данных по эффективности включал всех рандомизированных пациентов (197 CHOP, 202 R-CHOP) и представлял среднюю продолжительность наблюдения, равную приблизительно 31 месяцу. Обе группы лечения были хорошо сбалансированы в отношении характеристик заболевания и статуса на исходном уровне. Окончательный анализ подтвердил, что лечение R-CHOP было связано с клинически значимым и статистически значимым улучшением продолжительности бессобытийной выживаемости (первичный параметр эффективности; событиями были смерть, рецидив или прогрессирование инфомы или переход на новый антидепрессант). -лимфомы) (p = 0,0001). Оценка Каплана-Мейера средней продолжительности бессобытийной выживаемости составила 35 месяцев в группе R-CHOP по сравнению с 13 месяцами в группе CHOP, что представляет снижение риска на 41%. Через 24 месяца общая оценка выживаемости составила 68,2% в группе R-CHOP по сравнению с 57,4% в группе CHOP. Последующий анализ общей продолжительности выживаемости, проведенный при средней продолжительности наблюдения 60 месяцев, подтвердил преимущество лечения R-CHOP над CHOP (p = 0,0071), что составляет снижение риска на 32%.
Анализ всех вторичных параметров (скорость ответа, выживаемость без прогрессирования, выживаемость без заболевания, продолжительность ответа) подтвердил эффективность лечения R-CHOP по сравнению с CHOP. Частота полного ответа после 8 циклов составила 76,2% в группе R-CHOP и 62,4% в группе CHOP (p = 0,0028). Риск прогрессирования заболевания снизился на 46%, а риск рецидива - на 51%.
Во всех подгруппах пациентов (пол, возраст, IPI с поправкой на возраст, стадия Анн-Арбора, ECOG, β2-микроглобулин, ЛДГ, альбумин, симптомы B, объемное заболевание, экстранодальные участки, поражение костного мозга) соотношения рисков выживаемость без событий и общая выживаемость (RCHOP по сравнению с CHOP) была менее 0,83 и 0,95 соответственно. R-CHOP был связан с улучшением прогноза как у пациентов с высоким, так и с низким риском в соответствии с IPI с поправкой на возраст.
Клинические лабораторные данные
Никаких ответов не наблюдалось у 67 пациентов, прошедших тест на человеческие антитела к мыши (HAMA). Из 356 пациентов, прошедших тест HACA, 1,1% (4 пациента) дали положительный результат.
Хронический лимфолейкоз
В двух рандомизированных открытых исследованиях в общей сложности 817 пациентов с ранее нелеченым ХЛЛ и 552 пациента с рецидивирующим / рефрактерным ХЛЛ были рандомизированы для получения химиотерапии CF (флударабин 25 мг / м2, циклофосфамид 250 мг / м2, дни 1-3) каждый раз. 4 недели по 6 циклов или Мабтера в сочетании с FC (R-FC). Мабтера вводили в дозе 375 мг / м2 в течение первого цикла, за день до химиотерапии и в дозе 500 мг / м2 в день 1 каждого последующего цикла лечения. Пациенты были исключены из исследования рецидивирующего / рефрактерного ХЛЛ, если они ранее лечились моноклональными антителами или были рефрактерными (определяемыми как неспособность достичь частичной ремиссии в течение как минимум 6 месяцев) к флударабину или любому аналогу нуклеозидов. Всего 810 пациентов (403 R-FC, 407 FC) для исследования первой линии (таблица 8a и таблица 8b) и 552 пациента (276 R-FC, 276 FC) для рецидивирующего / рефрактерного исследования (таблица 9). были проанализированы на эффективность.
В исследовании первой линии после среднего времени наблюдения 48,1 месяца медиана ВБП составила 55 месяцев в группе R-FC и 33 месяца в группе FC (p
Общий анализ выживаемости продемонстрировал значительное преимущество лечения RFC по сравнению с одной химиотерапией CF (p = 0,0319, лог-ранговый тест) (таблица 8a). Преимущество PFS постоянно наблюдалось в большинстве подгрупп пациентов, проанализированных в соответствии с исходным риском заболевания (в частности, стадии AC по Бине. ) (таблица 8b).
Таблица 8a Лечение первой линии хронического лимфолейкоза
Описание результатов эффективности Мабтеры плюс HR vs. Только ЧСС - среднее время наблюдения 48,1 месяца.
Процент ответов и процент CR, проанализированных в соответствии с тестом хи-квадрат. NR: не достигнуто; n.a .: не применимо.
*: Применимо только к пациентам, получившим CR, nPR, PR.
**: применимо только к пациентам, достигшим полного ответа.
Таблица 8b. Лечение первой линии хронического лимфолейкоза. Отношение рисков выживаемости без прогрессирования в зависимости от стадии Бине (ITT) - среднее время наблюдения 48,1 мес.
CI: доверительный интервал
В исследовании с рецидивом / рефрактерным лечением средняя выживаемость без прогрессирования (первичная конечная точка) составила 30,6 месяцев в группе R-FC и 20,6 месяцев в группе FC (p = 0,0002, логранговый тест).
Преимущество ВБП наблюдалось почти во всех подгруппах пациентов, проанализированных по исходному риску заболевания. Сообщалось о небольшом, но не значительном улучшении общей выживаемости в группе R-FC по сравнению с группой FC.
Таблица 9 Лечение рецидивирующего / рефрактерного хронического лимфоцитарного лейкоза - описание результатов эффективности Мабтеры плюс HR по сравнению с одним HR (среднее время наблюдения 25,3 месяца)
Процент ответов и процент CR, проанализированных в соответствии с тестом хи-квадрат.
*: применимо только к пациентам, получившим CR, nPR, PR; NR = не достигнуто; нет данных = не применимо.
**: применимо только к пациентам, достигшим полного ответа.
Также результаты других поддерживающих исследований с использованием Мабтеры в сочетании с другими схемами химиотерапии (включая CHOP, FCM, PC, PCM, бендамустин и кладрибин) для лечения ранее нелеченных и / или рецидивирующих пациентов с ХЛЛ / рефрактерными показали «высокий процент глобальных ответов с преимуществами в процентах от ВБП, хотя и с немного более высокой токсичностью (особенно миелотоксичностью). Эти исследования подтверждают возможность использования Мабтеры при любой химиотерапии.
Данные примерно 180 пациентов, предварительно получавших Мабтера, продемонстрировали клиническую пользу (включая полный ответ) и поддержку повторного лечения Мабтерой.
Педиатрическая популяция
Европейское агентство по лекарственным средствам отказалось от обязательства предоставлять результаты исследований с Мабтерой во всех подгруппах педиатрической популяции при фолликулярной лимфоме и хроническом лимфолейкозе. Информацию о педиатрическом применении см. В разделе 4.2.
Клинический опыт лечения ревматоидного артрита
Эффективность и безопасность Мабтеры в облегчении симптомов и признаков ревматоидного артрита у пациентов с неадекватным ответом на ингибиторы ФНО были продемонстрированы в базовом рандомизированном контролируемом двойном слепом многоцентровом исследовании (Исследование 1).
В исследовании 1 оценивали 517 пациентов с неадекватным ответом или непереносимостью одного или нескольких препаратов ингибиторов ФНО. У подходящих пациентов был «активный ревматоидный артрит, диагностированный в соответствии с критериями Американского колледжа ревматологии (ACR)». Мабтера вводили 2 в / в инфузии. разделенные интервалом в 15 дней. Пациенты получали 2 х 1000 мг внутривенных инфузий Мабтеры или плацебо в сочетании с метотрексатом. Все пациенты получали одновременно 60 мг преднизолона перорально на 2-7 дни и 30 мг на 8-14 дни после первой инфузии. Первичной конечной точкой была доля пациентов, достигших ответа ACR20 на 24-й неделе. Пациенты наблюдались дольше 24 недель для достижения долгосрочных целей, которые включали рентгенографическое обследование на 56-й и 104-й неделе. В течение этого периода «81% пациентов» из исходной группы плацебо получали Мабтеру между 24 и 56 неделями в рамках «открытого» исследования расширения протокола.
Исследования с применением Мабтеры у пациентов со стадийным артритом рано (пациенты, ранее не получавшие метотрексат, и пациенты с неадекватным ответом на метотрексат, но еще не получавшие ингибиторы TNF-альфа) достигли своих основных конечных точек. Мабтера не показана этим пациентам, поскольку данных о безопасности длительного лечения мабтерой недостаточно, особенно в отношении риска развития рака или ПМЛ.
Результаты активности болезни
Мабтера в сочетании с метотрексатом значительно увеличила долю пациентов, достигших не менее 20% улучшения ответа ACR по сравнению с пациентами, получавшими только метотрексат (таблица 10). Во всех основных исследованиях эффективность лечения была одинаковой у пациентов независимо от возраста, пола, площади поверхности тела, расы, количества предшествующих процедур или статуса заболевания.
Клинически и статистически значимые улучшения также наблюдались во всех отдельных компонентах ответа ACR (количество болезненных и опухших суставов, общая оценка пациента и врача, индекс инвалидности (HAQ), боль и С-реактивный белок (мг / дл)).
Таблица 10 Результаты клинического ответа в первичной конечной точке исследования 1 (ITT-популяция).
† Результат через 24 недели
Значительное отличие от плацебо + метотрексата и др. момент времени первичный: *** p ≤ 0,0001
У пациентов, получавших Мабтера в сочетании с метотрексатом, наблюдалось значительно большее снижение DAS28 (Оценка активности заболевания) по сравнению с пациентами, получавшими только метотрексат (таблица 9). Точно так же во всех исследованиях ответ EULAR (Европейская лига против ревматизма) от хорошего до среднего было достигнуто у значительно большего числа пациентов, получавших Мабтера и метотрексат, чем пациентов, получавших только метотрексат (Таблица 10).
Радиологический ответ
Структурное повреждение сустава было установлено рентгенологически и выражено как изменение модифицированной общей оценки остроты (mTSS) и ее компонентов, оценки эрозии и оценки сужения суставной щели.
В исследовании 1, проведенном с участием субъектов с неадекватным ответом или непереносимостью терапии одним или несколькими антагонистами ФНО, получавших Мабтеру в комбинации с метотрексатом, на 56 неделе у пациентов было значительно меньшее рентгенографическое прогрессирование, чем у тех, кто первоначально получал только метотрексат. Из пациентов, первоначально получавших только метотрексат, 81% получали Мабтеру в качестве терапии спасения между 16 и 24 неделями или в качестве продолжения исследования до 56 недели.
Кроме того, более высокий процент пациентов, получавших исходную терапию Мабтерой / метотрексатом, не показал прогрессирования эрозивных поражений в течение 56 недель (таблица 11).
Таблица 11 Радиологические результаты через 1 год (популяция mITT)
150 пациентов, первоначально рандомизированных в исследование 1 на группу плацебо + метотрексат, получали по крайней мере один курс лечения RTX + метотрексатом в течение одного года.
* п
Подавление скорости прогрессирования повреждения суставов также наблюдалось в течение длительного времени.Двухлетний рентгенографический анализ в исследовании 1 продемонстрировал значительное снижение прогрессирования структурных повреждений суставов у пациентов, получавших Мабтеру в комбинации с метотрексатом, по сравнению с пациентами, получавшими только метотрексат, а также значительно более высокий процент пациентов без прогрессирования суставов. повреждение свыше 2 лет.
Физические функции и качество жизни.
Значительное снижение индекса инвалидности (HAQ-DI) и астении (FACIT-Fatigue) наблюдалось у пациентов, получавших Мабтера, по сравнению с пациентами, получавшими только метотрексат. Доля пациентов, получавших Мабтера, у которых была клинически значимая минимальная разница (MCID) в HAQ-DI (определяемая как снижение индивидуального общего балла> 0,22), также была выше, чем у пациентов, получавших только метотрексат (таблица 12). .
Значительное улучшение здоровья с точки зрения качества жизни было продемонстрировано со значительным улучшением как оценки физического здоровья (PHS), так и оценки психического здоровья (MHS) по шкале SF-36. Более того, значительно более высокий процент пациентов достиг MCID по этим показателям (Таблица 12).
Таблица 12 Физические функции и качество жизни на 24-й неделе исследования 1
† Результаты на 24 неделе.
Значительная разница между плацебо и момент времени первичный: * p
MCID HAQ-DI ≥0,22, MCID SF-36 PHS> 5,42, MCID SF-36 MHS> 6,33.
Эффективность у серопозитивных пациентов с аутоантителами (РФ и / или анти-ЦЦП)
Серопозитивные пациенты с ревматоидным фактором (РФ) и / или циклическим пептидом цитруллинатом (анти-ЦЦП), которые лечились Мабтерой в комбинации с метотрексатом, показали лучший ответ, чем пациенты, отрицательные к обоим.
Результаты эффективности у пациентов, получавших MabThera, были проанализированы на основании статуса аутоантител до начала лечения. На 24-й неделе пациенты, которые были серопозитивными к RF и / или анти-CCPs на исходном уровне, имели значительно больший ответ по ACR20 и 50, чем у серонегативных. пациентов (p = 0,0312 и p = 0,0096) (таблица 13). Эти результаты были воспроизведены на 48 неделе, когда серопозитивность по аутоантителам значительно увеличивала вероятность достижения ACR70. На 48 неделе серопозитивные пациенты в 2-3 раза чаще достигают ответа ACR, чем серонегативные пациенты. Серопозитивные пациенты также имели значительно большее снижение DAS28. -ESR, чем у серонегативных пациентов.
Таблица 13 Сводная информация об эффективности на основе статуса аутоантител на исходном уровне
Значимые уровни были определены как * п
Долгосрочная эффективность при повторных курсах терапии
Лечение Мабтерой в сочетании с метотрексатом в течение нескольких циклов привело к значительному улучшению клинических признаков и симптомов ревматоидного артрита, о чем свидетельствуют ответы ACR, DAS28-VES и EULAR, которые были очевидны во всех исследованных популяциях. Наблюдались существенные улучшения. физическая функция, на которую указывают показатель HAQ-DI и процент пациентов, достигших MCID для HAQ-DI.
Результаты клинической лаборатории
В клинических исследованиях 392 из 3095 (12,7%) пациентов с ревматоидным артритом дали положительный результат на HACA после лечения Мабтерой. У большинства пациентов начало HACA не было связано с клиническим ухудшением или повышенным риском реакций на последующие инфузии. Наличие HACA может быть связано с ухудшением инфузионных или аллергических реакций после второй инфузии последующих курсов.
Педиатрическая популяция
Европейское агентство по лекарственным средствам отказалось от обязательства предоставлять результаты исследований с Мабтерой во всех подгруппах педиатрической популяции при аутоиммунном артрите. Информацию о педиатрическом применении см. В разделе 4.2.
Клинический опыт лечения гранулематоза с полиангиитом (Вегенера) и микроскопическим полиангиитом Всего 197 пациентов в возрасте 15 лет и старше с активным и тяжелым полиангиитом с полиангиитом (75%) и микроскопическим полиангиитом (24%) были включены в исследование и пролечены в многоцентровом рандомизированном исследовании. , двойное слепое, активное сравнительное исследование не меньшей эффективности.
Пациенты были рандомизированы в соотношении 1: 1 для приема перорального циклофосфамида ежедневно (2 мг / кг / день) в течение 3-6 месяцев или Мабтеры (375 мг / м2) один раз в неделю в течение 4 недель. Все пациенты в группе циклофосфамида получали поддерживающую терапию азатиоприном во время наблюдения. Пациенты в обеих группах получали 1000 мг метилпреднизолона внутривенно болюсно (или другую эквивалентную дозу глюкокортикоида) в день в течение 1-3 дней с последующим пероральным приемом преднизона (1 мг / кг / день, но не более 80 мг / день). Снижение преднизона было завершено в течение 6 месяцев после начала исследуемого лечения. Первичной конечной точкой было достижение полной ремиссии через 6 месяцев, определяемой как Активность Бирмингемского васкулита для гранулематоза Вегенера (BVAS / WG) 0 и отсутствие терапии глюкокортикоидами. Маржа не меньшей эффективности по умолчанию для разницы между видами лечения составляла 20%. Исследование продемонстрировало не меньшую эффективность Мабтеры перед циклофосфамидом в отношении полной ремиссии (ПР) через 6 месяцев (таблица 14). Эффективность наблюдалась как у вновь диагностированных пациентов, так и у пациентов с рецидивирующим заболеванием (таблица 15).
Таблица 14 Процент пациентов, достигших полной ремиссии через 6 месяцев (группа, собирающаяся лечиться *)
Таблица 15 Полная ремиссия через 6 месяцев в зависимости от статуса заболевания
К пациентам с отсутствующими данными применяется наихудший случай.
Полная ремиссия через 12 и 18 месяцев
В группе Мабтеры 48% пациентов достигли полного ответа через 12 месяцев, а 39% пациентов достигли полного результата через 18 месяцев. У пациентов, получавших циклофосфамид (с последующим приемом азатиоприна для поддержания полной ремиссии), 39% пациентов достигли полной ремиссии через 12 месяцев, а 33% пациентов достигли полной ремиссии через 18 месяцев. С 12 по 18 месяц в группе Мабтеры наблюдалось 8 рецидивов по сравнению с 4 в группе циклофосфамида.
Повторное лечение с Мабтерой
Согласно заключению исследователя, 15 пациентов прошли второй курс терапии Мабтерой для лечения рецидива активности заболевания, который произошел между 6 и 18 месяцами после первого курса Мабтеры. Ограниченные данные текущего исследования не позволяют делать какие-либо выводы относительно эффективности последующие курсы Мабтеры у пациентов с гранулематозом с полиангиитом и микроскопическим полиангиитом.
Непрерывная иммуносупрессивная терапия может быть особенно целесообразной у пациентов с риском рецидива (например, с историей предыдущих рецидивов и гранулематоза с полиангиитом, или у пациентов с восстановлением B-клеток в дополнение к PR3-ANCA во время мониторинга). После достижения ремиссии с помощью Мабтеры можно рассмотреть возможность продолжения иммуносупрессивной терапии для предотвращения рецидива. Эффективность и безопасность Мабтеры в поддерживающей терапии не установлены.
Лабораторные тесты
В общей сложности 23/99 (23%) пациентов, получавших Мабтеру в исследовании, дали положительный результат на HACA в течение 18 месяцев. Ни у одного из 99 пациентов, получавших MabThera, при скрининге не было обнаружено HACA. Клиническое значение развития НАСА у пациентов, получавших Мабтера, неясно.
05.2 «Фармакокинетические свойства.
Неходжкинской лимфомы
На основании «популяционного фармакокинетического анализа 298 пациентов с НХЛ, которые получали» однократную или многократную инфузию Мабтеры в качестве одного агента или в сочетании с терапией СНОР (используемые дозы Мабтеры в диапазоне от 100 до 500 мг / м2), типичные оценки населения для неспецифический клиренс (CL1), специфический клиренс (CL2) с вероятным вкладом В-клеток или опухолевой массы и объем распределения в центральном отделении (V1) составляли 0,14 л / день, 0,59 л / день и 2,7 л соответственно. Среднее предполагаемое конечное время полувыведения Мабтеры составляло 22 дня (диапазон: 6,1 - 52 дня). Исходное количество CD19-положительных клеток и диаметр поддающихся измерению опухолевых очагов частично способствовали изменчивости CL2 Мабтеры, как видно из данных 161. пациенты, которые принимали 375 мг / м2 в качестве внутривенной инфузии в течение 4 еженедельных доз. Пациенты с более высоким числом CD19-положительных клеток или более крупными опухолевыми поражениями имели более высокий уровень CL2. Однако значительный компонент межиндивидуальной вариабельности оставался для CL2 после коррекции на CD19. -положительное количество клеток и диаметр очага опухоли. V1 варьировался в зависимости от площади поверхности тела (Площадь поверхности тела, BSA) и терапии CHOP. Эта вариабельность V1 (27,1% и 19,0%), определяемая диапазоном BSA (1,53–2,32 м2) и сопутствующей терапией CHOP, соответственно, была относительно небольшой. Возраст, пол и эффективность Статус ВОЗ не повлиял на фармакокинетику Мабтеры. Анализ показывает, что корректировка дозы Мабтеры с учетом любой из оцененных ковариат вряд ли приведет к значительному снижению ее фармакокинетической изменчивости.
Мабтера, вводимая в виде внутривенной инфузии в дозе 375 мг / м2 с недельными интервалами для 4 доз 203 пациентам с НХЛ, ранее не получавшим Мабтеру, приводила к средней Cmax после четвертой инфузии 486 мкг / мл (диапазон: 77,5-996, 6 мкг / мл). Ритуксимаб обнаруживался в сыворотке крови пациента через 3-6 месяцев после завершения последнего курса лечения.
После введения Мабтеры в дозе 375 мг / м2 в / в. с недельными интервалами для 8 доз 37 пациентам с НХЛ средний C увеличивался с каждой последующей инфузией, в диапазоне от 243 мкг / мл (диапазон: 16-582 мкг / мл) после первой инфузии до 550 мкг / мл (диапазон: 171 - 1177 мкг / мл) после восьмой инфузии.
Фармакокинетический профиль Мабтеры при введении в виде 6 инфузий по 375 мг / м2 в сочетании с 6 циклами химиотерапии CHOP был аналогичен таковому, наблюдаемому при использовании только Мабтеры.
Хронический лимфолейкоз
Мабтера вводили внутривенно с дозой 375 мг / м2 в первом цикле, увеличивая ее до 500 мг / м2 для каждого последующего цикла, из расчета 5 доз в комбинации с флударабином и циклофосфамидом пациентам с ХЛЛ. Средняя Cmax (N = 15) после пятой инфузии 500 мг / м2 составляла 408 мкг / мл (диапазон 97-764 мкг / мл), а средний конечный период полувыведения составлял 32 дня (диапазон 14-62 дня).
Ревматоидный артрит
После двух внутривенных инфузий Мабтеры в дозе 1000 мг с интервалом в две недели средний конечный период полувыведения составил 20,8 дня (диапазон от 8,58 до 35,9 дня), средний системный клиренс составил 0,23 л / день (диапазон от 0,091 до 0,67 л / сут). день), а средний стационарный объем распределения составлял 4,6 л (диапазон от 1,7 до 7,51 л). Популяция тех же данных дала аналогичные средние значения для системного клиренса и периода полувыведения, 0,26 л / день и 20,4 дня, соответственно. Популяционный фармакокинетический анализ показал, что ППТ и пол были наиболее значимыми ковариантами для объяснения индивидуальной вариабельности фармакокинетических параметров. После корректировки на BSA у субъектов мужского пола был больший объем распределения и более быстрое очищение, чем у субъектов женского пола. Фармакокинетические различия, связанные с полом, не считались клинически значимыми, и корректировка дозировки не требовалась. Фармакокинетические данные у пациентов с почечной или печеночной недостаточностью отсутствуют.
Фармакокинетика ритуксимаба оценивалась после двух внутривенных (внутривенных) доз 500 мг и 1000 мг в дни 1 и 15 в четырех исследованиях. Во всех этих исследованиях фармакокинетика ритуксимаба была пропорциональна дозе в пределах изученного ограниченного диапазона дозировок.Средняя сывороточная Cmax ритуксимаба после первой инфузии составляла от 157 до 171 мкг / мл для дозы 2 x 500 мг и между 298 и 298 и 298 мкг / мл. 341 мкг / мл для дозы 2 x 1000 мг. После второй инфузии среднее значение Cmax составляло от 183 до 198 мкг / мл для дозы 2 x 500 мг и от 355 до 404 мкг / мл для дозы 2 x 1000 мг. Средний период полувыведения составил от 15 до 16 дней для дозы 2 x 500 мг и от 17 до 21 дня для дозы 2 x 1000 мг. Cmax была на 16-19% выше после второй инфузии по сравнению с первая настойка для обеих дозировок.
Фармакокинетику ритуксимаба оценивали после двух в / в. 500 мг и 1000 мг после обработки во втором цикле. Средняя Cmax ритуксимаба в сыворотке крови после первой инфузии составляла от 170 до 175 мкг / мл для дозы 2 x 500 мг и от 317 до 370 мкг / мл для дозы 2 x 1000 мг.После второй инфузии среднее значение Cmax составляло 207 мкг / мл для дозы 2 x 500 мг и от 377 до 386 мкг / мл для дозы 2 x 1000 мг. Средний конечный период полувыведения после второй инфузии, после второго цикла, составлял 19 дней для дозы 2 х 500 мг и от 21 до 22 дней для дозы 2 х 1000 мг. Фармакокинетические параметры ритуксимаба были сопоставимы в течение двух курсов лечения.
Фармакокинетические параметры в популяции субъектов с неадекватным ответом на антитела к TNF, подвергнутых одинаковому режиму дозирования (2 x 1000 мг внутривенно, с интервалом 2 недели), были аналогичными со средней максимальной концентрацией в сыворотке 369 мкг / мл и половиной - срок службы "средний терминал 19,2 дня.
Гранулематоз с полиангиитом и микроскопическим полиангиитом
На основании популяционного фармакокинетического анализа данных 97 пациентов с гранулематозом с полиангиитом и микроскопическим полиангиитом, получавших 375 мг / м2 Мабтеры один раз в неделю в течение четырех недель, средний расчетный период полувыведения составил 23 дня (диапазон от 9 до 49 дней). . Средний клиренс и объем распределения ритуксимаба составляли 0,313 л / день (диапазон от 0,116 до 0,726 л / день) и 4,50 л (диапазон от 2,25 до 7,39 л), соответственно. Фармакокинетические параметры ритуксимаба у этих пациентов похожи на параметры, наблюдаемые у пациентов с ревматоидным артритом.
05.3 Доклинические данные по безопасности
Было показано, что ритуксимаб обладает высокой специфичностью в отношении антигена CD20 на В-клетках. Исследования токсичности на обезьянах циномолгус они не выявили никаких других эффектов, кроме ожидаемого фармакологического истощения В-клеток в периферической крови и ткани лимфатических узлов.
Исследования эволюционной токсичности проводились на обезьянах. циномолгус с дозами до 100 мг / кг (лечение на 20-50 дни гестации) и показали отсутствие доказательств токсичности ритуксимаба для плода. Однако в лимфоидных органах плода наблюдалось дозозависимое истощение В-клеток. фармакология, которая сохранялась до момента рождения и была связана со снижением уровня IgG у пораженных новорожденных животных. Количество В-клеток нормализовалось у этих животных в течение 6 месяцев после рождения и не повлияло на реакцию иммунизации.
Стандартные тесты на мутагенность не проводились, так как эти тесты не имеют отношения к этой молекуле. Долгосрочные исследования на животных для определения канцерогенного потенциала ритуксимаба не проводились. Специальных исследований для определения влияния ритуксимаба на фертильность не проводилось. Обычно в исследованиях токсичности на обезьянах циномолгус не наблюдалось вредного воздействия на мужские или женские репродуктивные органы.
06.0 ФАРМАЦЕВТИЧЕСКАЯ ИНФОРМАЦИЯ
06.1 Вспомогательные вещества
Цитрат натрия
Полисорбат 80
Натрия хлорид
Гидроксид натрия
Соляная кислота
Вода для инъекций
06.2 Несовместимость
Несовместимости между Мабтерой и поливинилхлоридом, полиэтиленовыми пакетами или инфузионным оборудованием не наблюдалось.
06.3 Срок действия
30 месяцев
Приготовленный для инфузии раствор Мабтеры физически и химически стабилен в течение 24 часов при температуре от 2 ° C до 8 ° C, а затем в течение 12 часов при комнатной температуре.
С микробиологической точки зрения приготовленный раствор для инфузий следует использовать немедленно. Если не использовать немедленно, время и условия хранения перед использованием являются обязанностью пользователя и обычно не превышаются. 24 часа при температуре от 2 ° C до 8 ° C, если разбавление не проводилось в контролируемых и утвержденных асептических условиях.
06.4 Особые меры предосторожности при хранении
Хранить в холодильнике (2-8 ° C). Храните контейнер во внешней упаковке, чтобы защитить его от света.
Условия хранения после разведения лекарственного средства см. В разделе 6.3.
06.5 Характер непосредственной упаковки и содержимого упаковки
Флаконы из прозрачного стекла типа I с бутилкаучуковой пробкой, содержащие 500 мг ритуксимаба в 50 мл. В пачках по 1 флакону.
06.6 Инструкции по эксплуатации и обращению
Мабтера поставляется в стерильных, не содержащих консервантов, апирогенных флаконах для одноразового использования.
Аспирируйте в стерильных условиях необходимое количество Мабтеры и разведите ритуксимаб до расчетной концентрации от 1 до 4 мг / мл в инфузионный пакет, содержащий стерильный апирогенный раствор хлорида натрия 9 мг / мл (0,9%) для инъекций. ) или 5% D-глюкозы в воде. Чтобы перемешать раствор, медленно переверните пакет, чтобы не допустить вспенивания. Необходимо следить за стерильностью приготовленных растворов. Поскольку лекарственный препарат не содержит противомикробных консервантов или бактериостатических агентов, следует соблюдать асептические методы.
Перед введением лекарственные средства для парентерального введения следует визуально проверить на наличие частиц или обесцвечивания.
Неиспользованные лекарства и отходы, полученные из этого лекарства, необходимо утилизировать в соответствии с местными правилами.
07.0 ДЕРЖАТЕЛЬ РАЗРЕШЕНИЯ НА МАРКЕТИНГ
Roche Registration Limited
6 Соколиный путь
Shire Park
Welwyn Garden City
AL7 1TW
Соединенное Королевство
08.0 НОМЕР РАЗРЕШЕНИЯ НА МАРКЕТИНГ
EU / 1/98/067/002
033315021
09.0 ДАТА ПЕРВОГО РАЗРЕШЕНИЯ ИЛИ ПРОДЛЕНИЯ РАЗРЕШЕНИЯ
Дата первого разрешения: 2 июня 1998 г.
Дата последнего обновления: 2 июня 2008 г.
10.0 ДАТА ПЕРЕСМОТРА ТЕКСТА
11.0 ДЛЯ РАДИОПРЕПАРАТОВ - ПОЛНЫЕ ДАННЫЕ ПО ДОЗИМЕТРИИ ВНУТРЕННЕГО ИЗЛУЧЕНИЯ
12.0 ДЛЯ РАДИОПРЕПАРАТОВ, ДОПОЛНИТЕЛЬНЫЕ ПОДРОБНЫЕ ИНСТРУКЦИИ ПО ЧРЕЗВЫЧАЙНОЙ ПОДГОТОВКЕ И КОНТРОЛЮ КАЧЕСТВА