Активные ингредиенты: Фебуксостат.
АДЕНУРИК 80 мг таблетки, покрытые пленочной оболочкой
АДЕНУРИК 120 мг таблетки, покрытые пленочной оболочкой
Почему используется аденурик? Для чего это?
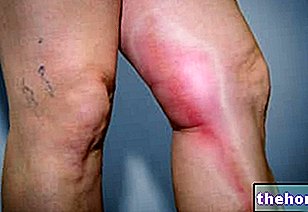
Таблетки АДЕНУРИК содержат активное вещество фебуксостат и используются для лечения подагры - заболевания, связанного с повышенным содержанием мочевой кислоты (уратов) в организме. У некоторых людей количество мочевой кислоты, которая накапливается в крови, может стать слишком большим. остаются в растворе. В этом случае кристаллы уратов могут образовываться внутри и вокруг суставов и почек. Эти кристаллы могут вызвать внезапную сильную боль, покраснение, тепло и отек в суставе (приступ подагры). Если не лечить, в суставах и вокруг них могут образовываться более крупные отложения, называемые тофусами. Tophi может повредить суставы и кости.
АДЕНУРИК работает за счет снижения уровня мочевой кислоты. Поддержание низкого уровня мочевой кислоты за счет приема АДЕНУРИКА один раз в день предотвращает накопление кристаллов и со временем уменьшает симптомы. Если уровень мочевой кислоты сохраняется на низком уровне в течение достаточно длительного времени, тофусы также могут реабсорбироваться.
Таблетки АДЕНУРИК 120 мг также используются для лечения и профилактики повышенного уровня мочевой кислоты в крови, который может возникнуть в случае химиотерапии рака крови. Раковые клетки разрушаются во время химиотерапевтического лечения, и уровень мочевой кислоты в крови повышается, если невозможно предотвратить образование этой кислоты.
АДЕНУРИК предназначен для взрослых.
Противопоказания Когда не следует применять аденурик
Не принимайте АДЕНУРИК:
- Если у вас аллергия на фебуксостат или любой другой ингредиент этого лекарства
Меры предосторожности при использовании Что следует знать перед приемом аденурика
Перед приемом АДЕНУРИКА проконсультируйтесь с врачом:
- Если у вас есть или вы страдали от сердечной недостаточности или других проблем с сердцем
- Если у вас есть или были заболевание почек и / или тяжелые аллергические реакции на аллопуринол (лекарство, используемое для лечения подагры)
- Если у вас есть или были заболевания печени или отклонения в тестах функции печени
- Если у вас повышенный уровень мочевой кислоты из-за синдрома Леша-Найхана (редкое наследственное заболевание, при котором в крови слишком много мочевой кислоты)
- Если у вас есть проблемы с щитовидной железой.
При возникновении аллергических реакций на АДЕНУРИК прекратите прием лекарства. Возможными симптомами аллергических реакций могут быть:
- сыпь, включая тяжелые формы (например, волдыри, шишки, зудящая сыпь, эксфолиативная сыпь), зуд
- отек конечностей или лица
- затруднение дыхания
- лихорадка с увеличенными лимфатическими узлами
- но также и тяжелые, опасные для жизни аллергические состояния с остановкой сердца и кровообращения.
Ваш врач может решить навсегда прекратить лечение аденурии.
Сообщалось о редких, опасных для жизни кожных высыпаниях (синдром Стивенса-Джонсона) при применении АДЕНУРИКА; первоначально они появлялись на туловище в виде красноватых пятен или круглых пятен, часто с центральными волдырями. Они также могут включать язвы. Во рту, горле и т. Д. нос, половые органы и конъюнктивит (красные и опухшие глаза). Сыпь может прогрессировать до обширных пузырей или шелушения кожи.
Если у вас развился синдром Стивенса-Джонсона на фоне приема фебуксостата, лечение АДЕНУРИКОМ больше не следует начинать. Если у вас появилась сыпь или эти кожные симптомы, немедленно обратитесь к врачу и сообщите ему, что вы лечитесь этим лекарством. .
Если у вас в настоящее время приступ подагры (внезапное появление сильной боли, болезненности, покраснения, тепла и отека одного сустава), дождитесь прекращения приступа подагры, прежде чем начинать терапию АДЕНУРИКОМ.
У некоторых людей приступы подагры могут обостриться в начале определенных методов лечения, используемых для контроля уровня мочевой кислоты. Не все люди испытывают обострения, но вы также можете испытать обострение при приеме АДЕНУРИКА, особенно в течение первых нескольких недель или месяцев терапии. Важно, чтобы вы продолжали принимать АДЕНУРИК даже в случае обострения, поскольку АДЕНУРИК продолжает снижать уровень мочевой кислоты. Если вы продолжите принимать АДЕНУРИК каждый день, со временем обострения будут происходить реже и будут становиться все менее и менее болезненными.
При необходимости врач часто прописывает другие лекарства, чтобы предотвратить или лечить симптомы обострения (например, боль и отек в суставе).
У пациентов с очень высоким уровнем уратов (например, пациентов, получающих химиотерапию), лечение препаратами, снижающими уровень мочевой кислоты, может вызвать накопление ксантина в мочевыводящих путях с возможным камнеобразованием, хотя этого не наблюдалось. У пациентов, получавших АДЕНУРИК от опухолей Синдром лизиса.
Ваш врач может назначить анализы крови, чтобы убедиться, что ваша печень функционирует нормально.
Дети и подростки
Не давайте это лекарство детям младше 18 лет, поскольку безопасность и эффективность не установлены.
Взаимодействия Какие лекарства или продукты могут изменить действие аденурика?
Сообщите своему врачу или фармацевту, если вы принимаете, недавно принимали или собираетесь принимать любые другие лекарства, даже те, которые получены без рецепта.
Очень важно, чтобы вы сообщили своему врачу или фармацевту, если вы принимаете лекарство, содержащее любое из следующих веществ, поскольку они могут взаимодействовать с АДЕНУРИКОМ, и ваш врач может принять соответствующие меры:
- Меркаптопурин (используется для лечения рака)
- Азатиоприн (используется для снижения иммунного ответа)
- Теофиллин (используется для лечения астмы)
Предупреждения Важно знать, что:
Беременность и кормление грудью
Неизвестно, может ли АДЕНУРИК нанести вред нерожденному ребенку. АДЕНУРИК не следует применять во время беременности. Неизвестно, попадает ли АДЕНУРИК в грудное молоко. Вы не должны принимать АДЕНУРИК, если кормите грудью или намереваетесь это сделать.
Если вы беременны или кормите грудью, подозреваете, что беременны или планируете беременность, перед приемом этого лекарства проконсультируйтесь с врачом или фармацевтом.
Вождение и использование машин
Имейте в виду, что во время лечения вы можете почувствовать головокружение, сонливость, помутнение зрения, онемение или покалывание, и при появлении этих симптомов вам не следует водить машину или работать с механизмами.
АДЕНУРИК содержит лактозу
Таблетки ADENURIC содержат лактозу (разновидность сахара). Если вы знаете, что у вас непереносимость некоторых сахаров, проконсультируйтесь с врачом, прежде чем принимать это лекарство.
Доза, способ и время приема Как применять аденурик: дозировка
Всегда принимайте это лекарство точно так, как вам сказал врач. Если вы не уверены, вам следует проконсультироваться с врачом или фармацевтом.
- Обычная доза - одна таблетка в день. На обратной стороне полоски показаны дни недели, чтобы помочь вам проверить, принимали ли вы свою дозу каждый день.
- Таблетки необходимо принимать внутрь. Вы можете брать их рядом с едой или вдали от нее.
Хроническая гиперурикемия с отложением уратов АДЕНУРИК выпускается в таблетках по 80 или 120 мг. Ваш врач назначит вам наиболее подходящую дозировку.
Продолжайте принимать АДЕНУРИК каждый день, даже если у вас нет обострения или приступа подагры.
Профилактика и лечение повышенного уровня мочевой кислоты у пациентов, проходящих химиотерапию. АДЕНУРИК выпускается в виде таблеток по 120 мг.
Начните принимать АДЕНУРИК за два дня до химиотерапии и продолжайте принимать его в соответствии с рекомендациями врача. Использование обычно недолговечно.
Передозировка Что делать, если вы приняли слишком много аденурика
Если вы приняли больше АДЕНУРИКА, чем предусмотрено
В случае случайной передозировки спросите своего врача, что делать, или обратитесь в ближайшее отделение неотложной помощи.
Если вы забыли принять АДЕНУРИК
Если вы забыли принять дозу АДЕНУРИКА, примите ее, как только заметите это, если только не пришло время для следующей дозы. В этом случае пропустите пропущенную дозу и примите следующую дозу в назначенное время. Не принимайте двойную дозу, чтобы восполнить пропущенную дозу.
Если вы перестанете принимать АДЕНУРИК
Не прекращайте прием АДЕНУРИКА без согласия врача, даже если вы чувствуете себя лучше. Если вы прекратите принимать АДЕНУРИК, уровень мочевой кислоты может начать повышаться, а симптомы могут ухудшиться из-за образования новых кристаллов уратов в суставах и почках и вокруг них.
Если у вас есть дополнительные вопросы по применению этого лекарства, обратитесь к врачу или фармацевту.
Побочные эффекты Каковы побочные эффекты аденурика?
Как и все лекарства, это лекарство может вызывать побочные эффекты, хотя они возникают не у всех.
Прекратите принимать лекарство и немедленно обратитесь к врачу или обратитесь в ближайшее отделение неотложной помощи, если у вас возникнут следующие редкие побочные эффекты (им может быть подвержено до 1 человека из 1000), поскольку может последовать серьезная аллергическая реакция:
- анафилактические реакции, гиперчувствительность к лекарствам (см. также раздел «Предупреждения и меры предосторожности»)
- Опасные для жизни кожные высыпания, характеризующиеся образованием пузырей и шелушением кожи и внутренних поверхностей полости тела, например. во рту и гениталиях, болезненные язвы во рту и / или на половых органах, сопровождающиеся лихорадкой, болью в горле и усталостью (синдром Стивенса-Джонсона / токсический эпидермальный некролиз) или увеличенными лимфатическими узлами, увеличенной печенью, гепатитом (вплоть до печеночной недостаточности), повышенное количество лейкоцитов (лекарственная реакция с эозинофилией и системными симптомами - ПЛАТЬЕ).
- генерализованная сыпь
Общие побочные эффекты (им могут быть подвержены до 1 человека из 10):
- отклонения в результатах тестов функции печени
- понос
- Головная боль
- сыпь (включая различные типы кожной сыпи, см. ниже в разделах «необычные» и «редкие»)
- тошнота
- усиление симптомов подагры
- локализованный отек из-за задержки жидкости в тканях (отек)
Другие побочные эффекты, не упомянутые выше, перечислены ниже.
Необычные побочные эффекты (им могут быть подвержены до 1 человека из 100):
- снижение аппетита, изменение уровня сахара в крови (диабет), симптомом которого может быть чрезмерная жажда, повышенный уровень жира в крови, увеличение веса
- потеря либидо (сексуальное желание)
- проблемы со сном, сонливость
- головокружение, онемение, покалывание, снижение или изменение тактильных ощущений (гипестезия, гемипарез или парестезия), изменение вкуса (дисгевзия), снижение обоняния (гипосмия)
- отклонения от нормы ЭКГ, нерегулярное или учащенное сердцебиение, восприятие сердцебиения (сердцебиение)
- покраснение или покраснение (например, покраснение лица или шеи), повышение артериального давления, кровотечение (кровотечение, наблюдаемое только у пациентов, проходящих химиотерапию по поводу заболеваний крови)
- кашель, одышка, боль в груди, воспаление носового прохода и / или горла (инфекция дыхательных путей), бронхит
- сухость во рту, боль или дискомфорт в животе, избыток газов, изжога / несварение желудка, запор, более частые испражнения, рвота, дискомфорт в желудке
- зуд, крапивница, воспаление кожи, изменение цвета кожи, маленькие красные или пурпурные пятна на коже, маленькие плоские красные пятна на коже, красные участки на коже, покрытые небольшими сливными шишками, сыпь, участки покраснения и пятна на кожа, другие кожные заболевания
- мышечные спазмы, мышечная слабость, боль в мышцах или суставах, бурсит или артрит (воспаление суставов, обычно сопровождающееся болью, отеком и / или скованностью), боль в конечностях, боль в спине, мышечные спазмы
- кровь в моче, учащенное мочеиспускание, аномальные результаты анализа мочи (повышенный уровень белка в моче) снижение способности почек функционировать должным образом
- усталость, боль в груди, дискомфорт в груди
- камни в желчном пузыре или желчном протоке (желчнокаменная болезнь)
- повышенный уровень тиреотропного гормона (ТТГ) в крови
- изменения в биохимических анализах крови или количестве эритроцитов или тромбоцитов (изменения в результатах анализа крови)
- камни в почках
- трудности с эрекцией
Редкие побочные эффекты (им могут быть подвержены до 1 человека из 1000):
- повреждение мышц, состояние, которое в редких случаях может быть серьезным. Могут развиться мышечные проблемы, и, в частности, если вы одновременно чувствуете недомогание или у вас высокая температура, это может быть результатом аномального разрушения мышечных клеток. Немедленно обратитесь к врачу, если вы испытываете мышечную боль, нежность или слабость.
- заметный отек более глубоких слоев кожи, особенно вокруг губ, глаз, гениталий, рук, ног или языка, с возможным внезапным затруднением дыхания
- высокая температура, связанная с кожной сыпью, похожей на корь, увеличенные лимфатические узлы, увеличенная печень, гепатит (вплоть до печеночной недостаточности), повышенное количество лейкоцитов (лейкоцитоз, связанный или не связанный с эозинофилией)
- покраснение кожи (эритема), сыпь различного типа (например, зуд, белые пятна, волдыри, гнойные пузыри, шелушение кожи, корь, похожая на сыпь), диффузная эритема, некроз и образование пузырей на эпидермисе и слизистых оболочках , что приводит к отшелушиванию и возможному сепсису (синдром Стивенса-Джонсона / токсический эпидермальный некролиз)
- нервозность
- жажда
- звон в ушах
- помутнение зрения, изменение зрения
- выпадение волос
- щечная язва
- воспаление поджелудочной железы: частыми симптомами являются боли в животе, тошнота и рвота.
- повышенное потоотделение
- снижение веса, повышение аппетита, неконтролируемая потеря аппетита (анорексия)
- жесткость мышц и / или суставов
- аномально низкий уровень клеток крови (лейкоцитов или эритроцитов или тромбоцитов)
- позыв к мочеиспусканию
- изменения или уменьшение количества мочи из-за воспаления почек (тубулоинтерстициальный нефрит)
- воспаление печени (гепатит)
- пожелтение кожи (желтуха)
- повреждение печени
Если вы заметили какие-либо побочные эффекты, обратитесь к врачу или фармацевту, включая любые возможные побочные эффекты, не указанные в данном информационном листке.
Сообщение о побочных эффектах
Если вы заметили какие-либо побочные эффекты, обратитесь к врачу или фармацевту, включая любые возможные побочные эффекты, не указанные в данном информационном листке. Вы также можете сообщить о побочных эффектах напрямую через национальную систему отчетности, указанную в Приложении V. Сообщая о побочных эффектах, вы можете помочь получить больше информации о безопасности этого лекарства.
Срок действия и удержание
Храните это лекарство в недоступном для детей месте.
- Не используйте лекарство после истечения срока годности, указанного на упаковке и на фольге блистера с таблетками после «EXP». Срок годности относится к последнему дню месяца.
- Это лекарство не требует особых условий хранения.
Не выбрасывайте лекарства в сточные воды или бытовые отходы. Спросите своего фармацевта, как утилизировать лекарства, которые вы больше не используете. Это поможет защитить окружающую среду.
Что содержит АДЕНУРИК
Действующее вещество - фебуксостат.
Каждая таблетка содержит 80 или 120 мг фебуксостата.
Вспомогательные вещества:
Ядро планшета: моногидрат лактозы, микрокристаллическая целлюлоза, стеарат магния, гидроксипропилцеллюлоза, кроскармеллоза натрия, коллоидный гидрат кремнезема.
Покрытие таблеток: Opadry II желтый, 85F42129, содержащий: поливиниловый спирт, диоксид титана (E171), макрогол типа 3350, тальк, оксид железа желтый (E172).
Как выглядит АДЕНУРИК и что содержится в упаковке
Таблетки ADENURIC, покрытые пленочной оболочкой, имеют бледно-желто-желтый цвет и имеют форму капсулы.Таблетки, покрытые пленочной оболочкой 80 мг, имеют отметку «80» на одной стороне. Таблетки 120 мг, покрытые пленочной оболочкой, имеют отметку «120» на одной стороне.
АДЕНУРИК 80 мг и 120 мг упакован в прозрачный блистер (Аклар / ПВХ / Алюминий), содержащий 14 таблеток.
АДЕНУРИК 80 мг и 120 мг доступен в упаковках по 14, 28, 42, 56, 84 и 98 таблеток, покрытых пленочной оболочкой.
Не все размеры упаковки могут быть проданы.
Листовка с исходным кодом: AIFA (Итальянское агентство по лекарственным средствам). Контент опубликован в январе 2016 года. Представленная информация может быть устаревшей.
Чтобы иметь доступ к самой последней версии, рекомендуется зайти на сайт AIFA (Итальянское агентство по лекарственным средствам). Заявление об ограничении ответственности и полезная информация.
01.0 НАИМЕНОВАНИЕ ЛЕКАРСТВЕННОГО ПРЕПАРАТА
ADENURIC 80 MG ТАБЛЕТКИ, ПОКРЫТЫЕ ПЛЕНКОЙ
02.0 КАЧЕСТВЕННЫЙ И КОЛИЧЕСТВЕННЫЙ СОСТАВ
Каждая таблетка содержит 80 мг фебуксостата.
Вспомогательные вещества с известными эффектами:
Каждая таблетка содержит 76,50 мг лактозы (в виде моногидрата).
Полный список вспомогательных веществ см. В разделе 6.1.
03.0 ФАРМАЦЕВТИЧЕСКАЯ ФОРМА
Таблетка (таблетка), покрытая пленочной оболочкой.
Таблетки светло-желтого / желтого цвета, покрытые оболочкой, капсулы с тиснением "80" на одной стороне.
04.0 КЛИНИЧЕСКАЯ ИНФОРМАЦИЯ
04.1 Терапевтические показания
Лечение хронической гиперурикемии с отложением уратов (включая анамнез или наличие тофусов и / или подагрического артрита).
АДЕНУРИК показан у взрослых.
04.2 Дозировка и способ применения
Дозировка
Рекомендуемая пероральная доза АДЕНУРИКА составляет 80 мг один раз в день, и ее можно принимать как во время еды, так и вне ее. быть на рассмотрении.
ADENURIC действует достаточно быстро, чтобы позволить новое определение мочевой кислоты в сыворотке крови через 2 недели.Терапевтическая цель - снизить и поддерживать уровень мочевой кислоты в сыворотке ниже 6 мг / дл (357 мкмоль / л).
Для профилактики обострений подагры рекомендуется период лечения не менее 6 месяцев (см. Раздел 4.4).
Пожилые люди
У пожилых людей коррекция дозы не требуется (см. Раздел 5.2).
Почечная недостаточность
Эффективность и безопасность лекарственного препарата у пациентов с тяжелой почечной недостаточностью полностью не установлены (клиренс креатинина).
У пациентов с почечной недостаточностью легкой или средней степени тяжести коррекции дозы не требуется.
Печеночная недостаточность
Эффективность и безопасность фебуксостата не изучались у пациентов с тяжелой печеночной недостаточностью (класс C по шкале Чайлд-Пью).
Рекомендуемая доза для пациентов с легким нарушением функции печени составляет 80 мг. Информация о применении лекарственного средства у пациентов с умеренной печеночной недостаточностью ограничена.
Педиатрическая популяция
Безопасность и эффективность АДЕНУРИКА у детей в возрасте до 18 лет не установлены.
Способ применения
Пероральное употребление
АДЕНУРИК следует вводить перорально, с пищей или без нее.
04.3 Противопоказания
Повышенная чувствительность к активному веществу или любому из вспомогательных веществ, перечисленных в разделе 6.1 (см. Также раздел 4.8).
04.4 Особые предупреждения и соответствующие меры предосторожности при использовании
Сердечно-сосудистые расстройства
Лечение фебуксостатом не рекомендуется пациентам с ишемической болезнью сердца или застойной сердечной недостаточностью.
В группе фебуксостата наблюдалось численно более высокое количество сердечно-сосудистых событий APTC (конечные точки, определенные в сотрудничестве с участниками Anti-Platelet Trialists) (включая смерть от сердечно-сосудистых заболеваний, нефатальный инфаркт миокарда, нефатальный инсульт) по сравнению с группой, получавшей лечение фебуксостатом. аллопуринол в исследованиях APEX и FACT (1,3 против 0,3 случая на 100 пациенто-лет), но не в исследовании CONFIRMS (подробные характеристики исследования см. в разделе 5.1). Частота сердечно-сосудистых событий APTC, сообщенных исследователем, в объединенных исследованиях фазы 3 (APEX, FACT и CONFIRMS) составила 0,7 против 0,6 случая на 100 пациенто-лет.
В долгосрочных расширенных исследованиях частота случаев APTC, о которых сообщил исследователь, составила 1,2 и 0,6 случая на 100 пациенто-лет для фебуксостата и аллопуринола, соответственно. Статистически значимых различий и причинно-следственной связи с фебуксостатом не выявлено. Факторами риска, выявленными для этих пациентов, были наличие в анамнезе атеросклеротического заболевания и / или инфаркта миокарда или застойной сердечной недостаточности.
Аллергия / гиперчувствительность к препарату
В постмаркетинговый период были собраны редкие сообщения о тяжелых аллергических реакциях / реакциях гиперчувствительности, включая опасный для жизни синдром Стивенса-Джонсона, токсический эпидермальный некролиз и острые анафилактические реакции / шок. В большинстве случаев эти реакции возникали в течение первого месяца терапии фебуксостатом. Некоторые, но не все, из этих пациентов сообщили о почечной недостаточности и / или предшествующей гиперчувствительности к аллопуринолу. В некоторых случаях тяжелые реакции гиперчувствительности, включая лекарственную реакцию с эозинофилией и системными симптомами (DRESS), были связаны с лихорадкой, гематологическим поражением, поражением почек. или печеночной. Пациентов следует проинформировать о признаках и симптомах и внимательно следить за симптомами аллергических реакций / реакций гиперчувствительности (см. раздел 4.8). Лечение фебуксостатом следует немедленно прекратить, если возникают тяжелые аллергические реакции / реакции гиперчувствительности, включая синдром Стивенса-Джонсона, поскольку превентивное прекращение лечения связано с лучшим прогнозом. Если у пациента развилась аллергическая реакция / реакция гиперчувствительности, включая синдром Стивенса-Джонсона и анафилактическую реакцию / шок, прием фебуксостата прекращается.
Острые приступы подагры (обострение)
Лечение фебуксостатом не следует начинать до полного исчезновения острого приступа подагры. В начале терапии могут возникнуть обострения подагры из-за изменения уровня мочевой кислоты в сыворотке крови. Определяется после мобилизации уратов из отложений в тканях. (см. разделы 4.8 и 5.1). В начале лечения фебуксостатом рекомендуется профилактика обострений подагры в течение не менее 6 месяцев с помощью НПВП или колхицина (см. Раздел 4.2).
Если во время лечения фебуксостатом возникает обострение подагры, его не следует отменять. Обострение следует лечить одновременно, в зависимости от индивидуальных потребностей пациента. Продолжение лечения фебуксостатом снижает частоту и интенсивность приступов подагры.
Отложение ксантина
У пациентов, у которых скорость образования уратов повышена (например, при злокачественных новообразованиях и во время их лечения или при синдроме Леша-Найхана), абсолютная концентрация ксантина в моче в редких случаях может увеличиваться до такой степени, чтобы позволить его отложение в мочевыводящих путях. Поскольку опыта применения фебуксостата нет, его применение этой категории пациентов не рекомендуется.
Меркаптопурин / азатиоприн
Использование фебуксостата не рекомендуется пациентам, одновременно принимающим меркаптопурин / азатиоприн. Если нельзя избежать одновременного применения, пациенты должны находиться под тщательным наблюдением. Во избежание возможных гематологических эффектов рекомендуется снижение дозы меркаптопурина или азатиоприна (см. Раздел 4.5).
Субъекты, перенесшие трансплантацию органов
Поскольку нет опыта применения АДЕНУРИКА у реципиентов трансплантата органов, использование фебуксостата у этих пациентов не рекомендуется (см. Раздел 5.1).
Теофиллин
Одновременное применение фебуксостата 80 мг и теофиллина 400 мг в виде однократной дозы у здоровых субъектов продемонстрировало отсутствие фармакокинетического взаимодействия (см. Раздел 4.5). Фебуксостат 80 мг можно применять у пациентов, принимающих одновременно теофиллин, без риска повышения уровня в плазме крови. теофиллин Данных для фебуксостата 120 мг нет.
Заболевания печени
В ходе объединенной фазы 3 клинических испытаний у пациентов, получавших фебуксостат, наблюдались легкие отклонения в тестах функции печени (5,0%). Перед началом терапии фебуксостатом и с периодичностью в дальнейшем по оценке врача рекомендуется проводить функциональные пробы печени (см. Раздел 5.1).
Заболевания щитовидной железы
В долгосрочных открытых расширенных исследованиях повышенные значения ТТГ (> 5,5 мкМЕ / мл) наблюдались у пациентов, длительно принимавших фебуксостат (5,5%). С осторожностью следует применять фебуксостат у пациентов с нарушением функции щитовидной железы (см. Раздел 5.1).
Лактоза
Таблетки Фебуксостат содержат лактозу. Пациентам с редкими наследственными формами непереносимости галактозы, дефицитом лактазы Лаппа или синдромом мальабсорбции глюкозы-галактозы не следует принимать это лекарство.
04.5 Взаимодействие с другими лекарственными средствами и другие формы взаимодействия
Меркаптопурин / азатиоприн
Основываясь на механизме действия фебуксостата на ингибирование ксантиноксидазы (XO), одновременный прием ADENURIC с меркаптопурином / азатиоприном не рекомендуется. Ингибирование XO фебуксостатом может вызвать повышение концентрации этих препаратов в плазме, что приводит к токсичности (см. Раздел 4.4. ). Исследования взаимодействия фебуксостата с препаратами, метаболизируемыми ХО, не проводились.
Исследования взаимодействия фебуксостата с цитотоксической химиотерапией не проводились.Нет данных о безопасности применения фебуксостата одновременно с цитотоксической терапией.
Субстраты розиглитазона / CYP2C8
Было показано, что фебуксостат является слабым ингибитором CYP2C8 in vitro. В исследовании на здоровых людях совместное введение 120 мг фебуксостата один раз в сутки с однократной пероральной дозой розиглитазона 4 мг не влияло на фармакокинетику розиглитазона и его метаболита N-десметилрозиглитазона, что указывает на то, что фебуксостат не является ингибитором ферментов CYP2C8 in vivo. Следовательно, не ожидается, что одновременное введение фебуксостата и розиглитазона или других субстратов CYP2C8 потребует какой-либо корректировки дозы этих соединений.
Теофиллин
Исследование взаимодействия с фебуксостатом было проведено на здоровых предметах, чтобы оценить, может ли ингибирование XO привести к увеличению уровней циркулирующего теофиллина, как сообщалось для других ингибиторов XO. Результаты исследования показывают, что совместное применение фебуксостата в дозе 80 мг один раз в сутки и теофиллина в дозе 400 мг не влияет на фармакокинетику и безопасность теофиллина. Следовательно, не требуется особой осторожности при одновременном применении фебуксостата 80 мг и теофиллина. Нет данных для фебуксостата 120 мг.
Напроксен и другие ингибиторы глюкуронизации
Метаболизм фебуксостата зависит от ферментов уридин-глюкуронозилтрансферазы (УГТ). Препараты, подавляющие глюкуронирование, такие как НПВП и пробенецид, теоретически могут влиять на выведение фебуксостата. У здоровых субъектов одновременный прием фебуксостата и напроксена 250 мг два раза в день был связан с повышенным воздействием фебуксостата (Cmax 28%, AUC 41% и t1 / 2 26%). В клинических исследованиях использование напроксена или других НПВП / ингибиторов Цокс-2 не было связано с какими-либо клинически значимыми побочными эффектами. Фебуксостат можно назначать одновременно с напроксеном, без корректировки дозы фебуксостата или напроксена.
Индукторы глюкуронизации
Мощные индукторы ферментов UGT могут привести к усилению метаболизма и снижению эффективности фебуксостата. Поэтому рекомендуется проверка мочевой кислоты в сыворотке крови через 1-2 недели после начала терапии мощным индуктором глюкуронизации. И наоборот, может возникнуть прекращение лечения индуктором глюкуронизации. при повышенном уровне фебуксостата в плазме.
Колхицин / индометацин / гидрохлоротиазид / варфарин
Фебуксостат можно назначать одновременно с колхицином или индометацином без необходимости корректировать дозу фебуксостата или другого одновременно вводимого активного вещества.
При одновременном применении с гидрохлоротиазидом коррекции дозы фебуксостата не требуется.
При одновременном применении с фебуксостатом коррекции дозы варфарина не требуется. Введение фебуксостата (80 мг или 120 мг один раз в сутки) с варфарином не влияло на фармакокинетику варфарина у здоровых пациентов. Кроме того, прием фебуксостата не влияет на МНО и активированный фактор VII.
Субстраты дезипрамин / CYP2D6
Было показано, что фебуксостат является слабым ингибитором CYP2D6. in vitro. В исследовании с участием здоровых субъектов прием 120 мг АДЕНУРИКА один раз в день приводил к среднему увеличению на 22% AUC дезипрамина, субстрата CYP2D6, что указывает на возможное слабое ингибирующее действие фебуксостата на фермент CYP2D6. in vivo. Следовательно, в случае одновременного приема фебуксостата и других субстратов CYP2D6, необходимость в какой-либо корректировке дозы любого из этих соединений невозможна.
Антациды
Было показано, что одновременный прием антацида, содержащего гидроксид магния и гидроксид алюминия, задерживает абсорбцию фебуксостата (примерно на 1 час) и вызывает 32% -ное снижение Cmax, в то время как не наблюдалось значительных изменений в отношении AUC . Поэтому можно принимать фебуксостат без учета приема антацидных препаратов.
04.6 Беременность и кормление грудью
Беременность
Данные об очень ограниченном числе беременных, подвергшихся воздействию облучения, указывают на отсутствие нежелательного воздействия фебуксостата на беременность или на здоровье плода / новорожденного. Исследования на животных не указывают прямого или косвенного вредного воздействия на беременность, эмбриональное / внутриутробное развитие или роды (см. Раздел 5.3). Потенциальный риск для человека неизвестен. Фебуксостат нельзя применять во время беременности.
Время кормления
Неизвестно, выделяется ли фебуксостат с грудным молоком. Исследования на животных показали, что выведение этого активного ингредиента с грудным молоком сопровождается дефицитом развития у новорожденных во время лактации. Нельзя исключить риск для грудного ребенка. Фебуксостат не следует использовать во время кормления грудью.
Плодородие
В исследованиях репродукции животных дозы до 48 мг / кг / день не показали дозозависимых побочных эффектов на фертильность (см. Раздел 5.3). Влияние АДЕНУРИКА на фертильность человека неизвестно.
04.7 Влияние на способность управлять автомобилем и работать с механизмами
Сообщалось о сонливости, головокружении, парестезии и нечеткости зрения при применении фебуксостата. Пациентам следует проявлять большую осторожность перед вождением, работой с механизмами или выполнением опасных действий, пока они не будут достаточно уверены, что использование АДЕНУРИКА не ухудшает их работоспособность.
04.8 Побочные эффекты
Резюме профиля безопасности
Наиболее частыми побочными реакциями, о которых сообщалось в клинических испытаниях (4072 пациента, получавших по крайней мере дозу от 10 до 300 мг) и в постмаркетинговом опыте, были острые приступы подагры, нарушения функции печени, диарея, тошнота, головная боль, сыпь и отек. побочные реакции были в основном легкой или средней степени тяжести. В постмаркетинговом опыте наблюдались редкие серьезные реакции гиперчувствительности на фебуксостат, некоторые из которых были связаны с системными симптомами.
Табличный список побочных реакций
Общие побочные реакции (≥1 / 100 -
Таблица 1: Побочные реакции, сообщенные в долгосрочных комбинированных исследованиях фазы III и в постмаркетинговом опыте
* Нежелательные реакции, собранные в ходе постмаркетингового опыта.
** Новые методы лечения неинфекционной диареи и аномальных функциональных проб печени в комбинированных исследованиях фазы 3 чаще встречаются у пациентов, получавших одновременно колхицин.
*** См. Раздел 5.1 о частоте приступов подагры в индивидуальных рандомизированных контролируемых исследованиях 3 фазы.
Описание избранных побочных реакций
При постмаркетинговом опыте наблюдались редкие случаи тяжелых реакций гиперчувствительности на фебуксостат, включая синдром Стивенса-Джонсона, токсический эпидермальный некролиз и анафилактические / шоковые реакции. Синдром Стивенса-Джонсона и токсический эпидермальный некролиз характеризуются прогрессирующими кожными высыпаниями, связанными с волдырями или поражениями слизистых оболочек. и раздражение глаз.
Реакции гиперчувствительности на фебуксостат могут быть связаны со следующими симптомами: кожные реакции, характеризующиеся инфильтрированной макулопапулезной сыпью, генерализованными или эксфолиативными высыпаниями, а также кожными поражениями, отеком лица, лихорадкой, гематологическими изменениями, такими как тромбоцитопения и эозинофилия, а также поражением одного или нескольких органов ( печень и почки, включая тубулоинтерстициальный нефрит) (см. раздел 4.4).
Острые приступы подагры обычно наблюдались вскоре после начала лечения и в течение первых нескольких месяцев.После этого частота обострений подагры уменьшается со временем. Рекомендуется профилактика острых приступов подагры (см. Разделы 4.2 и 4.4).
Сообщение о предполагаемых побочных реакциях
Сообщение о предполагаемых побочных реакциях, возникающих после получения разрешения на лекарственный препарат, важно, поскольку оно позволяет осуществлять непрерывный мониторинг баланса пользы / риска лекарственного препарата. Медицинских работников просят сообщать о любых предполагаемых побочных реакциях через национальную систему отчетности. "Адрес https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Передозировка
В случае передозировки пациентам следует оказывать симптоматическую и поддерживающую терапию.
05.0 ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
05.1 Фармакодинамические свойства
Фармакотерапевтическая группа: Препараты, препятствующие выработке мочевой кислоты, препараты, подавляющие выработку мочевой кислоты.
Код УВД: M04AA03
Механизм действия
Мочевая кислота является конечным продуктом метаболизма пуринов, и у людей она вырабатывается в соответствии с последовательностью гипоксантин → ксантин → мочевая кислота. Обе стадии вышеуказанной реакции катализируются ксантиноксидазой (XO). Фебуксостат является производным 2 -арилтиазола, который имеет терапевтический эффект снижения уровня мочевой кислоты в сыворотке за счет селективного ингибирования XO. Фебуксостат - мощный непуриновый селективный ингибитор XO (NP-SIXO) со значением Ki (постоянное ингибирование d) in vitro менее 1 наномоля. Было показано, что фебуксостат с большой эффективностью ингибирует ХО как в окисленной, так и в восстановленной форме. В терапевтических концентрациях фебуксостат не ингибирует другие ферменты, участвующие в метаболизме пуринов или пиримидинов, а именно гуаниндезаминазу, гипоксантингуанинфосфорибозилтрансферазу, оротатфосфорибозилтрансферазу, оротидинмонофосфатдекарбоксилазу или пуриновую нуклеозилазу.
Клиническая эффективность и безопасность
Эффективность АДЕНУРИКА была продемонстрирована в трех основных исследованиях фазы 3 (два основных исследования APEX и FACT и дополнительное исследование CONFIRMS, описанное ниже), которые были проведены у 4 101 пациента с гиперурикемией и подагрой. В каждом из исследований основной фазы 3 АДЕНУРИК продемонстрировал большую способность, чем аллопуринол, снижать и поддерживать уровни мочевой кислоты в сыворотке. Первичной конечной точкой эффективности в исследованиях APEX и FACT был процент пациентов, у которых уровень мочевой кислоты в сыворотке за последние 3 месяца был
Исследование APEX: APEX (исследование эффективности аллопуринола и плацебо-контролируемой эффективности фебуксостата - исследование эффективности контролируемого фебуксостата в отношении аллопуринола и плацебо) было рандомизированным двойным слепым многоцентровым 28-недельным исследованием фазы 3. кто получал: плацебо (n = 134), ADENURIC 80 мг один раз в день (n = 267), ADENURIC 120 мг один раз в день (n = 269), ADENURIC 240 мг один раз в день (n = 134) или аллопуринол (в дозе 300 мг один раз в сутки [n = 258] для пациентов с исходным уровнем креатинина сыворотки ≤1,5 мг / дл или в дозе 100 мг один раз в сутки [n = 10] для пациентов с исходным уровнем креатинина сыворотки> 1,5 мг / дл и ≤2,0 мг / дл ) Для оценки безопасности использовалась доза фебуксостата 240 мг (что в два раза больше максимальной рекомендованной дозы).
Исследование APEX продемонстрировало статистически значимое превосходство групп, получавших как АДЕНУРИК 80 мг один раз в сутки, так и АДЕНУРИК 120 мг один раз в сутки, в снижении уровня мочевой кислоты в сыворотке до уровней ниже 6 мг / дл (357 мкмоль / л) по сравнению с группами, получавшими обычные дозы аллопуринола. 300 мг (n = 258) / 100 мг (n = 10) (см. Таблицу 2 и Рисунок 1). Исследование FACT: FACT (контролируемое исследование фебуксостата аллопуринола) было 52-недельным рандомизированным двойным слепым многоцентровым исследованием фазы 3. Были рандомизированы 760 пациентов, которые получали: АДЕНУРИК 80 мг один раз в сутки (n = 256), АДЕНУРИК 120 мг один раз в сутки (n = 251) или аллопуринол 300 мг один раз в сутки (n = 253).
Исследование FACT продемонстрировало статистически значимое превосходство групп АДЕНУРИКА 80 мг и АДЕНУРИКА 120 мг один раз в сутки в снижении и поддержании уровня мочевой кислоты в сыворотке ниже 6 мг / дл (357 мкмоль / л) по сравнению с группой, получавшей обычную дозу аллопуринола 300. мг.
В таблице 2 приведены результаты первичной конечной точки эффективности:
Таблица 2
Процент пациентов с уровнем мочевой кислоты в сыворотке крови
Последние три посещения в месяц
Способность АДЕНУРИКА снижать уровень мочевой кислоты в сыворотке была быстрой и стойкой. Снижение уровня мочевой кислоты в сыворотке до значений.
Исследование CONFIRMS: исследование CONFIRMS представляло собой 26-недельное рандомизированное контролируемое исследование фазы 3 для оценки безопасности и эффективности фебуксостата 40 мг и 80 мг по сравнению с аллопуринолом 300 или 200 мг у пациентов с подагрой и гиперурикемией. Пациенты были рандомизированы: АДЕНУРИК 40 мг один раз в сутки (n = 757), АДЕНУРИК 80 мг один раз в сутки (n = 756) или аллопуринол 300/200 мг один раз в сутки (n = 756). 65% пациентов имели почечную недостаточность от легкой до умеренной ( с клиренсом креатинина 30-89 мл / мин) Профилактика подагры была обязательной после 26-недельного периода.
Доля пациентов с уровнем уратов в сыворотке мкмоль / л на последнем визите составила 45% для 40 мг фебуксостата, 67% для 80 мг фебуксостата и 42% для аллопуринола 300/200 мг, соответственно.
Первичная конечная точка в подгруппе пациентов с почечной недостаточностью
В исследовании APEX оценивалась эффективность препарата у 40 пациентов с почечной недостаточностью (исходный уровень креатинина сыворотки> 1,5 мг / дл и ≤ 2,0 мг / дл). Для пациентов с нарушением функции почек, которые были рандомизированы для приема аллопуринола, последняя доза была ограничена до 100 мг. один раз в день. Аденурик достиг первичной конечной точки эффективности у 44% (80 мг один раз в день), 45% (120 мг один раз в день) и 60% (240 мг один раз в день) пациентов соответственно по сравнению с 0%, обнаруженным у аллопуринола 100 мг один раз в день и группы плацебо.
Не наблюдалось клинически значимых различий в скорости снижения концентрации мочевой кислоты в сыворотке крови у здоровых субъектов независимо от их почечного функционального статуса (58% в группе с нормальной функцией почек и 55% в группе с тяжелой почечной недостаточностью).
«Анализ у пациентов с подагрой и почечной недостаточностью был проспективно определен в исследовании CONFIRMS и продемонстрировал, что фебуксостат значительно более эффективен в снижении уровня уратов в сыворотке, чем
Первичная конечная точка в подгруппе пациентов с уровнем мочевой кислоты в сыворотке ≥ 10 мг / дл
Примерно 40% пациентов (APEX и FACT вместе взятые) имели исходное значение мочевой кислоты в сыворотке ≥ 10 мг / дл. В этой подгруппе ADENURIC достиг первичной конечной точки эффективности (уровень мочевой кислоты
В исследовании CONFIRMS доля пациентов, достигших первичной конечной точки эффективности (уровень мочевой кислоты
Клинические результаты: процент пациентов, которым потребовалось лечение от приступа подагры.
Исследование APEX: в течение 8-недельного периода профилактики большая часть (36%) пациентов, получавших фебуксостат в дозе 120 мг, нуждалась в лечении от приступа подагры, чем фебуксостат 80 мг (28%), аллопуринол 300 мг (23%) и плацебо ( 20%). Приступы увеличивались после периода профилактики и постепенно уменьшались с течением времени. От 46% до 55% субъектов получали лечение от острых приступов подагры с 8 по 28 неделю. Приступы подагры в течение последних 4 недель исследования (24 недели). -28) наблюдались у 15% (фебуксостат 80, 120 мг), 14% (аллопуринол 300 мг) и 20% (плацебо) пациентов. ФАКТ: В течение 8-недельного периода профилактики большая часть (36%) пациентов, получавших фебуксостат в дозе 120 мг, требовалось лечение обострения подагры, чем при лечении фебуксостатом в дозе 80 мг (22%) и аллопуринолом в дозе 300 мг (21%).
После 8-недельного периода профилактики частота острых приступов постепенно увеличивалась и снижалась с течением времени (64% и 70% субъектов получали лечение от острых приступов подагры с 8-й по 52-ю неделю). исследования (49-52 недели) наблюдались у 6-8% (фебуксостат 80 мг, 120 мг) и 11% (аллопуринол 300 мг) пациентов.
Процент пациентов, которым потребовалось лечение обострения подагры (исследования APEX и FACT), был численно ниже в группах, которые достигли среднего уровня уратов в сыворотке после исходного уровня.
Во время исследования CONFIRMS процент пациентов, нуждающихся в лечении приступов подагры (с 1-го по 6-й месяц), составлял 31% и 25% для групп фебуксостата 80 мг и аллопуринола, соответственно. Не было различий в доле пациентов, нуждающихся в лечении приступов подагры, между группами фебуксостата 80 мг и 40 мг.
Долгосрочные исследования по расширению открытых лейблов
Исследование EXCEL (C02-021): EXCEL представляло собой трехлетнее открытое, многоцентровое, рандомизированное, контролируемое аллопуринолом, расширенное исследование безопасности фазы 3 для пациентов, которые завершили основные исследования фазы 3 (APEX или FACT). Всего было включено 1086 пациентов: АДЕНУРИК 80 мг один раз в сутки (n = 649), АДЕНУРИК 120 мг один раз в сутки (n = 292) и аллопуринол 300/100 мг один раз в сутки (n = 145). Примерно 69% пациентов не потребовалось никаких изменений в лечении для достижения стабильного окончательного ответа. Пациенты с тремя последовательными уровнями мочевины> 6,0 мг / дл были исключены.
Уровни уратов в сыворотке крови поддерживались с течением времени (например, 91% и 93% пациентов, получавших первоначальное лечение фебуксостатом 80 мг и 120 мг, соответственно, имели урикемию.
Трехлетние данные продемонстрировали снижение частоты обострений подагры менее чем у 4% пациентов, нуждающихся в лечении по поводу обострения (т. Е. У более 96% пациентов, не нуждающихся в лечении обострения) через 16-24 месяцев и 30 лет. 36 месяцев 46% и 38% пациентов, получавших окончательное стабильное лечение фебуксостатом 80 мг или 120 мг один раз в день, соответственно, имели полное разрешение пальпируемого первичного тофуса от исходного уровня до последнего визита.
Исследование FOCUS (TMX-01-005): FOCUS представляло собой 5-летнее открытое многоцентровое расширенное исследование безопасности фазы 2 для пациентов, которые завершили 4 недели приема фебуксостата в двойном слепом исследовании TMX -00-004. В исследование были включены 116 пациентов, которые первоначально получали фебуксостат 80 мг один раз в сутки. 62% пациентов не нуждались в коррекции дозы для поддержания урикемии.
Доля пациентов с уровнем уратов в сыворотке крови
Во время фазы 3 клинических испытаний у пациентов, получавших фебуксостат, наблюдались незначительные изменения показателей функции печени (5,0%). Эти значения были аналогичны тем, о которых сообщалось для аллопуринола (4,2%) (см. Раздел 4.4). Повышенные значения ТТГ (> 5,5 мкМЕ / мл) наблюдались в долгосрочных открытых расширенных исследованиях у пациентов. у пациентов, получавших фебуксостат (5,5%), и у пациентов, получавших аллопуринол (5,8%) (см. раздел 4.4).
05.2 Фармакокинетические свойства
У здоровых субъектов Cmax (максимальная концентрация в плазме) и AUC (площадь под кривой) фебуксостата увеличивались пропорционально дозе после однократного и многократного введения с 10 мг до 120 мг. Для доз фебуксостата от 120 мг до 300 мг больше чем наблюдается пропорциональное дозе увеличение AUC. После приема доз от 10 мг до 240 мг каждые 24 часа заметного накопления не наблюдается. Фебуксостат имеет очевидный конечный период полувыведения (t1 / 2) примерно 5-8 часов.
Популяционный фармакокинетический / фармакодинамический анализ был проведен у 211 пациентов с гиперурикемией и подагрой, получавших АДЕНУРИК в дозе 40–240 мг один раз в сутки.
В целом фармакокинетические параметры фебуксостата, оцененные с помощью этих анализов, соответствуют параметрам, наблюдаемым у здоровых субъектов, что указывает на то, что здоровые субъекты являются репрезентативными для целей фармакокинетической / фармакодинамической оценки в популяции пациентов с подагрой.
Абсорбция
Фебуксостат всасывается быстро (Tmax 1,0–1,5 ч) и почти полностью (не менее 84%). После приема однократной пероральной дозы или нескольких пероральных доз 80 и 120 мг один раз в день Cmax составляет приблизительно 2,8–3,2 мкг / мл и 5,0–5,3 мкг / мл, соответственно. Абсолютная биодоступность таблетированной формы фебуксостата не изучалась.
После приема нескольких пероральных доз 80 мг один раз в сутки или однократной дозы 120 мг вместе с пищей с высоким содержанием жиров наблюдалось снижение Cmax на 49% и 38%, соответственно, и снижение Cmax. "AUC 18 % и 16% соответственно.
Однако клинически значимых изменений в процентном снижении концентрации мочевой кислоты в сыворотке крови при оценке (повторные дозы 80 мг) не наблюдалось, поэтому АДЕНУРИК можно принимать как во время еды, так и вдали от нее.
Распределение
Кажущийся объем распределения при устойчивое состояние (Vss / F) фебуксостата составляет от 29 до 75 л после перорального приема 10-300 мг. Связывание фебуксостата с белками плазмы составляет приблизительно 99,2% (в основном с альбумином), и остается постоянным при концентрациях, достигнутых при дозах от 80 до 120 мг. Связывание с белками плазмы метаболитов составляет приблизительно от 82% до 91%.
Биотрансформация
Фебуксостат интенсивно метаболизируется путем конъюгации через ферментную систему уридиндифосфатглюкуронозилтрансферазы (UDPGT) и путем окисления через систему цитохрома P450 (CYP). Идентифицировано четыре фармакологически активных гидроксильных метаболита, три из которых можно наблюдать в плазме человека. Исследования in vitro с микросомами печени человека показали, что эти окислительные метаболиты состоят в основном из CYP1A1, CYP1A2, CYP2C8 или CYP2C9 и глюкуронида фебуксостата в основном из UGT 1A1, 1A8 и 1A9.
Устранение
Фебуксостат выводится как через печень, так и через почки. После перорального приема 80 мг фебуксостата, меченного 14C, примерно 49% дозы было извлечено с мочой в виде неизмененного фебуксостата (3%), активного вещества ацилглюкуронида (30%), его окислительных метаболитов вместе с их конъюгатами (13 %) и другие неизвестные метаболиты (3%). Помимо выведения с мочой, примерно 45% дозы было извлечено с фекалиями в виде неизмененного фебуксостата (12%), ацилглюкуронида активного ингредиента (1%), его известных окислительных метаболитов вместе с их конъюгатами (25%). ) и другие неизвестные метаболиты (7%).
Почечная недостаточность
После приема повторных доз 80 мг АДЕНУРИКА пациентам с легкой, умеренной или тяжелой почечной недостаточностью Cmax фебуксостата не отличалась от таковой у пациентов с нормальной функцией почек. Общая средняя AUC фебуксостата увеличилась примерно в 1,8 раза с 7,5 мкг.ч / мл в группе с нормальной функцией почек до 13,2 мкг.ч / мл в группе с тяжелой почечной недостаточностью. AUC активных метаболитов увеличилась до 2 и 4 фолд соответственно. Однако у пациентов с легкой или умеренной почечной недостаточностью коррекция дозы не требуется.
Печеночная недостаточность
После повторного введения 80 мг АДЕНУРИКА пациентам с легким (класс A по классификации Чайлд-Пью) или умеренным (класс B по классификации Чайлд-Пью) печеночной недостаточностью Cmax и AUC фебуксостата и его метаболитов существенно не изменились по сравнению с пациентами с нормальным состоянием. функция печени. Исследования у пациентов с тяжелой печеночной недостаточностью (класс C по шкале Чайлд-Пью) не проводились.
Возраст
Не наблюдалось значительных изменений AUC фебуксостата или его метаболитов после повторного приема пероральных доз АДЕНУРИКА пожилым людям по сравнению с более молодыми здоровыми людьми.
Тип
После повторных пероральных доз АДЕНУРИКА Cmax и AUC у женщин были на 24% и 12% выше, чем у мужчин, соответственно. Однако скорректированные по массе Cmax и AUC были одинаковыми для обоих полов. Коррекция дозы в зависимости от пола не требуется.
05.3 Доклинические данные по безопасности
Эффекты, которые имели место в доклинических исследованиях, обычно наблюдались при воздействии лекарств, превышающей максимальное воздействие на человека.
Канцерогенез, мутагенез, нарушение фертильности
У самцов крыс статистически значимое увеличение опухолей мочевого пузыря (переходно-клеточная папиллома и карцинома) наблюдалось только при наличии ксантиновых камней в группе, получавшей самую высокую дозу, соответствующую дозам, примерно в 11 раз превышающим дозу воздействия. Нет значительного увеличения ни у одного из других типов опухолей, ни у самцов мышей или крыс, ни у самок мышей или крыс. Эти наблюдения считаются следствием видоспецифичного метаболизма пуринов и состава мочи и не имеют отношения к клиническое применение лекарственного средства.
Стандартная батарея тестов на генотоксичность не выявила каких-либо значимых генотоксических эффектов фебуксостата.
Фебуксостат в пероральных дозах до 48 мг / кг / сут не влиял на фертильность и репродуктивную способность как у самцов, так и у самок крыс.
Не было доказательств нарушения фертильности, тератогенных эффектов или вредных последствий для плода от действия фебуксостата. У крыс при высоких дозах и при воздействии примерно в 4,3 раза больше, чем у человека, наблюдалась токсичность для матери, сопровождаемая снижение индекса отъема и задержка развития потомства.Тератологические исследования, проведенные на беременных крысах и кроликах с экспозицией примерно в 4,3 и 13 раз выше, чем у человека, соответственно, не выявили каких-либо тератогенных эффектов фебуксостата.
06.0 ФАРМАЦЕВТИЧЕСКАЯ ИНФОРМАЦИЯ
06.1 Вспомогательные вещества
Ядро планшета
Моногидрат лактозы
Микрокристаллическая целлюлоза
Стеарат магния
Гидроксипропилцеллюлоза
Кроскармеллоза натрия
Кремнезем коллоидный гидратированный
Покрытие таблеток
Опадрий II, желтый, 85F42129, содержащий:
Поливиниловый спирт
Диоксид титана (E171)
Макрогол типа 3350
Тальк
Желтый оксид железа (E172)
06.2 Несовместимость
Не имеет значения.
06.3 Срок действия
3 года.
06.4 Особые меры предосторожности при хранении
Это лекарство не требует особых условий хранения.
06.5 Характер непосредственной упаковки и содержимого упаковки
Прозрачный блистер (Aclar / PVC / Aluminium), содержащий 14 таблеток.
АДЕНУРИК 80 мг выпускается в упаковках по 14, 28, 42, 56, 84 и 98 таблеток, покрытых пленочной оболочкой.
Не все размеры упаковки могут быть проданы.
06.6 Инструкции по эксплуатации и обращению
Никаких особых инструкций.
07.0 ДЕРЖАТЕЛЬ РАЗРЕШЕНИЯ НА МАРКЕТИНГ
Menarini International Operations Luxembourg S.A.
1, Avenue de la Gare, L-1611 Люксембург
Люксембург
08.0 НОМЕР РАЗРЕШЕНИЯ НА МАРКЕТИНГ
EU / 1/08/447/001
EU / 1/08/447/002
EU / 1/08/447/005
EU / 1/08/447/006
EU / 1/08/447/007
EU / 1/08/447/008
039538018
039538020
09.0 ДАТА ПЕРВОГО РАЗРЕШЕНИЯ ИЛИ ПРОДЛЕНИЯ РАЗРЕШЕНИЯ
Дата первого разрешения: 21 апреля 2008 г.
Дата последнего обновления: 20 декабря 2012 г.
10.0 ДАТА ПЕРЕСМОТРА ТЕКСТА
Апрель 2015 г.