Есть опасения, что генные манипуляции также могут быть применены, чтобы попытаться улучшить спортивные результаты; в этом смысле Всемирное антидопинговое агентство (ВАДА) уже предприняло шаги, включив генетический допинг в список запрещенных методов и веществ.
Теоретически все уровни белков, присутствующих в нашем организме, можно регулировать с помощью генной терапии.
Конференция по генетическому допингу, проведенная в марте 2002 года ВАДА [Pound R, WADA 2002], и «Европейский трудовой конгресс по гармонизации и будущему развитию антидопинговой политики», который проходил в Арнеме, Голландия, в том же год, дал возможность ученым, врачам, врачам, правительствам, антидопинговым организациям и фармацевтическим предприятиям обмениваться любой информацией о результатах исследований и методах обнаружения, касающихся этого нового метода допинга.
С 1 января 2003 г. Международный олимпийский комитет (МОК) включил генетический допинг в список запрещенных классов и методов веществ [WADA, 2007]. С 2004 года ВАДА взяло на себя ответственность за публикацию международного списка допинга, который ежегодно обновляется. Метод генетического допинга, включенный в этот список, определяется как нетерапевтическое использование клеток, генов, генетических элементов или модуляция экспрессии генов с целью улучшения спортивных результатов.
Эта статья направлена на:
- выяснить, действительно ли в спорте можно использовать все новые знания, полученные в результате генной терапии, новой и многообещающей отрасли традиционной медицины;
- определить возможные способы использования генной терапии для повышения производительности.
В этот «век генетики и геномики» можно будет выявить гены, определяющие генетическую предрасположенность человека к конкретному виду спорта [Ранкинен Т. и др., 2004]. Изучение генов в молодом возрасте может представлять собой лучший способ развить великого спортсмена, начиная с ребенка, и создать конкретную персональную программу тренировок. Это исследование, применяемое к спортсменам, также может быть использовано для определения конкретных тренировочных методов с целью увеличения генетической предрасположенности к этому типу тренировок [Rankinen T. et al., 2004].
Но приведет ли изучение генов к лучшим спортсменам?
Мэрион Джонс и Тим Монтгомери оба были чемпионами по скорости на 100 м, у них летом 2003 года родился ребенок. У Штеффи Граф и Андре Агасси (оба чемпионата мира по теннису) также есть дети. Эти дети, скорее всего, будут фаворитами. По сравнению с другими, но есть также другие факторы, такие как экологические и психологические, которые будут определять вероятность того, что они станут чемпионами, или нет.
Генную терапию можно определить как перенос генного материала в клетки человека для лечения или предотвращения заболевания или дисфункции. Этот материал представлен ДНК, РНК или генетически измененными клетками. Принцип генной терапии основан на введении в клетку терапевтического гена для компенсации недостающего гена или замены аномального. Обычно используется ДНК, которая кодирует терапевтический белок и активируется, когда достигает ядра.
«Большинство спортсменов принимают наркотики» [De Francesco L, 2004].
Опрос, проведенный Центром исследования лекарств, показал, что менее 1% населения Нидерландов хотя бы раз принимали допинг, в общей сложности около 100 000 человек. 40% этих людей употребляли допинг в течение многих лет, и большинство из них занимаются силовыми тренировками или бодибилдингом. Использование допинговых веществ в элитном спорте, по-видимому, выше, чем 1%, указанный для населения в целом, но точная цифра неизвестна. Доля элитных спортсменов, у которых положительный результат теста на допинг-контроль колеблется от 1%. 1,3% и 2,0% в последние годы [DoCoNed, 2002].
Определение генетического допинга ВАДА оставляет место для вопросов
- Что именно означает нетерапевтическое?
- Будут ли допущены к соревнованиям пациенты с мышечными дисфункциями, леченными генной терапией?
То же самое относится и к онкологическим больным, которые прошли курс химиотерапии и теперь получают ген ЭПО, кодирующий эритропоэтин, для ускорения восстановления функции костного мозга.
Текущие исследования в области генной терапии также проводятся для ускорения процесса заживления ран или для облегчения боли в мышцах после упражнений; такие методы не могут рассматриваться всеми как «терапевтические», и их свойства повышения эффективности могут быть поставлены под сомнение.
С клинической точки зрения было бы более уместно дать более точное определение генетическому допингу, особенно в свете неправильного использования технологий переноса генов.
ВАДА (раздел М3 Всемирный антидопинговый кодекс (версия от 1 января 2007 г.) обосновал запрет на генетический допинг следующими пунктами:
- научные доказательства, подтвержденный фармакологический эффект или опыт, что вещества или методы, включенные в список, обладают способностью повышать спортивные результаты;
- использование вещества или метода создает реальный или предполагаемый риск для здоровья спортсмена.
- Использование допинга нарушает дух спорта. Этот дух описан во введении к Кодексу со ссылкой на ряд ценностей, таких как этика, честная игра, честность, здоровье, веселье, счастье и соблюдение правил.
Есть много неопределенностей относительно долгосрочных эффектов модификации генов; многие из этих эффектов также могут никогда не быть обнаружены либо потому, что они не были тщательно изучены (из-за финансовых проблем), либо потому, что трудно определить надежные образцы для изучения побочных эффектов совершенно новых методов или приложений.
В отличие от терапии соматическими клетками, изменения зародышевых линий являются постоянными и также передаются потомству. В этом случае, помимо возможного риска для здоровья спортсменов, существуют также риски для третьих лиц, таких как потомство, родители или партнеры.
В области фармакогенетики, развитие которой зависит от объединенных усилий науки и фармацевтической промышленности, основная цель - разработать лекарство, «адаптированное» для каждого из нас. Как известно, многие лекарства имеют совершенно разные зависимости. От того, кто их принимает, это связано с тем, что их развитие носит родовой характер и не учитывает индивидуальные генетические особенности. Если бы фармакогенетика получила распространение в мире спорта, сама идея соревнования между очевидно равными спортсменами, готовящимися более или менее сопоставимым образом, могла бы стать устаревшей.
Экспериментальные клинические данные генной терапии показали очень обнадеживающие результаты у пациентов с тяжелым комбинированным иммунодефицитом [Hacein-Bey-Abina S et al., 2002] и гемофилией B [Kay MA, et al. 2000]. Кроме того, ангиогенная терапия с использованием векторов, экспрессирующих фактор роста эндотелия сосудов, для лечения ишемической болезни сердца дала хорошие результаты при стенокардии [Losordo DW et al., 2002].
Если использовать перенос генов, кодирующих факторы роста тканей [Huard J, Li Y, Peng HR, Fu FH, 2003], теоретически может привести к лечению различных повреждений, связанных со спортивной практикой, таких как разрыв связок или разрыв мышц. в лучшей регенерации. Эти подходы сейчас оцениваются на животных моделях, но в ближайшие годы, безусловно, будут активизированы клинические испытания на людях.
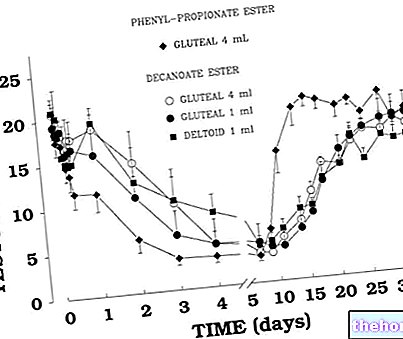
В 1964 году лыжник из Северной Финляндии Ээро Мянтюранта сделал усилия своих оппонентов бесполезными, выиграв два олимпийских золота на Играх в Инсбруке, Австрия. Через несколько лет было показано, что Mantyranta несет редкую мутацию в гене рецептора эритропоэтина, которая, нарушая нормальный контроль количества эритроцитов с обратной связью, вызывает полицитемию с последующим увеличением на 25-50% кислородная транспортная способность. Увеличение количества кислорода к тканям означает повышение устойчивости к усталости. В Мянтюранте было то, чего хочет каждый спортсмен: ЭПО. Спортсмены будущего могут иметь возможность внедрить в свое тело ген, имитирующий эффект мутации гена, естественным образом возникший в Мянтюранте, и способствующий повышению производительности.
Инсулиноподобный фактор роста (IGF-1) вырабатывается как печенью, так и мышцами, и его концентрация зависит от концентрации гормона роста человека (hGH).
Тренировка, как предполагает Суини, стимулирует клетки-предшественники мышц, называемые «сателлитами», чтобы они были более «восприимчивыми к IGF-I».
[Ли С. Бартон ER, Суини Х.Л., Фаррар Р.П., 2004]. Применение этого лечения к спортсменам означало бы укрепить плечевые мышцы теннисиста, икроножные мышцы бегуна или бицепсы боксера. Считается, что такая терапия относительно безопаснее, чем ЭПО, поскольку эффект локализуется только в целевой мышце. Вероятно, что уже в ближайшие несколько лет этот подход будет применяться и к людям.
Изоформа инсулиноподобного фактора роста-1 (IGF-1), механический фактор роста (MGF), активируется механическими стимулами, такими как, например, Упражнение для мышц. Этот белок, помимо стимуляции роста мышц, играет важную роль в восстановлении поврежденной мышечной ткани (как это происходит, например, после интенсивных тренировок или соревнований).
MGF вырабатывается в мышечной ткани и не циркулирует в крови.
VEGF представляет собой фактор роста эндотелия сосудов и может использоваться для облегчения роста новых кровеносных сосудов. Терапия VEGF была разработана для проведения аортокоронарного шунтирования у пациентов с ишемической болезнью сердца или для помощи пожилым людям с заболеванием периферических артерий. Гены этот код для VEGF может способствовать росту новых кровеносных сосудов, обеспечивая больший приток кислорода к тканям.
До сих пор эксперименты по генной терапии проводились для лечения таких заболеваний, как ишемия сердца [Barton-Davis ER et al., 1998; Losordo DW et al., 2002; Tio RA et al., 2005] или периферической артериальной недостаточности [Baumgartner I и др., 1998; Раджагопалан С. и др., 2003].
Если бы эти методы лечения применялись также к спортсменам, результатом было бы увеличение содержания кислорода и питательных веществ в тканях, но, прежде всего, возможность отсрочить истощение как сердечных, так и скелетных мышц.
Поскольку VEGF уже используется во многих клинических испытаниях, генетический допинг уже возможен.
Нормальный дифференциация костно-мышечной массы это имеет фундаментальное значение для правильного функционирования организма; эта функция стала возможной благодаря действию миостатина, белка, ответственного за рост и дифференциацию скелетных мышц.
Он действует как негативный регулятор, подавляя пролиферацию сателлитных клеток в мышечных волокнах.
Экспериментально используется миостатин. in vivo для подавления мышечного развития в различных моделях млекопитающих.
Миостатин действует как по аутокринному, так и по паракринному механизму, как на скелетно-мышечном, так и на сердечном уровне. Его физиологическая роль еще полностью не изучена, хотя использование ингибиторов миостатина, таких как фоллистатин, вызывает резкое и повсеместное увеличение мышечной массы [Lee SJ, McPherron AC, 2001]. Такие ингибиторы могут улучшить регенеративное состояние у пациентов, страдающих от серьезные заболевания, такие как мышечная дистрофия Дюшенна [Богданович С. и др., 2002]].
Миостатин принадлежит к суперсемейству TGF beta и впервые был обнаружен группой Се-Джин Ли [McPherron et al., 1997]. В 2005 году Се-Джин Ли из Университета Джона Хопкинса указал, что у мышей, лишенных гена миостатина (нокаутные мыши), развивается гипертрофическая мускулатура.
Эти супермыши были способны подниматься по лестнице с тяжелыми грузами, прикрепленными к их хвостам. В течение того же года три другие исследовательские группы показали, что фенотип крупного рогатого скота, обычно называемый «двойными мышцами», является следствием мутации в гене, кодирующем миостатин [Grobet et al., 1997; Kambadur et al., 1997; McPherron & Lee, 1997].
Мутация гомозиготного типа mstn - / - была недавно обнаружена у немецкого ребенка, который развил необычайную мышечную массу. Мутация упоминается как эффект подавления экспрессии миостатина у людей. Ребенок хорошо развил мышцы при рождении, но взросление также увеличило развитие мышечной массы, и к 4 годам он уже мог поднимать 3 кг веса; он сын бывшего профессионального спортсмена, а его дедушка и бабушка были известны как очень сильные мужчины.
Генетический анализ матери и ребенка выявил мутацию в гене миостатина, приводящую к недостатку продукции белка [Shuelke M et al., 2004].
Как в случае экспериментов, проведенных на мышах группой Се-Джин Ли, так и в экспериментах с ребенком, мышца выросла как в поперечном сечении (гипертрофия), так и в количестве миофибрилл (гиперплазия) [McPherron et al. ., 1997].
Боль - это неприятное сенсорное и эмоциональное переживание, связанное с действительным или потенциальным повреждением тканей и описываемое в терминах такого повреждения [iasp]. Из-за своей неприятной эмоции боль нельзя игнорировать и побуждает субъекта, который пытается ее, избегать (ядовитых) стимулов, ответственных за нее; этот аспект настраивает защитную функцию боли.
В спорте использование сильнодействующих обезболивающих может побудить спортсменов тренироваться и соревноваться за пределы нормального болевого порога.
Это может стать причиной значительного риска для здоровья спортсмена, поскольку травма может значительно усугубиться, превратившись в необратимую травму. Использование этих препаратов также может привести спортсмена к психофизической зависимости от них.
Альтернативой легальным обезболивающим может быть использование обезболивающих пептидов, таких как эндорфины или энкефалины. Доклинические исследования на животных показали, что гены, кодирующие эти пептиды, влияют на восприятие воспалительной боли [Lin CR et al., 2002; Smith O. , 1999].
Однако генная терапия для обезболивания еще далека от своего клинического применения.
, химические вещества, вирусы и т. д.) и закодированный трансген.На сегодняшний день клинические исследования относительно безопасны [Kimmelman J, 2005]. Более 3000 пациентов прошли курс лечения, и только один из них умер от хронического заболевания печени и передозировки переносчиками инфекции [Raper SE et al., 2003]. У трех других пациентов, лечившихся от синдрома иммунодефицита, развились симптомы, похожие на лейкемию [Hacein-Bey-Abina S et al., 2002], и один из них умер. С тех пор другие исследовательские группы лечили подобных пациентов с аналогичными терапевтическими результатами, без каких-либо побочных эффектов [Cavazzana-Calvo M. Fischer A, 2004]. В этом случае исследование направлено на лечение пациентов с переносчиками, которые нельзя использовать для повышения работоспособности.
Люди, которые пытаются неестественно повысить уровень ЭПО, также увеличивают вероятность сердечных приступов или острых эпизодов в мозге. Увеличение количества красных кровяных телец также определяет увеличение плотности крови, что может вызвать образование тромбов, поэтому не ошибочно думать, что побочные реакции, наблюдаемые у пациентов, также могут возникать у здоровых спортсменов [Lage JM et al., 2002].
Если бы ЭПО был введен генетически, уровень и продолжительность выработки эритропоэтина были бы менее контролируемыми, так что гематокрит почти бесконечно увеличивался до патологического уровня.
Предполагается, что лечение IGF-1 может привести к росту гормонозависимых опухолей.
Поэтому критически важно, чтобы использование фармакогенетически выбранных векторов имело хорошо известную и контролируемую модель экспрессии генов.
Точные методы обнаружения генетического допинга еще не установлены, в том числе потому, что ДНК, которая передается с помощью генной терапии, имеет человеческое происхождение и поэтому не отличается от ДНК спортсменов, которые ее используют.
Мышечная терапия ограничивается местом инъекции или тканями в непосредственной близости, поэтому большинство генных технологий в мышцах не может быть обнаружено с помощью классического антидопингового анализа образцов мочи или крови; биопсия мышцы была бы необходима, но она слишком инвазивна, чтобы ее можно было рассматривать как нормальное средство допинг-контроля.
Многие формы генетического допинга не требуют прямого введения генов в желаемый орган; ген ЭПО, например, может быть введен в любую часть тела и локально продуцирует белок, который затем поступит в кровоток. Поиск места инъекции ЭПО был бы подобен поиску иголки в стоге сена.
Однако в большинстве случаев генетический допинг приводит к введению гена, который является точной копией эндогенного и способен давать белок, полностью идентичный эндогенному в его посттрансляционных модификациях.
В недавней публикации указывается, что можно обнаружить разницу между врожденным белком и продуктом генной терапии на основе различного паттерна гликозилирования в разных типах клеток; еще неизвестно, относится ли это к всем типам генетического допинга [ Lasne F et al., 2004].
Государственные органы и спортивные организации, включая Международный олимпийский комитет, осудили допинг еще в 1960-х годах. Последние достижения в области биопрепаратов существенно повлияют на характер лекарств, назначаемых пациентам, а также изменят выбор лекарств, используемых для лечения. улучшить спортивные результаты.
Генная терапия разрешена исключительно для клинических испытаний продуктов соматической генной терапии на людях, строго исключая возможность рассмотрения любого типа генной терапии зародышевой линии человека как возможного.
Запрещение генетического допинга Всемирным антидопинговым агентством (ВАДА) и международными спортивными федерациями обеспечивает прочную основу для его искоренения в спорте, но также будет зависеть от того, как различные правила воспринимаются спортсменами.
У большинства спортсменов недостаточно знаний, чтобы полностью понять потенциальный негативный эффект генетического допинга. По этой причине очень важно, чтобы они и их вспомогательный персонал были хорошо обучены, чтобы предотвратить его использование. Спортсмены также должны знать о рисках, связанных с использованием генетического допинга при использовании в неконтролируемых учреждениях, без каких-либо компромиссов. безграничный потенциал официальной генной терапии для лечения серьезных патологий.
Фармацевтическая промышленность хорошо осведомлена о возможностях и рисках, связанных с использованием генетического допинга, и хочет сотрудничать в разработке исследований для обнаружения генных продуктов, присутствующих в ее лекарствах. Желательно, чтобы он подписал кодекс, в котором он обязуется никогда не производить и не продавать по какой-либо причине генетические продукты для нетерапевтического использования.
Было опрошено ограниченное количество людей из различных дисциплин науки и спорта, чтобы получить «представление о понятии и возможном влиянии генетического допинга на них. Среди опрошенных было три спортивных врача, фармацевт, четыре человека. элитные спортсмены и пять ученых из академических кругов и фармацевтической промышленности; вот вопросы:
- Вам знаком термин генетический допинг?
- Как вы думаете, что означает этот термин?
- Вы верите в улучшение результатов за счет использования генетического допинга?
- Каковы, по вашему мнению, риски для здоровья, связанные с использованием генетического допинга?
- Применяется ли генетический допинг уже или он будет только в будущем?
- Легко ли будет выявить генетический допинг?
Из различных ответов ясно, что люди, не относящиеся к научному сообществу, мало осведомлены об использовании этой терапии; распространены опасения, что генная терапия может повлиять на потомство или вызвать рак. Генетический допинг будет сложным, а профилактические меры - трудными. с другой стороны, все настаивают на том, что генетический допинг будет использоваться спортсменами, как только он станет доступен, и что это произойдет в ближайшие несколько лет.
Профессионалы, окружающие элитных спортсменов, очень обеспокоены возможным использованием генетического допинга и рекомендуют обучать своих спортсменов и их медицинский вспомогательный персонал в поддержку разработки профилактических исследований по антидопинговым измерениям. Эти профессионалы убеждены, что проблема применения генетического допинга у спортсменов возникнет в ближайшие несколько лет, и что его выявление будет довольно сложно.
Мир спорта рано или поздно столкнется с феноменом генетического допинга; точное количество лет, которое должно пройти, чтобы это произошло, оценить сложно, но можно предположить, что это произойдет в ближайшее время, в ближайшие несколько лет (Олимпийские игры 2008 года в Пекине или, самое позднее, в последующие).
От езды на велосипеде до тяжелой атлетики, от плавания до футбола и катания на лыжах - все виды спорта могут выиграть от генетических манипуляций: просто выберите ген, который улучшает требуемый тип работоспособности! [Бернардини Б., 2006].