Структура и функции
Гемоглобин - это содержащийся в эритроцитах металлопротеин, ответственный за перенос кислорода в кровоток. Фактически, кислород лишь умеренно растворяется в воде; следовательно, количества растворенного в крови (менее 2% от общего количества) недостаточно для удовлетворения метаболических потребностей тканей. Таким образом, очевидна потребность в конкретном носителе.
В кровотоке кислород не может связываться напрямую и обратимо с белками, как это происходит с металлами, такими как медь и железо. Неудивительно, что в центре каждой белковой субъединицы гемоглобина, завернутой в белковую оболочку, мы находим так называемые протезы. группа EME, с металлическим сердцем, представленным атомом железа в степени окисления Fe2 + (восстановленное состояние), который обратимо связывает кислород.
Анализ крови
- Нормальный уровень гемоглобина в крови: 13-17 г / 100 мл.
У женщин значения в среднем на 5-10% ниже, чем у мужчин.
Возможные причины высокого гемоглобина
- Полицитемии
- Длительное пребывание на высоте
- Хронические заболевания легких
- Сердечное заболевание
- Кровяной допинг (использование эритропоэтина и производных или веществ, имитирующих их действие)
Возможные причины низкого гемоглобина
- Анемии
- Дефицит железа (дефицит железа)
- Обильное кровотечение
- Карциномы
- Беременность
- Талассемии
- Ожоги
Таким образом, содержание кислорода в крови определяется суммированием небольшого количества, растворенного в плазме, с фракцией, связанной с железом гемоглобина.
Более 98% кислорода, присутствующего в крови, связано с гемоглобином, который, в свою очередь, циркулирует в кровотоке, выделяемом внутри эритроцитов. Таким образом, без гемоглобина эритроциты не могут выполнять свою функцию переносчиков кислорода в крови.
Учитывая центральную роль этого металла, синтез гемоглобина требует адекватного поступления железа с пищей. Около 70% железа, присутствующего в организме, фактически содержится в гемовых группах гемоглобина.
Гемоглобин состоит из 4 субъединиц, структурно очень похожих на миоглобин *.
* В то время как гемоглобин переносит кислород из легких в ткани, миоглобин переносит кислород, выделяемый гемоглобином, в различные клеточные органеллы, которые его используют (например, митохондрии).

Гемоглобин - это большой и сложный металлопротеин, характеризующийся четырьмя глобулярными белковыми цепями, соответственно обернутыми вокруг гемовой группы, содержащей Fe2 +.
Таким образом, для каждой молекулы гемоглобина мы находим четыре гемовые группы, заключенные в соответствующую глобулярную белковую цепь. Поскольку в каждой молекуле гемоглобина четыре атома железа, каждая молекула гемоглобина может связывать с собой четыре атома кислорода в соответствии с обратимой реакцией:
Hb + 4O2 ← → Hb (O2) 4
Как известно большинству, задача гемоглобина состоит в том, чтобы забирать кислород в легкие, отдавать его нуждающимся в нем клеткам, забирать у них углекислый газ и выпускать его в легкие, где снова начинается хилос.
Во время прохождения крови по капиллярам легочных альвеол гемоглобин связывает с собой кислород, который впоследствии выделяется в ткани периферического кровообращения. Этот обмен происходит потому, что связи кислорода с железом группы EME лабильны и чувствительны ко многим факторам, наиболее важным из которых является напряжение или парциальное давление кислорода.
Связывание кислорода с гемоглобином и эффект Бора
В легких давление кислорода в плазме увеличивается из-за диффузии газа из альвеол в кровь (↑ PO2); это увеличение заставляет гемоглобин активно связываться с кислородом; противоположное происходит в периферических тканях, где концентрация растворенного кислорода в крови уменьшается (↓ PO2), а парциальное давление углекислого газа увеличивается (↑ CO2); это заставляет гемоглобин выделять кислород и заряжаться CO2. Максимально упрощая концепцию, чем больше углекислого газа присутствует в крови, тем меньше кислорода остается связанным с гемоглобином.
Хотя количество кислорода, физически растворенного в крови, очень мало, поэтому он играет фундаментальную роль. Фактически, это количество сильно влияет на прочность связи между кислородом и гемоглобином (а также представляет собой «важную контрольную величину при регулировании легочной вентиляции»).
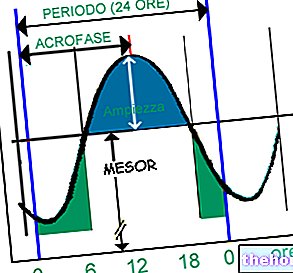
Обобщая все с помощью графика, количество кислорода, связанного с гемоглобином, растет по отношению к pO2 по сигмовидной кривой:

Тот факт, что область плату настолько велика, создает важный запас прочности при максимальном насыщении гемоглобина во время прохождения в легкие. Хотя pO2 на альвеолярном уровне обычно равно 100 мм рт. даже при парциальном давлении кислорода, равном 70 мм рт. ст. (типичное явление некоторых заболеваний или пребывания на большой высоте), процент насыщенного гемоглобина остается близким к 100%.
В области максимального наклона, когда парциальное давление кислорода падает ниже 40 мм рт. Ст., Способность гемоглобина связывать кислород резко падает.
В условиях покоя РО2 во внутриклеточных жидкостях составляет примерно 40 мм рт. в этом месте, в соответствии с законами газов, растворенный в плазме кислород диффундирует к более бедным тканям O2, пересекая капиллярную мембрану. Следовательно, давление O2 в плазме еще больше падает, и это способствует высвобождению кислорода из гемоглобина. . С другой стороны, при интенсивных физических нагрузках давление кислорода в тканях падает до 15 мм рт. Ст. Или менее, в результате чего кровь сильно обедняется кислородом.
Как уже было сказано, в условиях покоя важное количество оксигенированного гемоглобина покидает ткани, оставаясь доступным в случае необходимости (например, для борьбы с внезапным повышением метаболизма в некоторых клетках).
Сплошная линия, показанная на изображении выше, называется кривой диссоциации гемоглобина; обычно его определяют in vitro при pH 7,4 и температуре 37 ° C.
Эффект Бора влияет как на поступление O2 на уровне легких, так и на его высвобождение на уровне тканей.
Там, где больше растворенного диоксида углерода в форме бикарбоната, гемоглобин легче выделяет кислород и заряжается диоксидом углерода (в форме бикарбоната).

Тот же эффект дает подкисление крови: чем больше снижается pH крови, тем меньше кислорода остается связанным с гемоглобином; неудивительно, что в крови углекислый газ растворяется в основном в форме угольной кислоты, которая диссоциирует.



В честь его первооткрывателя влияние pH или углекислого газа на диссоциацию кислорода известно как эффект Бора.
Как и ожидалось, в кислой среде гемоглобин легче выделяет кислород, в то время как в основной среде связь с кислородом сильнее.

К другим факторам, способным изменять сродство гемоглобина к кислороду, относятся температура. В частности, сродство гемоглобина к кислороду уменьшается с повышением температуры тела. Это особенно полезно в зимние и весенние месяцы, поскольку температура легочной крови (при контакте с воздух внешней среды) ниже, чем в тканях, поэтому выделение кислорода облегчается.

2.3 дифосфоглицерат является промежуточным звеном в гликолизе, который влияет на сродство гемоглобина к кислороду. Если его концентрация в красных кровяных тельцах увеличивается, сродство гемоглобина к кислороду уменьшается, что способствует высвобождению кислорода к тканям. Неудивительно, что концентрации эритроцитов 2,3 дифосфоглицерата повышаются, например, при анемии, сердечно-легочной недостаточности и во время пребывания на большой высоте.
В целом эффект 2,3-бисфосфоглицерата относительно медленный, особенно по сравнению с быстрой реакцией на изменения pH, температуры и парциального давления углекислого газа.

Эффект Бора очень важен при интенсивной мышечной работе; в таких условиях, фактически, в тканях, наиболее подверженных стрессу, происходит локальное повышение температуры и давления углекислого газа, следовательно, кислотности крови. Как объяснялось выше, все это способствует высвобождению кислорода к тканям, сдвигая кривую диссоциации гемоглобина вправо.