Под редакцией доктора Лоренцо Боскариола
" вторая часть
Ремонт второго намерения
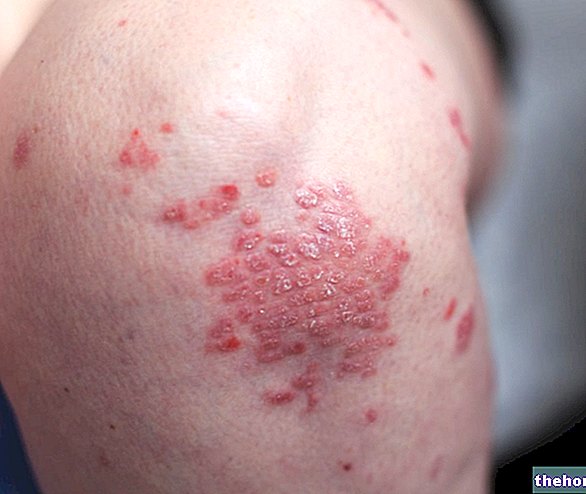
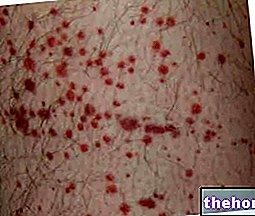
В случае ран, характеризующихся значительной потерей вещества или инфицированными и, следовательно, осложненными «серьезной воспалительной реакцией», регенерация паренхиматозных клеток сама по себе недостаточна для восстановления целостности ткани на ранних стадиях заживления, но необходима массивное образование грануляционной ткани, задачей которой является заполнение большой площади потери вещества между двумя краями (не затронутыми) раны. В этом случае реэпителизация более продолжительна и менее эффективна, а отложение соединительных волокон более заметно. Рубцовые исходы ран, которые подвергаются заживлению вторичным натяжением, продиктованы внутренними характеристиками репаративного процесса, который требует интенсивной активности воспалительных клеток (для удаления некротических клеток, остатков тканей, «обширного сгустка») и «обширного сгустка». формирование грануляционной ткани с одновременным образованием ECM и новообразованных ваз. Обычно чем больше протяженность грануляционной ткани, тем больше простирается соединительный рубец. Важным явлением процесса восстановления, также присутствующим при заживлении посредством первого натяжения, но гораздо более значимым при вторичном натяжении, является сокращение раны, тем более важным, чем более обширная потеря ткани и образование грануляционной ткани. . Сокращение может быть очень заметным, в некоторых случаях даже уменьшая поверхность поражения до 10% от первоначальной, и происходит как из-за обезвоживания сгустка (особенно поверхности, подверженной воздействию воздуха), так и из-за действия миофибробласты.
Эволюция репаративного процесса
«Созревание» рубца - это процесс, который продолжается далеко за пределами морфологически более заметной фазы замещения грануляционной ткани и реэпителизации. Соединительная ткань, откладываемая в фазе реабсорбции грануляционной ткани, претерпевает «обширную реорганизацию, которая изменяет ее биохимические и механические свойства. Сначала фибробласты откладывают коллаген типа III, который затем заменяется коллагеном типа I. часов, а затем снижается. По всей видимости, существует обратная зависимость между скоростью прекращения синтеза гиалуроновой кислоты и разрастанием фиброзной ткани рубца, что означает, что быстрое ингибирование синтеза кислоты гиалуроновой кислоты, по-видимому, предрасполагает к образованию более обширного фиброзного рубца. . Отложение эластичных волокон слабое. Механическое сопротивление заживляемой раны, очевидно, ниже, чем у здоровой ткани. По оценкам, курс в первую неделю составляет около 10%, затем возрастает до 70-80%. 3 месяца Сопротивление не восстанавливается m оригинальная экканика.
Клеточная биология заживления ран.
Заживление ран - это скоординированный и сложный процесс, в котором участвуют все фундаментальные биохимические и молекулярные процессы, участвующие в росте и дифференцировке клеток. После того, как начальная гемостатическая и острая воспалительная фазы исчерпаны, естественное течение раны определяется хроническим воспалительным инфильтратом (резорбция и ремоделирование ткани), отложением ВКМ и ангиогенезом. Эти поздние фазы имеют свое происхождение и основание «находиться» в наборе медиаторов, вырабатываемых локально во время образования сгустка и в ходе раннего острого воспалительного инфильтрата.
Тромбоциты содержат два типа секреторных гранул, плотные тела и альфа-гранулы, в которых накапливаются многочисленные агенты, способные стимулировать или модулировать воспаление (серотонин, гистамин, гепарин, адреналин, нуклеотиды), а также факторы роста, такие как фактор роста тромбоцитов. (PDGF) и трансформирующий фактор роста-b (TGF-b). Активация тромбоцитов в сгустке приводит к взрывному и сильно локализованному высвобождению этих медиаторов, которые, таким образом, действуют не только на лейкоциты, в свою очередь заключенные в сгусток, но и на окружающие субэндотелиальные соединительные клетки. Эти медиаторы, помимо их хорошо известной активности в отношении сосудистого тонуса и проницаемости, стимулируют набор и активацию полиморфно-ядерных гранулоцитов, фибробластов, моноцитов / макрофагов и дендритных клеток в этой временной последовательности. Также фибринопептиды, продуцируемые действием тромбина на фибриноген (и сам тромбин) стимулируют хемотаксис лейкоцитов, продукцию радикальных видов и экзоцитоз секреторных гранул, в то время как активированный фактор Хагемана действует на кининоген и систему комплемента, производя вазоактивные кинины и активированный комплемент (C5a, C3a и т. д.). Лейкоцитарный инфильтрат при восстановлении тканей становится очень важным источником не только дополнительных предварительно сформированных или неосинтезированных химических медиаторов, но также факторов роста и ферментов, способных разрушать ECM.
Помимо ферментов с деградационной активностью, содержащихся в определенных азурофильных или третичных гранулах (эластаза, коллагеназа и желатиназа), нейтрофилы также продуцируют цитокины и хемокины, такие как фактор некроза опухоли-a, TNF-a), интерлейкины-1a и 1b (IL -1a и IL-1b), хемотаксические белки для моноцитов 1 и 2 (хемиотаксический белок моноцитов, MCP-1 и MCP-2), воспалительный белок макрофагов (MIP 1a). Есть признаки того, что нейтрофилы могут также продуцировать факторы роста для соединительных клеток и кератиноцитов, такие как факторы роста фибробластов 1, 2 и 5 (фактор роста фибробластов, FGF, 1, 2 и 5, уровень экспрессии увеличивается примерно в 10 раз в восстанавливаемой ткани. ) и FGF-7, также известный как фактор роста кератиноцитов (KGF), уровень экспрессии которого увеличивается в 160 раз.
Фаза репарации дополнительно усиливается за счет прибытия макрофагов. Эти клетки являются даже более важным источником факторов роста и клеточной модуляции, чем нейтрофилы. В частности, в дополнение к IL-1 и TNF-a макрофаги продуцируют TGF-b, PDGF. , инсулиноподобный фактор роста (IGF). Из этих факторов роста TGF-b, вероятно, является наиболее важным в процессе восстановления из-за его мощного воздействия почти на все клетки, участвующие в процессе восстановления, а не только на фибробласты. Фактически, TGF-b в низких концентрациях оказывает сильное ингибирующее действие на рост клеток, в то время как при высоких концентрациях он стимулирует пролиферацию. Он также оказывает мощный хемотический эффект на клетки, которые принимают участие в построении грануляционной ткани, стимулирует отложение ECM и ингибирует его деградацию. В конечном итоге, TGF-b становится одним из наиболее важных факторов, способствующих образованию d Эль грануляционная ткань.
Другим ключевым фактором в формировании грануляционной ткани являются матричные металлопротеазы (ММП), набор ферментов, разрушающих соединительную ткань, играющих ключевую роль в воспалении и восстановлении тканей, источником которых являются макрофаги. В процессе заживления ран эти ферменты подвергаются действию тщательный процесс активации / деактивации, чтобы позволить ремоделирование новообразованной ткани и образование рубца. Различные факторы роста, цитокины и гормоны стимулируют (PDGF, IL-1, TNF-a) или ингибируют (TGF-b, кортикостероиды) синтез ММП путем модуляции экспрессии их генов, в то время как плазмин вызывает протеолитическую активацию предшественников (проММП). После активации ММП быстро ингибируются тканевыми ингибиторами протеаз (тканевые ингибиторы металлопротеаз, ТИМП). Макрофаги также являются основным источником активатора плазминог eno (активатор плазминогена урокиназного типа, uPA), фактор, ответственный за активацию плазминогена, который, в свою очередь, является повсеместным предшественником плазмина, наиболее важного фибринолитического фермента. С секрецией uPA начинается процесс деградации сгустка и начинается фаза образования грануляционной ткани.
Еще статьи на тему «Заживление ран - эволюция восстановительного процесса»
- Заживление ран - Первичное намеренное лечение
- Лечение раны
- Заживление ран - фаза рубца