Активные ингредиенты: леналидомид
Ревлимид 2,5 мг в твердых капсулах
Ревлимид в твердых капсулах 5 мг
Ревлимид в твердых капсулах 7,5 мг
Ревлимид в твердых капсулах 10 мг
Ревлимид в твердых капсулах 15 мг
Ревлимид в твердых капсулах 20 мг
Ревлимид в твердых капсулах 25 мг
Почему используется Ревлимид? Для чего это?
Ревлимид содержит действующее вещество «леналидомид». Это лекарство относится к группе лекарств, влияющих на работу иммунной системы.
Ревлимид применяется у взрослых при:
- Множественная миелома
- Миелодиспластические синдромы
- Лимфома из клеток мантии
Множественная миелома и Ревлимид
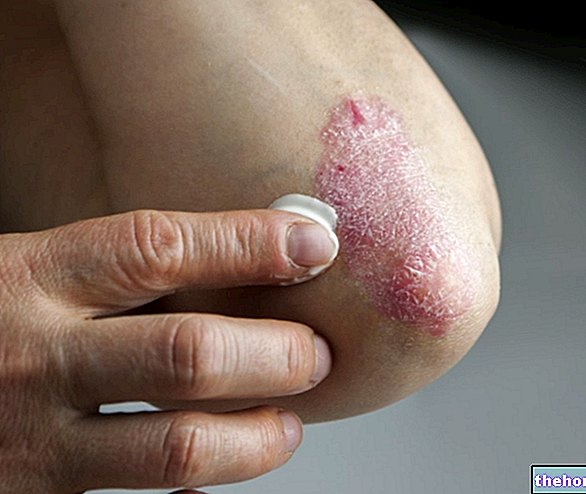
Множественная миелома - это тип рака, который поражает определенный тип белых кровяных телец, называемых плазматическими клетками. Эти клетки накапливаются в костном мозге и неконтролируемо делятся. Это может повредить кости и почки.
Множественная миелома обычно неизлечима. Однако признаки и симптомы могут значительно уменьшиться или исчезнуть на некоторое время. Этот результат называется «ответ».
При лечении множественной миеломы Ревлимид используется в сочетании с другими лекарствами.
Ревлимид у пациентов с впервые выявленной множественной миеломой
Ревлимид используется только у недавно диагностированных пациентов, когда им не может быть пересадка костного мозга.
Если вам 75 лет и старше или у вас есть проблемы с почками от умеренной до тяжелой, ваш врач внимательно осмотрит вас перед началом лечения.
У недавно диагностированных пациентов есть два типа лечения:
- Ревлимид вместе с противовоспалительным лекарством под названием «дексаметазон».
- Ревлимид вместе с химиотерапевтическим препаратом под названием «мелфалан» и иммунодепрессантом под названием «преднизон». Вы примете эти другие лекарства в начале лечения, а затем продолжите принимать только Ревлимид.
Ревлимид у пациентов с множественной миеломой, которые ранее получали хотя бы один другой вид лечения
- Ревлимид принимается вместе с противовоспалительным лекарством под названием «дексаметазон».
Ревлимид может предотвратить ухудшение признаков и симптомов множественной миеломы. Также было показано, что он задерживает возвращение множественной миеломы после лечения.
Миелодиспластические синдромы и Ревлимид
Миелодиспластические синдромы (МДС) - это совокупность множества различных заболеваний крови и костного мозга. Клетки крови становятся ненормальными и не функционируют должным образом. У пациентов могут быть различные признаки и симптомы, включая низкое количество эритроцитов (анемия), необходимость переливания крови и риск заражения.
Ревлимид сам по себе используется для лечения взрослых пациентов с диагнозом миелодиспластический синдром, у которых есть все следующие состояния:
- если вам необходимо регулярное переливание крови для лечения низкого уровня эритроцитов («трансфузионно-зависимая анемия»)
- если у вас есть «аномалия клеток костного мозга, называемая« изолированной цитогенетической аномалией с делецией 5q ». Это означает, что ваше тело не производит достаточно здоровых клеток крови
- если другие использованные ранее методы лечения непригодны или недостаточно эффективны.
Ревлимид может увеличить количество здоровых эритроцитов, производимых организмом, за счет уменьшения количества аномальных клеток:
- Это может уменьшить количество необходимых переливаний крови. Переливание может не потребоваться.
Лимфома из клеток мантии и Ревлимид
Лимфома из клеток мантии - это рак лимфатической ткани (части иммунной системы), который поражает тип белых кровяных телец, называемых B-лимфоцитами. При лимфоме из клеток мантии B-лимфоциты бесконтрольно растут и накапливаются в лимфатической ткани, костном мозге. , или кровь.
Ревлимид используется самостоятельно для лечения взрослых пациентов, у которых ранее диагностирована нелеченая лимфома из мантийных клеток.
Как работает Ревлимид
Ревлимид действует на иммунную систему организма и непосредственно на опухоль несколькими способами:
- остановка развития раковых клеток
- остановка роста кровеносных сосудов, несущих кровь к опухолевым клеткам
- стимулируя часть иммунной системы атаковать раковые клетки.
Противопоказания Когда нельзя применять Ревлимид
Не принимайте Ревлимид
- Если вы беременны или думаете, что беременны, или если вы планируете забеременеть, поскольку ожидается, что Ревлимид будет вредным для будущего ребенка (см. Раздел 2, «Предупреждения и меры предосторожности» и «Беременность и кормление грудью»). .
- Если есть вероятность, что вы можете забеременеть, если вы не примете все необходимые меры для предотвращения беременности (см. Разделы 2 «Предупреждения и меры предосторожности» и «Беременность и кормление грудью»). Если есть вероятность, что вы можете забеременеть, ваш врач будет отмечать и подтверждать каждым рецептом, что были приняты необходимые меры для предотвращения беременности.
- Если у вас аллергия на леналидомид или какие-либо другие ингредиенты этого лекарства (перечислены в разделе 6). Если вы считаете, что у вас аллергия, посоветуйтесь с врачом.
Если что-либо из этого относится к вам, не принимайте Ревлимид. В случае сомнений проконсультируйтесь с врачом.
Меры предосторожности при использовании Что следует знать перед приемом Ревлимида
Сообщите своему врачу перед началом лечения, если:
- когда-либо были эпизоды образования тромбов, так как риск образования тромбов в венах и артериях увеличивается во время лечения
- есть какие-либо признаки инфекции, такие как кашель или лихорадка
- у вас проблемы с почками - ваш врач может изменить дозу Ревлимида
- у вас был сердечный приступ, у вас был тромб, или если вы курите, у вас высокое кровяное давление или высокий уровень холестерина
- имеет высокую опухолевую нагрузку по всему телу, в том числе в костном мозге. Это может привести к заболеванию, при котором опухоли разрушаются и вызывают необычный уровень химических веществ в крови, что может привести к почечной недостаточности (это заболевание называется "опухолью"). синдром лизиса »)
- были аллергические реакции во время лечения талидомидом, такие как сыпь, зуд, отек, головокружение или затрудненное дыхание
Если что-либо из этого относится к вам, сообщите об этом врачу перед началом лечения.
Если у вас миелодиспластические синдромы, у вас больше шансов заболеть более запущенным заболеванием, которое называется острым миелоидным лейкозом (ОМЛ). Кроме того, неизвестна роль ревлимида в вероятности развития ОМЛ. Ваш врач может попросить вас пройти несколько тестов, чтобы проверить признаки, которые могли бы более точно предсказать вероятность развития ОМЛ во время лечения ревлимидом.
Анализ и контроль
У вас будут регулярные анализы крови до и во время лечения Ревлимидом, поскольку Ревлимид может вызвать уменьшение количества клеток крови, которые защищают вас от инфекций (лейкоцитов), и тех, которые помогают свертыванию крови (тромбоциты). Ваш врач попросит вас сдать анализ крови:
- до лечения
- каждую неделю в течение первых 8 недель лечения (для пациентов с лимфомой из мантийных клеток это будет происходить каждые 2 недели в циклах 3 и 4, а затем в начале каждого цикла)
- в дальнейшем не реже одного раза в месяц.
Ваш врач может проверить наличие изменений на вашей коже, таких как красные пятна или сыпь.
Ваш врач может решить скорректировать дозу Ревлимида или прекратить лечение в зависимости от результатов анализов крови и вашего общего состояния. Если вам недавно поставили диагноз, ваш врач может также оценить лечение с учетом вашего возраста и любых других состояний, которые могут уже присутствовать.
Донорство крови
Не следует сдавать кровь во время терапии леналидомидом и в течение одной недели после прекращения лечения.
Дети и подростки
Ревлимид не рекомендуется применять детям и подросткам до 18 лет.
Взаимодействие Какие лекарства или продукты могут изменить действие Ревлимида
Сообщите своему врачу или медсестре, если вы принимаете, недавно принимали или собираетесь принимать какие-либо другие лекарства, в том числе лекарства, отпускаемые без рецепта, и лекарства на травах. Это связано с тем, что Ревлимид может влиять на действие некоторых других лекарств, а некоторые другие лекарства могут влиять на действие Ревлимида. работает.
В частности, сообщите своему врачу или медсестре, если вы принимаете какие-либо из следующих лекарств:
- некоторые лекарства, используемые для предотвращения беременности, такие как оральные контрацептивы, поскольку они могут больше не быть эффективными
- некоторые лекарства, используемые при сердечных заболеваниях, например дигоксин
- некоторые лекарства, используемые для разжижения крови, такие как варфарин
Предупреждения Важно знать, что:
Беременность, кормление грудью и контрацепция - информация для мужчин и женщин
Беременность
Для женщин, принимающих Ревлимид
- Вы не должны принимать Ревлимид, если вы беременны, поскольку ожидается, что это лекарство будет вредным для будущего ребенка.
- Во время лечения Ревлимидом нельзя забеременеть. Если есть вероятность беременности, необходимо использовать эффективные методы контрацепции (см. Раздел «Контрацепция»).
- Если вы забеременели во время приема Ревлимида, вы должны немедленно прекратить лечение и сообщить своему врачу.
Для мужчин, принимающих Ревлимид
- Если ваш партнер забеременеет, пока вы принимаете Ревлимид, немедленно сообщите об этом своему врачу. Также рекомендуется, чтобы ваш партнер обратился к врачу.
- Кроме того, необходимо использовать эффективные методы контрацепции (см. Раздел «Контрацепция»).
Время кормления
Вы не должны кормить грудью, принимая Ревлимид, так как неизвестно, проникает ли это лекарство в грудное молоко.
Контрацепция
Для женщин, принимающих Ревлимид
Перед началом лечения вам следует спросить своего врача, есть ли у вас возможность забеременеть, даже если вы думаете, что это маловероятно.
Если есть вероятность, что вы забеременеете
- вам необходимо будет проходить тесты на беременность под наблюдением врача (перед каждым лечением, каждые 4 недели во время лечения и через 4 недели после окончания лечения), за исключением случаев, когда было подтверждено, что маточные трубы были разрезаны и закрыты, чтобы предотвратить яйца от попадания в матку (стерилизация путем завязывания трубок)
- вы должны использовать эффективные методы контрацепции в течение 4 недель до начала лечения, во время лечения и до 4 недель после прекращения лечения.Ваш врач посоветует вам подходящие методы контрацепции.
Для мужчин, принимающих Ревлимид
Ревлимид переходит в сперму человека. Если есть вероятность, что ваша партнерша беременна или забеременеет, и она не использует эффективные методы контрацепции, вам следует использовать презервативы во время лечения и в течение одной недели после его окончания, даже если вам сделали вазэктомию.
Вождение и использование машин
Не садитесь за руль и не работайте с механизмами, если вы чувствуете головокружение, усталость, сонливость, головокружение или нечеткость зрения.
Ревлимид содержит лактозу
Ревлимид содержит лактозу. Если врач сказал вам, что у вас «непереносимость некоторых сахаров», обратитесь к врачу, прежде чем принимать Ревлимид.
Доза, способ и время приема Как применять Ревлимид: Дозировка
Ревлимид должен назначаться медицинскими работниками, имеющими опыт лечения множественной миеломы или миелодиспластических синдромов и лимфомы из клеток мантии.
- При лечении множественной миеломы Ревлимид принимают в сочетании с другими лекарствами (см. Раздел 1 «Что такое Ревлимид и для чего он применяется»).
- При использовании для лечения миелодиспластических синдромов и лимфомы из клеток мантии принимают только Ревлимид.
Всегда принимайте Ревлимид отдельно или Ревлимид в сочетании с другими лекарствами, всегда точно следуя указаниям врача. В случае сомнений проконсультируйтесь с врачом или фармацевтом.
Если вы принимаете Ревлимид в сочетании с другими лекарствами, пожалуйста, ознакомьтесь с листками-вкладышами этих лекарств для получения дополнительной информации об их использовании и эффектах.
Цикл лечения
- Ревлимид и лекарства, которые необходимо принимать в сочетании с Ревлимидом, принимают в течение нескольких дней в течение 4 недель (28 дней).
- Каждый 28-дневный период называется «циклом лечения».
- В зависимости от дня менструации вы примете одно или несколько лекарств. Однако через несколько дней вы не будете принимать никаких лекарств.
- После завершения каждого 28-дневного цикла в следующие 28 дней должен начаться новый «цикл».
Доза ревлимида, которую нужно принимать
Перед началом лечения врач скажет вам:
- доза Ревлимида, чтобы принять
- доза других лекарств, которые следует принимать в сочетании с Ревлимидом, если это предписано
- в какие дни цикла лечения принимать каждое лекарство.
Врачи могут заметить изменения на коже, такие как красные пятна или сыпь.
Ваш врач также может принять решение об изменении дозы Ревлимида или других лекарств во время лечения на основании результатов анализов крови и вашего общего состояния (см. Раздел 2 «Что вам нужно знать перед приемом Ревлимида»).
Как и когда принимать Ревлимид
- Капсулы следует проглатывать целиком, желательно, запивая водой.
- Не разламывайте, не открывайте и не разжевывайте капсулы.
- Капсулы можно принимать во время еды или без нее.
- Принимать Ревлимид следует в назначенные дни примерно в одно и то же время.
Чтобы вынуть капсулу из блистера, надавите только на одну сторону капсулы, проталкивая ее через алюминиевую фольгу.Не нажимайте на центр капсулы, иначе она может сломаться.
Продолжительность лечения Ревлимидом
Ревлимид принимают курсами по 28 дней каждый (см. «Цикл лечения» выше). Вам следует продолжать курсы лечения до тех пор, пока врач не скажет вам о прекращении лечения.
Если вы забыли принять Ревлимид
Если вы забыли принять Ревлимид в обычное время e
- прошло менее 12 часов: немедленно примите капсулу
- прошло более 12 часов: не принимать забытую капсулу, а принять следующую капсулу на следующий день в обычное время.
Если у вас есть дополнительные вопросы по применению этого лекарства, обратитесь к врачу или фармацевту.
Передозировка Что делать, если вы приняли слишком много Ревлимида
Если вы приняли больше Ревлимида, чем было рекомендовано, немедленно сообщите об этом врачу.
Побочные эффекты Каковы побочные эффекты Ревлимида
Как и все лекарства, это лекарство может вызывать побочные эффекты, хотя они возникают не у всех.
Серьезные побочные эффекты, которые могут возникать более чем у 1 из 10 человек.
Ревлимид может уменьшить количество лейкоцитов, которые борются с инфекциями, и клеток крови, которые способствуют свертыванию крови (тромбоциты), что может привести к нарушениям свертываемости крови, например. кровотечение из носа и синяки. Ревлимид также может вызывать образование тромбов в венах (тромбоз).
Поэтому вам следует немедленно обратиться за медицинской помощью, если у вас возникнут какие-либо из следующих побочных эффектов:
- лихорадка, озноб, боль в горле, кашель, язвы во рту или любые другие симптомы инфекции (в том числе в кровотоке (сепсис))
- кровотечение или синяк при отсутствии ран
- боль в груди или ногах
- сбивчивое дыхание.
Если вы испытываете какие-либо из перечисленных выше побочных эффектов, немедленно сообщите об этом своему врачу.
Другие побочные эффекты перечислены ниже.
Важно отметить, что у небольшого числа пациентов могут развиться другие типы рака, и возможно, что этот риск может увеличиться при лечении Ревлимидом; Поэтому ваш врач должен тщательно взвесить пользу и риск при назначении вам Ревлимида.
Очень частые побочные эффекты могут возникать более чем у 1 из 10 человек:
- Снижение количества эритроцитов (анемия), что может вызвать усталость и слабость
- Запор, диарея, тошнота, покраснение кожи, сыпь, рвота, мышечные спазмы, мышечные боли, боли в костях, боли в суставах, усталость, общий отек, включая отек рук и ног
- Симптомы лихорадки и гриппа, включая лихорадку, мышечную боль, головную боль, боль в ухе и озноб
- Онемение, покалывание или жжение на коже, боль в руках или ногах, головокружение, тремор, изменение вкуса
- Боль в груди с иррадиацией в руки, шею, челюсть, спину или живот с ощущением потоотделения и одышки, тошнотой или рвотой, которые могут быть симптомами сердечного приступа (инфаркта миокарда)
- Снижение аппетита
- Низкий уровень калия в крови
- Боль в ногах (которая может быть симптомом тромбоза), боль в груди или одышка (что может быть симптомом тромбов в легких, называемых тромбоэмболией легочной артерии)
- Любые инфекции
- Инфекция легких и верхних дыхательных путей, одышка
- Затуманенное зрение
- Затуманенное зрение (катаракта)
- Проблемы с почками
- Изменения белка в крови, которые могут вызвать отек артерий (васкулит)
- Повышение уровня сахара в крови (диабет)
- Головная боль
- Сухая кожа
- Боль в животе
- Изменение настроения, трудности со сном
Общие побочные эффекты могут возникать у 1 из 10 человек:
- Инфекция носовых пазух
- Кровотечение из десен, желудка или кишечника
- Повышенная боль, размер опухоли, покраснение вокруг опухоли
- Повышение или снижение артериального давления, медленное, учащенное или нерегулярное сердцебиение
- Потемнение кожи
- Сыпь, растрескивание кожи, шелушение или шелушение
- Крапивница, зуд, повышенное потоотделение, обезвоживание
- Боль во рту с язвами, сухость во рту, затрудненное глотание
- Боль в животе
- Выработка мочи намного больше или меньше, чем обычно (что может быть признаком почечной недостаточности), кровь в моче
- Одышка, особенно в положении лежа (что может быть признаком сердечной недостаточности).
- Трудности с эрекцией
- Инсульт, обморок
- Мышечная слабость
- Припухлость суставов
- Изменения гормона щитовидной железы в крови, низкий уровень кальция, фосфата или магния в крови
- Депрессия
- Глухота
- Аномальные функциональные пробы печени
- Нарушения равновесия, затруднения движений
- Звон в ушах (тиннитус)
- Железная перегрузка
- Жажда
- Путаница
- Зубная боль
- Потеря веса.
Необычные побочные эффекты могут возникать у 1 из 100 человек:
- Кровоизлияние внутри черепа
- Проблемы с кровообращением
- Потеря зрения
- Потеря полового влечения (либидо)
- Обильный поток мочи с болью и слабостью в костях, что может быть симптомом заболевания почек (синдром Фанкони).
- Боль в желудке, вздутие живота или диарея, которые могут быть симптомами воспаления толстой кишки (так называемого колита или тифлита).
- Выработка гораздо большего или меньшего количества мочи, чем обычно, что может быть симптомом заболевания почек (называемого некрозом почечных канальцев).
- Изменение цвета кожи, чувствительность к солнечному свету
- Некоторые виды рака кожи
- Крапивница, сыпь, отек глаз, рта или лица, затрудненное дыхание или зуд, которые могут быть симптомами аллергической реакции.
Редкие побочные эффекты могут возникать у 1 из 1000 человек:
- Тяжелая аллергическая реакция, которая может начаться в виде сыпи на одном участке, но распространяется с обширной потерей кожи по всему телу (синдром Стивенса-Джонсона и / или токсический эпидермальный некролиз).
- Синдром лизиса опухоли - метаболические осложнения, которые могут возникнуть во время лечения опухоли, а иногда и без лечения. Эти осложнения вызваны продуктами распада умирающих раковых клеток и могут включать следующие осложнения: изменение гематологических параметров; высокие значения калия, фосфора и мочевой кислоты; и низкие уровни кальция, которые, как следствие, приводят к изменениям функции почек, частоте сердечных сокращений, судорогам и, иногда, к смерти.
Частота неизвестна: частота не может быть оценена на основе имеющихся данных:
- Внезапная или легкая, но усиливающаяся боль в верхней части живота и / или спины, которая сохраняется в течение нескольких дней, возможно, с тошнотой, рвотой, лихорадкой и учащенным пульсом. Эти симптомы могут быть связаны с воспалением поджелудочной железы.
- Свистящее дыхание, одышка или сухой кашель, которые могут быть симптомами, вызванными воспалением легочной ткани.
- Желтоватое изменение цвета кожи, слизистых оболочек или глаз (желтуха), светлый стул, темная моча, кожный зуд, сыпь, боль или вздутие живота. Это могут быть симптомы поражения печени (заболевание печени).
- Наблюдались редкие случаи разрушения мышц (боль, слабость или отек мышц), которые могут вызвать проблемы с почками (рабдомиолиз), некоторые из которых, когда Ревлимид назначается со статином (тип препарата, снижающего уровень холестерина).
- Заболевание, поражающее кожу и вызываемое воспалением мелких кровеносных сосудов, с болями в суставах и лихорадкой (лейкоцитокластический васкулит).
- Ухудшение стенок желудка или кишечника, которое может вызвать очень серьезные инфекции. Сообщите своему врачу, если у вас сильная боль в животе, жар, тошнота, рвота, кровь в стуле или изменения в привычках кишечника.
Сообщение о побочных эффектах
Если у вас появятся какие-либо побочные эффекты, поговорите со своим врачом, фармацевтом или медсестрой. Это включает в себя любые возможные побочные эффекты, не перечисленные в этой брошюре. Вы также можете сообщить о побочных эффектах напрямую через национальную систему отчетности, перечисленную в Приложении V. Побочные эффекты, которым вы можете помочь предоставьте дополнительную информацию о безопасности этого лекарства.
Срок действия и удержание
- Храните это лекарство в недоступном для детей месте.
- Не используйте это лекарство по истечении срока годности, указанного на блистере и коробке после «EXP». Срок годности относится к последнему дню этого месяца.
- Это лекарство не требует особых условий хранения.
- Не используйте это лекарство, если вы заметили повреждения или признаки вскрытия упаковки.
- Не выбрасывайте лекарства в сточные воды или бытовые отходы. Спросите своего фармацевта, как утилизировать лекарства, которые вы больше не используете. Это поможет защитить окружающую среду.
Срок »> Другая информация
Что содержит Ревлимид
Твердые капсулы Ревлимид 2,5 мг:
- Действующее вещество - леналидомид. Каждая капсула содержит 2,5 мг леналидомида.
- Остальные ингредиенты:
- содержимое капсулы: безводная лактоза, микрокристаллическая целлюлоза, кроскармеллоза натрия и стеарат магния.
- оболочка капсулы: желатин, диоксид титана (E171), индигокармин (E132) и желтый оксид железа (E172)
- буквенные чернила: шеллак, пропиленгликоль, гидроксид калия и черный оксид железа (E172).
Ревлимид в твердых капсулах 5 мг:
- Действующее вещество - леналидомид. Каждая капсула содержит 5 мг леналидомида.
- Остальные ингредиенты:
- содержимое капсулы: безводная лактоза, микрокристаллическая целлюлоза, кроскармеллоза натрия и стеарат магния.
- оболочка капсулы: желатин и диоксид титана (E171)
- печатные чернила: шеллак, пропиленгликоль, гидроксид калия и черный оксид железа (E172).
Твердые капсулы Ревлимид 7,5 мг:
- Действующее вещество - леналидомид. Каждая капсула содержит 7,5 мг леналидомида.
- Остальные ингредиенты:
- содержимое капсулы: безводная лактоза, микрокристаллическая целлюлоза, кроскармеллоза натрия и стеарат магния.
- оболочка капсулы: желатин, диоксид титана (E171), желтый оксид железа (E172)
- буквенные чернила: шеллак, пропиленгликоль, гидроксид калия и черный оксид железа (E172).
Ревлимид в твердых капсулах 10 мг:
- Действующее вещество - леналидомид. Каждая капсула содержит 10 мг леналидомида.
- Остальные ингредиенты:
- содержимое капсулы: безводная лактоза, микрокристаллическая целлюлоза, кроскармеллоза натрия и стеарат магния.
- препарат капсулы: желатин, диоксид титана (E171), индигокармин (E132) и желтый оксид железа (E172)
- буквенные чернила: шеллак, пропиленгликоль, гидроксид калия и черный оксид железа (E172).
Твердые капсулы Ревлимид 15 мг:
- Действующее вещество - леналидомид. Каждая капсула содержит 15 мг леналидомида.
- Остальные ингредиенты:
- содержимое капсулы: безводная лактоза, микрокристаллическая целлюлоза, кроскармеллоза натрия и стеарат магния.
- оболочка капсулы: желатин, диоксид титана (E171) и индигокармин (E132)
- буквенные чернила: шеллак, пропиленгликоль, гидроксид калия и черный оксид железа (E172).
Ревлимид в твердых капсулах 20 мг:
- Действующее вещество - леналидомид. Каждая капсула содержит 20 мг леналидомида.
- Остальные ингредиенты:
- содержимое капсулы: безводная лактоза, микрокристаллическая целлюлоза, кроскармеллоза натрия и стеарат магния.
- оболочка капсулы: желатин, диоксид титана (E171), индигокармин (E132) и желтый оксид железа (E172)
- печатные чернила: шеллак, пропиленгликоль, гидроксид калия и черный оксид железа (E172).
Ревлимид в твердых капсулах 25 мг:
- Действующее вещество - леналидомид. Каждая капсула содержит 25 мг леналидомида.
- Остальные ингредиенты:
- содержимое капсулы: безводная лактоза, микрокристаллическая целлюлоза, кроскармеллоза натрия и стеарат магния.
- оболочка капсулы: желатин и диоксид титана (E171)
- печатные чернила: шеллак, пропиленгликоль, гидроксид калия и черный оксид железа (E172).
Как выглядит Ревлимид и что содержится в упаковке
Твердые капсулы Ревлимид 2,5 мг имеют сине-зеленый / белый цвет с маркировкой «REV 2,5 мг».
Капсулы поставляются в упаковках, по одному или по три блистера в каждой. Каждый блистер содержит семь капсул, всего 7 или 21 капсула в упаковке.
Твердые капсулы Ревлимид 5 мг белого цвета с маркировкой «REV 5 мг».
Капсулы поставляются в упаковках, по одному или по три блистера в каждой. Каждый блистер содержит семь капсул, всего 7 или 21 капсула в упаковке.
Твердые капсулы Revlimid 7,5 мг бледно-желтого / белого цвета с маркировкой «REV 7,5 мг».
Капсулы поставляются в упаковках по три блистера в каждой. Каждый блистер содержит семь капсул, всего 21 капсула в упаковке.
Твердые капсулы Ревлимид 10 мг имеют сине-зеленый / светло-желтый цвет с маркировкой «REV 10 мг».
Капсулы поставляются в упаковках по три блистера в каждой. Каждый блистер содержит семь капсул, всего 21 капсула в упаковке.
Твердые капсулы Ревлимид 15 мг светло-голубого / белого цвета с маркировкой «REV 15 мг».
Капсулы поставляются в упаковках по три блистера в каждой. Каждый блистер содержит семь капсул, всего 21 капсула в упаковке.
Твердые капсулы Ревлимид 20 мг имеют сине-зеленый / голубой цвет, с маркировкой «REV 20 мг».
Капсулы поставляются в упаковках по три блистера в каждой. Каждый блистер содержит семь капсул, всего 21 капсула в упаковке.
Твердые капсулы Ревлимид 25 мг белого цвета с маркировкой «REV 25 мг».
Капсулы поставляются в упаковках по три блистера в каждой. Каждый блистер содержит семь капсул, всего 21 капсула в упаковке.
Листовка с исходным кодом: AIFA (Итальянское агентство по лекарственным средствам). Контент опубликован в январе 2016 года. Представленная информация может быть устаревшей.
Чтобы иметь доступ к самой последней версии, рекомендуется зайти на сайт AIFA (Итальянское агентство по лекарственным средствам). Заявление об ограничении ответственности и полезная информация.
01.0 НАИМЕНОВАНИЕ ЛЕКАРСТВЕННОГО ПРЕПАРАТА -
REVLIMID ЖЕСТКИЕ КАПСУЛЫ 10 МГ
▼ Лекарственный препарат, подлежащий дополнительному мониторингу. Это позволит быстро идентифицировать новую информацию по безопасности. Медицинских работников просят сообщать о любых предполагаемых побочных реакциях. См. Раздел 4.8 для получения информации о том, как сообщать о побочных реакциях.
02.0 КАЧЕСТВЕННЫЙ И КОЛИЧЕСТВЕННЫЙ СОСТАВ -
Каждая капсула содержит 10 мг леналидомида.
Вспомогательные вещества с известными эффектами:
Каждая капсула содержит 294 мг безводной лактозы.
Полный список вспомогательных веществ см. В разделе 6.1.
03.0 ФАРМАЦЕВТИЧЕСКАЯ ФОРМА -
Твердая капсула.
Капсулы сине-зеленые / светло-желтые, размером 0,21,7 мм, с маркировкой «REV 10 мг».
04.0 КЛИНИЧЕСКАЯ ИНФОРМАЦИЯ -
04.1 Терапевтические показания -
Множественная миелома
Ревлимид показан для лечения взрослых пациентов с ранее нелеченой множественной миеломой, которые не подходят для трансплантации (см. Раздел 4.2).
Ревлимид в комбинации с дексаметазоном показан для лечения взрослых пациентов с множественной миеломой, которые получали по крайней мере одну предыдущую терапию.
Миелодиспластические синдромы
Ревлимид показан для лечения пациентов с трансфузионно-зависимой анемией из-за миелодиспластических синдромов (МДС) низкого или среднего риска, связанных с изолированной цитогенетической аномалией с делецией 5q, когда другие варианты лечения недостаточны или неадекватны.
Лимфома из клеток мантии
Ревлимид показан для лечения взрослых пациентов с рецидивирующей или рефрактерной лимфомой из мантийных клеток (см. Разделы 4.4 и 5.1).
04.2 Дозировка и способ применения -
Лечение ревлимидом должно проходить под наблюдением врача, имеющего опыт лечения рака (см. Раздел 4.4, кариотип).
Дозировка
Недавно диагностированная множественная миелома
Леналидомид в комбинации с дексаметазоном до прогрессирования заболевания у лиц, не принимающих участие в лечении. подходит для трансплантации
Лечение леналидомидом не следует начинать, если абсолютное количество нейтрофилов (Абсолютный
Количество нейтрофилов, АНК) есть
Рекомендуемая доза
Рекомендуемая начальная доза леналидомида составляет 25 мг перорально один раз в сутки в дни 1-21 повторных 28-дневных циклов. Рекомендуемая доза дексаметазона составляет 40 мг перорально один раз в день в 1, 8, 15 и 22 дни повторных 28-дневных циклов. Пациенты могут продолжать терапию леналидомидом и дексаметазоном до прогрессирования заболевания или развития непереносимости.
Дозировка может быть продолжена или изменена на основании клинических и лабораторных данных (см. Раздел 4.4). Для пациентов старше 75 лет начальная доза дексаметазона составляет 20 мг / день в дни 1, 8, 15 и 22 каждого 28-дневного цикла лечения. Рекомендуемая доза леналидомида для пациентов с умеренной почечной недостаточностью составляет 10 мг один раз в сутки.
Рекомендуемая корректировка дозы во время лечения и при возобновлении лечения
Как обобщено в следующих таблицах, корректировка дозы рекомендуется для лечения тромбоцитопении и нейтропении 3 или 4 степени или для лечения любых других токсичностей 3 или 4 степени, которые предположительно связаны с леналидомидом.
• Уровни снижения дозы
• Тромбоцитопения
a Если наблюдается ограничивающая дозу токсичность (Токсичность, ограничивающая дозу, DLT)> на 15-й день цикла дозирование леналидомида будет прекращено, по крайней мере, на оставшуюся часть текущего 28-дневного цикла.
• Нейтропения
В случае нейтропении врач должен рассмотреть возможность использования факторов роста при ведении пациента.
Если доза леналидомида была снижена из-за гематологической DLT, доза леналидомида может быть повторно введена на следующем более высоком уровне дозы (до начальной дозы) по усмотрению лечащего врача, если продолжение терапии леналидомидом / дексаметазоном привело к улучшению костей. функция костного мозга (отсутствие DLT в течение как минимум 2 последовательных циклов и ANC ≥ 1500 / мкл при количестве тромбоцитов ≥ 100000 / мкл, в начале нового цикла при текущей дозе).
Леналидомид в комбинации с мелфаланом и преднизоном с последующей поддерживающей монотерапией при пациенты, не подходящие для трансплантации
Лечение леналидомидом не следует начинать, если ДРП
Рекомендуемая доза
Рекомендуемая начальная доза: леналидомид 10 мг / сут перорально в дни 1-21 повторных 28-дневных циклов до 9 циклов, мелфалан 0,18 мг / кг перорально в дни 1-4 повторных циклов 28 дней, преднизон 2 мг / сут. кг перорально в дни 1-4 повторных 28-дневных циклов. Пациенты, завершившие 9 циклов или неспособные завершить комбинированную терапию из-за непереносимости, должны получать монотерапию леналидомидом в дозе 10 мг / день перорально в дни 1-21 повторных циклов.28 дней до прогрессирования заболевания. Дозировка может быть продолжена или изменена на основании клинических и лабораторных данных (см. Раздел 4.4).
Рекомендуемая корректировка дозы во время лечения и при возобновлении лечения
Как показано в таблицах ниже, корректировка дозы рекомендуется для лечения тромбоцитопении или нейтропении 3 или 4 степени или для лечения любой другой токсичности 3 или 4 степени, которая, как считается, связана с леналидомидом.
• Уровни снижения дозы
Если нейтропения является единственным проявлением токсичности при любой дозировке, добавьте гранулоцитарный колониестимулирующий фактор (G-CSF) и поддерживайте дозировку леналидомида..
• Тромбоцитопения
• Нейтропения
a Если субъект не получал терапию G-CSF, начните терапию G-CSF. В день 1 следующего цикла продолжайте прием GCSF по мере необходимости и поддерживайте дозу мелфалана, если нейтропения была единственной DLT. В противном случае уменьшите один уровень дозы в начале следующего цикла.
В случае нейтропении следует рассмотреть возможность использования факторов роста при ведении пациента.
Множественная миелома, по крайней мере, при одном предшествующем лечении
Рекомендуемая доза
Рекомендуемая начальная доза составляет 25 мг леналидомида перорально один раз в день в дни 1-21 повторных 28-дневных циклов. Рекомендуемая доза дексаметазона составляет 40 мг перорально один раз в день в дни 1-4, 9-12 и 17-20 каждого 28-дневного цикла в течение первых 4 циклов терапии и 40 мг один раз в день в последующие дни. каждые 28 дней.
Дозировка может быть продолжена или изменена на основании клинических и лабораторных данных (см. Раздел 4.4). Врачи должны тщательно оценить дозировку дексаметазона для использования, принимая во внимание состояние пациента и статус болезни.
Лечение леналидомидом не следует начинать, если АНК представляет собой костный мозг плазматическими клетками, если количество тромбоцитов составляет
Рекомендуемая корректировка дозы во время лечения и при возобновлении лечения
Как показано в следующих таблицах, корректировка дозы рекомендуется для лечения нейтропении или тромбоцитопении 3 или 4 степени или для лечения любой токсичности 3 или 4 степени, которая, как считается, связана с леналидомидом.
• Уровни снижения дозы
• Тромбоцитопения
• Нейтропения
В случае нейтропении следует рассмотреть возможность использования факторов роста при ведении пациента.
Миелодиспластические синдромы
Лечение леналидомидом не следует начинать, если ДРП
Рекомендуемая доза
Рекомендуемая начальная доза составляет 10 мг леналидомида перорально один раз в сутки в дни 1-21 повторных 28-дневных циклов. Дозировка может быть продолжена или изменена на основании клинических и лабораторных данных (см. Раздел 4.4).
Рекомендуемая корректировка дозы во время лечения и при возобновлении лечения
Как показано в следующих таблицах, корректировка дозы рекомендуется для лечения нейтропении или тромбоцитопении 3 или 4 степени или для лечения любой токсичности 3 или 4 степени, которая, как считается, связана с леналидомидом.
• Уровни снижения дозы
Для пациентов, начинающих с дозы 10 мг и испытывающих тромбоцитопению или нейтропению:
• Тромбоцитопения
• Нейтропения
Суспензия леналидомида
Пациентам, у которых нет хотя бы легкой эритроидной реакции в течение 4 месяцев после начала терапии, что демонстрируется снижением потребности в переливании крови не менее чем на 50% или, если они не получают переливания, увеличением гемоглобина на 1 г / дл, следует прекратить прием леналидомида. лечение.
Лимфома из клеток мантии
Рекомендуемая доза
Рекомендуемая начальная доза составляет 25 мг леналидомида перорально один раз в день в дни 1-21 повторных 28-дневных циклов.
Анализ продолжается или изменяется на основании клинических и лабораторных данных (см. Раздел 4.4).
Рекомендуемая корректировка дозы во время лечения и при возобновлении лечения
Как указано в таблицах ниже, корректировка дозы рекомендуется для лечения нейтропении или тромбоцитопении 3 или 4 степени, а также для лечения любой токсичности 3 или 4 степени, которая, как считается, связана с леналидомидом.
• Уровни снижения дозы
1 - В странах, где доступны капсулы 2,5 мг.
• Тромбоцитопения
• Нейтропения
• Реакция обострения опухоли
Лечение леналидомидом можно продолжить у пациентов с Реакция опухолевой вспышкиВыходное пособие 1 или 2 степени без перерывов или изменений по усмотрению врача. Пациентам с СКР 3 или 4 степени лечения леналидомидом следует воздерживаться до тех пор, пока СКР не снизится до ≤ 1 степени; Для лечения симптомов пациентов можно лечить в соответствии с рекомендациями по СКР 1 и 2 степени (см. Раздел 4.4).
Все пациенты
В случае других токсических эффектов 3 или 4 степени, которые, как считается, связаны с леналидомидом, лечение следует прекратить и возобновить со следующей более низкой дозой только тогда, когда токсичность снизилась до ≤ 2 степени по усмотрению врача.
Прекращение или прекращение приема леналидомида следует рассматривать в случае кожной сыпи 2 или 3 степени. Лечение леналидомидом следует прекратить в случае ангионевротического отека, сыпи 4 степени, эксфолиативной или буллезной сыпи или при подозрении на сыпь Стивенса-Джонсона (SSJ) или токсическое эпидермальное поражение. некролиз (NET), и его не следует возобновлять после отмены из-за этих реакций.
Особые группы населения
Педиатрическая популяция
Ревлимид не следует применять детям и подросткам от рождения до 18 лет из соображений безопасности (см. Раздел 4.4).
Пожилые пациенты
Доступные в настоящее время фармакокинетические данные описаны в разделе 5.2. Леналидомид использовался в клинических исследованиях у пациентов с множественной миеломой в возрасте до 91 года, у пациентов с миелодиспластическими синдромами до 95 лет и у пациентов с лимфомой из мантийных клеток до 88 лет (см. Раздел 5.1).
У пациентов с впервые диагностированной множественной миеломой в возрасте 75 лет и старше, получавших леналидомид, наблюдалась более высокая частота серьезных побочных реакций и побочных реакций, приводящих к прекращению лечения (см. Раздел 4.4). Пациенты с впервые диагностированной множественной миеломой в возрасте 75 лет и старше должны тщательно оценивать, прежде чем рассматривать вопрос о лечении (см. раздел 4.4).
• Недавно диагностированная множественная миелома.
Для пациентов старше 75 лет, получавших леналидомид в комбинации с дексаметазоном, начальная доза дексаметазона составляет 20 мг / день в дни 1, 8, 15 и 22 каждого 28-дневного цикла лечения.
Для пациентов старше 75 лет, принимающих леналидомид в сочетании с мелфаланом и преднизоном, корректировка дозы не предлагается.
В клинических испытаниях недавно диагностированной множественной миеломы у пациентов, не подходящих для трансплантации, комбинированная терапия леналидомидом переносилась хуже у пациентов старше 75 лет, чем у более молодого населения. Среди этих пациентов процент прекративших лечение из-за непереносимости (нежелательные явления 3 или 4 степени и серьезные нежелательные явления) был выше, чем у пациентов в возрасте
• Множественная миелома, ранее лечившаяся по крайней мере с одной терапией.
Процент пациентов с множественной миеломой в возрасте 65 лет и старше существенно не отличался между группами леналидомид / дексаметазон и плацебо / дексаметазон. В целом, никаких различий в безопасности и эффективности между этими пациентами и более молодыми пациентами не наблюдалось, хотя нельзя исключать большую предрасположенность пожилых пациентов.
• Миелодиспластические синдромы
Для пациентов с миелодиспластическими синдромами, получавших леналидомид, не наблюдалось общей разницы в безопасности и эффективности между пациентами старше 65 лет и более молодыми пациентами.
• Лимфома из клеток мантии.
Для пациентов с лимфомой из клеток мантии, получавших леналидомид, не наблюдалось общей разницы в безопасности и эффективности между пациентами в возрасте 65 лет и старше и пациентами в возрасте до 65 лет.
Поскольку у пожилых пациентов чаще наблюдается нарушение функции почек, следует соблюдать особую осторожность при выборе дозы и в качестве меры предосторожности проводить мониторинг функции почек.
Пациенты с почечной недостаточностью
Леналидомид в основном выводится через почки; у пациентов с более высокой степенью почечной недостаточности переносимость лечения может измениться (см. раздел 4.4). Особое внимание следует уделять выбору дозировки и рекомендуется контролировать функцию почек.
Коррекция дозы не требуется у пациентов с легкой почечной недостаточностью и множественной миеломой, миелодиспластическими синдромами или лимфомой из клеток мантии. У пациентов с умеренной или тяжелой почечной недостаточностью или терминальной стадией почечной недостаточности в начале терапии и на протяжении всего курса лечения рекомендуются следующие корректировки дозы. Нет опыта клинических исследований фазы III у пациентов с терминальной стадией почечной недостаточности (ТПН). ) (Диализ CLcr).
• Множественная миелома
1 Дозу можно увеличить до 15 мг один раз в день после 2 циклов, если пациент не реагирует на лечение, но переносит лекарство.
2 В странах, где доступны капсулы 7,5 мг.
• Миелодиспластические синдромы
* Рекомендуемые уровни снижения дозы во время лечения и после возобновления лечения для лечения нейтропении или тромбоцитопении 3 или 4 степени или другой токсичности 3 или 4 степени, которая считается связанной с леналидомидом, как описано выше.
• Лимфома из клеток мантии
1 Дозу можно увеличить до 15 мг один раз в день после 2 циклов, если пациент не реагирует на лечение, но переносит лекарство.
2 В странах, где доступны капсулы 7,5 мг.
После начала терапии леналидомидом последующее изменение дозы леналидомида у пациентов с нарушением функции почек должно основываться на переносимости лечения для отдельного пациента, как описано выше.
Пациенты с нарушением функции печени
Леналидомид официально не изучался у пациентов с печеночной недостаточностью, и нет конкретных рекомендаций по дозировке.
Способ применения
Устное употребление.
Капсулы Ревлимид следует принимать в назначенные дни, примерно в одно и то же время. Капсулы нельзя открывать, ломать или жевать.Капсулы следует глотать целиком, желательно с водой, с едой или без. Пациент может принять пропущенную дозу, если с запланированного времени приема прошло менее 12 часов. Если, с другой стороны, прошло более 12 часов, пациент не должен принимать пропущенную дозу, а дождаться обычного время следующего дня для приема следующей дозы.
Рекомендуется надавить только на одну сторону капсулы, чтобы удалить ее из блистера, что снижает риск ее деформации или разрушения.
04.3 Противопоказания -
• Повышенная чувствительность к активному веществу или любому из вспомогательных веществ, перечисленных в разделе 6.1.
• Беременные женщины.
• Женщины детородного возраста, если не выполняются все условия Программы профилактики беременности (см. Разделы 4.4 и 4.6).
04.4 Особые предупреждения и соответствующие меры предосторожности при использовании -
Меры предосторожности при беременности
Леналидомид структурно связан с талидомидом, активным веществом с известным тератогенным действием у людей, которое вызывает серьезные опасные для жизни врожденные пороки развития. Леналидомид вызывает пороки развития у обезьян, аналогичные тем, которые описаны для талидомида (см. Разделы 4.6 и 5.3). Тератогенный эффект леналидомида ожидается у людей во время беременности.
Условия Программы предотвращения беременности должны соблюдаться для всех пациенток, если нет убедительных доказательств того, что пациентка не может забеременеть.
Критерии установления того, что женщина не детородна
Пациентка-женщина или партнер пациента-мужчины считаются способными к зачатию, если она не соответствует хотя бы одному из следующих критериев:
• Возраст ≥ 50 лет и естественная аменорея * ≥ 1 года
• Преждевременная недостаточность яичников, подтвержденная гинекологом.
• Предыдущая двусторонняя сальпингоофорэктомия или гистерэктомия
• Генотип XY, синдром Тернера, агенез матки.
* Аменорея после противоопухолевой терапии или во время кормления грудью не исключает возможности фертильности.
Ориентация
Леналидомид противопоказан женщинам детородного возраста, если не выполнены все следующие условия:
• Пациент осознает, что ожидается тератогенный риск для плода.
• Пациент осознает необходимость использования эффективных методов контрацепции без перерыва, за 4 недели до начала лечения, в течение всего курса лечения и до 4 недель после его окончания.
• Даже при наличии аменореи пациент детородного возраста должен соблюдать все рекомендации по эффективной контрацепции.
• Пациент должен уметь соблюдать эффективные меры контрацепции.
• Пациентка проинформирована и осведомлена о потенциальных последствиях беременности и о необходимости немедленного обращения за медицинской помощью, если существует риск беременности.
• Пациентка осознает необходимость начать лечение сразу после отпуска леналидомида после отрицательного результата теста на беременность.
• Пациентка осведомлена о необходимости и соглашается проходить тесты на беременность каждые 4 недели, за исключением случаев подтвержденной стерилизации путем перевязки маточных труб.
• Пациентка признает, что осознает риски и необходимые меры предосторожности, связанные с использованием леналидомида.
Для пациентов мужского пола, принимающих леналидомид, фармакокинетические исследования показали, что во время лечения леналидомид присутствует в сперме в крайне низких количествах и не обнаруживается в сперме здоровых субъектов через 3 дня после прекращения приема вещества (см. Параграф 5.2). В качестве меры предосторожности все пациенты мужского пола, принимающие леналидомид, должны соответствовать следующим условиям:
• Помните об ожидаемом тератогенном риске сексуальной активности с беременной женщиной или женщиной с детородным потенциалом.
• Помните о необходимости использования презервативов в случае полового акта с беременной или потенциально фертильной женщиной, которая не использует эффективную контрацепцию (даже если мужчине была сделана вазэктомия) во время лечения и в течение 1 недели после прерывания приема дозы и / или лечения. прекращение.
• Имейте в виду, что если партнерша забеременеет во время приема Ревлимида или вскоре после прекращения лечения Ревлимидом, они должны немедленно сообщить об этом врачу и направить партнера к специалисту или тератологу, который сможет оценить ситуацию и высказать свое мнение.
В случае с женщинами детородного возраста врач должен убедиться, что:
• Пациентка соответствует требованиям Программы предотвращения беременности, включая подтверждение того, что она имеет адекватный уровень понимания
• Пациент принял указанные выше условия.
Контрацепция
Женщины детородного возраста должны использовать эффективную контрацепцию в течение 4 недель до начала терапии, во время терапии и до 4 недель после терапии леналидомидом, а также в случае прерывания приема препарата, если только пациентка не обязуется соблюдать «абсолютное и непрерывное воздержание в течение месяца с подтверждением». по месяцам.Если эффективная противозачаточная терапия еще не была начата, пациента следует направить к врачу-специалисту, чтобы определить эффективный метод контрацепции.
Ниже приведены примеры адекватных методов контрацепции:
• Растение
• Внутриматочная система с высвобождением левоноргестрела (ВМС)
• Депо медроксипрогестерона ацетата
• Стерилизация маточных труб
• Половой акт только с партнером-мужчиной, которому сделана вазэктомия; вазэктомия должна быть подтверждена двумя отрицательными анализами спермы
• Таблетки, содержащие только прогестоген, для подавления овуляции (например, дезогестрел)
Из-за повышенного риска венозной тромбоэмболии у пациентов с множественной миеломой, принимающих леналидомид в комбинированных схемах, и в меньшей степени у пациентов с миелодиспластическими синдромами и лимфомой из мантийных клеток, принимающих только леналидомид, использование пероральных контрацептивов не рекомендуется. также раздел 4.5). Если пациентка в настоящее время принимает комбинированный пероральный контрацептив, ей следует заменить метод контрацепции на один из вышеперечисленных. Риск венозной тромбоэмболии сохраняется в течение 4-6 недель после отмены комбинированного перорального контрацептива. Эффективность противозачаточных стероидов может снижаться при одновременном лечении дексаметазоном (см. Раздел 4.5).
Внутриматочные имплантаты и системы, высвобождающие левоноргестрел, связаны с повышенным риском инфицирования при установке, а также с нерегулярным вагинальным кровотечением. Следует рассмотреть вопрос о профилактике антибиотиками, особенно у пациентов с нейтропенией.
Внутриматочные спирали с высвобождением меди обычно не рекомендуются из-за потенциального риска инфицирования с момента введения и из-за менструальной кровопотери, что может отрицательно сказаться на пациентах с нейтропенией или тромбоцитопенией.
Тест на беременность
В соответствии с местной практикой у пациенток с детородным потенциалом тесты на беременность с минимальной чувствительностью 25 мМЕ / мл должны проводиться под наблюдением врача, как описано ниже. Это обязательство также распространяется на пациентов детородного возраста, которые практикуют абсолютное и постоянное воздержание. В идеале тест на беременность, назначение и выдача лекарства должны происходить в один и тот же день. Леналидомид следует отпускать пациентам детородного возраста в течение 7 дней с даты назначения.
Перед началом лечения
После того, как пациентка использовала эффективную контрацепцию в течение как минимум 4 недель, следует провести тест на беременность под медицинским наблюдением во время консультации, на которой прописан леналидомид, или за 3 дня до визита к врачу. Перед началом лечения леналидомидом тест должен убедиться, что пациентка не беременна.
Последующее наблюдение и окончание лечения
Тест на беременность под медицинским наблюдением следует повторять каждые 4 недели, в том числе через 4 недели после окончания лечения, за исключением случаев подтвержденной стерилизации маточных труб. Эти тесты на беременность следует проводить в тот же день, что и по рецепту врача, или за 3 дня до его посещения.
Пациенты мужского пола
Во время лечения леналидомид присутствует в сперме в крайне низких количествах и не обнаруживается в сперме здоровых людей через 3 дня после отмены препарата (см. Раздел 5.2). В качестве меры предосторожности и с учетом особых групп пациентов с длительным периодом выведения, таких как пациенты с почечной недостаточностью, все пациенты мужского пола, принимающие леналидомид, должны использовать презервативы в течение всего периода лечения, при прекращении лечения. Доза и до одной недели после прекращения терапии, если ваша партнерша беременна или детородна и не использует эффективные средства контрацепции (даже если мужчине была сделана вазэктомия).
Дополнительные меры предосторожности при использовании
Пациенты должны быть проинструктированы никогда не давать это лекарство другим людям и возвращать неиспользованные капсулы фармацевту по окончании лечения.
Пациенты не должны сдавать кровь во время терапии леналидомидом и в течение как минимум одной недели после прекращения лечения.
Учебные материалы, ограничения по рецептам и отпуску
Чтобы помочь пациентам избежать воздействия леналидомида на плод, Держатель регистрационного удостоверения предоставит медицинскому персоналу образовательные материалы, чтобы усилить предупреждения об ожидаемой тератогенности леналидомида, дать рекомендации по контрацепции перед началом терапии и дать рекомендации относительно необходимости проведения теста на беременность. . Врач должен проинформировать пациентов мужского и женского пола о тератогенном риске и строгих мерах по предотвращению беременности, как указано в Программе предотвращения беременности, и предоставить пациентам соответствующий учебный буклет, карту пациента и / или аналогичный инструмент в соответствии с мерами, принятыми в национальный уровень. Национальная система контроля распределения была внедрена в сотрудничестве с каждым национальным компетентным органом. Эта система предусматривает использование карты пациента и / или аналогичного инструмента для контроля за назначением и отпуском, а также сбор подробных данных в отношении индикации, чтобы тщательно контролировать использование не по назначению В идеале, тест на беременность, выдача рецепта и выдача лекарства должны проводиться в один и тот же день.Леналидомид следует отпускать пациентам с детородным потенциалом в течение 7 дней с даты назначения и после отрицательного результата теста на беременность под медицинским наблюдением.
Дополнительные специальные предупреждения и меры предосторожности при использовании
Сердечно-сосудистые заболевания
Инфаркт миокарда
Случаи инфаркта миокарда наблюдались у пациентов, получавших леналидомид, особенно у пациентов с известными факторами риска, и в течение первых 12 месяцев при приеме в комбинации с дексаметазоном. Пациенты с известными факторами риска, включая пациентов с предшествующим тромбозом, должны находиться под тщательным наблюдением и должны быть приняты меры, чтобы попытаться свести к минимуму все изменяемые факторы риска (например, курение, артериальная гипертензия и гиперлипидемия).
Венозные и артериальные тромбоэмболические события
У пациентов с множественной миеломой комбинация леналидомида и дексаметазона связана с повышенным риском венозной тромбоэмболии (в основном тромбоза глубоких вен и тромбоэмболии легочной артерии) и артериальной тромбоэмболии (в основном инфаркта миокарда и цереброваскулярных событий). степень применения леналидомида в сочетании с мелфаланом и преднизоном при впервые выявленной множественной миеломе и в качестве монотерапии при миелодиспластических синдромах. См. разделы 4.5 и 4.8.
У пациентов с миелодиспластическими синдромами и лимфомой из клеток мантии лечение одним леналидомидом также было связано с риском венозной тромбоэмболии (в основном тромбоза глубоких вен и тромбоэмболии легочной артерии), но в меньшей степени, чем у пациентов с множественной миеломой - см. Разделы 4.5 и 4.8.
Поэтому за пациентами с известными факторами риска тромбоэмболии, включая перенесенный ранее тромбоз, следует внимательно наблюдать. Следует принять меры, чтобы попытаться свести к минимуму все поддающиеся изменению факторы риска (например, курение, гипертензию и гиперлипидемию). У этих пациентов одновременное введение эритропоэтических агентов или наличие в анамнезе тромбоэмболических явлений также может увеличить риск тромбоза. Поэтому пациентам с множественной миеломой, принимающим леналидомид и дексаметазон, рекомендуется применение эритропоэтических средств или других средств, которые могут повышать риск тромбоза, таких как, например, заместительная гормональная терапия. Если концентрация гемоглобина превышает 12 г / дл, применение эритропоэтических средств следует прекратить.
Пациенты и врачи должны осознавать необходимость обращать внимание на признаки и симптомы тромбоэмболии. Пациентам следует обратиться за медицинской помощью при появлении таких симптомов, как одышка, боль в груди, отек нижних или верхних конечностей. В профилактических целях следует рекомендовать прием антитромботических препаратов, особенно пациентам с дополнительными факторами риска тромботических заболеваний.Решение о применении профилактических антитромботических мер следует принимать после тщательного рассмотрения факторов риска для каждого отдельного пациента.
Если у пациента наблюдается какое-либо тромбоэмболическое событие, лечение следует прекратить и начать стандартную антикоагулянтную терапию. После стабилизации состояния пациента на антикоагулянтной терапии и исчезновения всех осложнений тромбоэмболического события лечение леналидомидом можно возобновить в исходной дозе после оценки соотношения польза-риск. Пациенту следует продолжить антикоагулянтную терапию во время лечения. Лечение леналидомидом.
Нейтропения и тромбоцитопения
Основные ограничивающие дозу токсические эффекты леналидомида включают нейтропению и тромбоцитопению. Чтобы отслеживать возможное возникновение цитопении, в течение первых 8 недель лечения следует проводить полный анализ крови, включая количество лейкоцитов, включая дифференциальное, количество тромбоцитов, гемоглобин и гематокрит, на исходном уровне один раз в неделю в течение первых 8 недель лечения. леналидомид, а затем - один раз в месяц.У пациентов с лимфомой из клеток мантии мониторинг следует проводить каждые 2 недели в циклах 3 и 4, а затем в начале каждого цикла. Может потребоваться снижение дозы (см. Раздел 4.2). В случае нейтропении врач должен рассмотреть возможность использования факторов роста при ведении пациента. Пациентам следует рекомендовать немедленно сообщать об эпизодах лихорадки. Рекомендуется соблюдать осторожность при одновременном применении леналидомида с другими миелосупрессивными средствами.
• Недавно диагностированная множественная миелома у пациентов, получавших леналидомид в сочетании с низкими дозами дексаметазона.
Нейтропения 4 степени наблюдалась в меньшей степени в группах лечения леналидомидом в сочетании с низкими дозами дексаметазона по сравнению с группой сравнения (8,5% в группах Rd [непрерывное лечение] и Rd18 [лечение в течение 18 циклов по четыре недели] по сравнению с 15 % в группе мелфалана / преднизона / талидомида, см. раздел 4.8). Эпизоды фебрильной нейтропении 4 степени соответствовали группе сравнения (0,6% у пациентов, получавших леналидомид / дексаметазон Rd и Rd18, по сравнению с 0,7% у пациентов в группе мелфалана / преднизона / талидомида, см. Раздел 4.8). Пациентам следует рекомендовать немедленно сообщать об эпизодах лихорадки, и может потребоваться снижение дозы (см. Раздел 4.2).
Тромбоцитопения 3 или 4 степени наблюдалась в меньшей степени в группах Rd и Rd18, чем в группе сравнения (8,1% против 11,1%, соответственно). Пациенты и врачи должны наблюдать признаки и симптомы кровотечения, включая петехии и носовое кровотечение, особенно у пациентов, проходящих сопутствующее лечение, которое может вызвать кровотечение (см. Раздел 4.8 «Нарушения свертываемости крови»).
• Недавно диагностированная множественная миелома у пациентов, получавших леналидомид в сочетании с мелфаланом и преднизоном.
В клинических исследованиях у пациентов с впервые диагностированной множественной миеломой комбинация леналидомида с мелфаланом и преднизоном ассоциировалась с более высокой частотой нейтропении 4 степени (34,1% у пациентов в группе мелфалана, преднизона и леналидомида с последующим лечением леналидомидом [MPR + R] мелфалан, преднизон и леналидомид с последующим приемом плацебо [MPR + p], по сравнению с 7,8% пациентов, получавших MPp + p; см. раздел 4.8). Эпизоды фебрильной нейтропении 4 степени наблюдались нечасто (1,7% у пациентов, получавших MPR + R / MPR + p по сравнению с 0,0% у пациентов, получавших MPp + p; см. Раздел 4.8).
У пациентов с множественной миеломой комбинация леналидомида с мелфаланом и преднизоном связана с более высокой частотой тромбоцитопении 3 и 4 степени (40,4% у пациентов, получавших MMR + R / MMR + p, по сравнению с 13,7% у пациентов, получавших MPp + p; см. Раздел 4.8). Пациенты и врачи должны быть внимательны в отношении признаков и симптомов кровотечения, включая петехии и носовое кровотечение, особенно у пациентов, одновременно принимающих лекарственные средства, повышающие предрасположенность к кровотечению (см. Раздел 4.8 «Нарушения свертываемости крови»).
• Множественная миелома, по крайней мере, при одном предшествующем лечении.
У пациентов с множественной миеломой, получавших по крайней мере одну предшествующую терапию, комбинация леналидомида и дексаметазона связана с более высокой частотой нейтропении 4 степени (5,1% пациентов, получавших леналидомид / дексаметазон, по сравнению с 0,6% пациентов, получавших плацебо / дексаметазон; см. раздел 4.8). Эпизоды фебрильной нейтропении 4 степени наблюдались нечасто (у 0,6% пациентов, получавших леналидомид / дексаметазон, по сравнению с 0,0% пациентов, получавших плацебо / дексаметазон; см. раздел 4.8) Пациентам следует рекомендовать немедленно сообщать об эпизодах лихорадки. Может потребоваться снижение дозы (см. Раздел 4.2) В случае нейтропении врачи должны рассмотреть возможность использования факторов роста при ведении пациентов.
У пациентов с множественной миеломой комбинация леналидомида и дексаметазона связана с более высокой частотой тромбоцитопении 3 и 4 степени (9,9% и 1,4% соответственно, более высокая частота тромбоцитопении 3 степени). 3 и 4 степени (9,9%) и 1,4% пациентов, получавших леналидомид / дексаметазон, соответственно, по сравнению с 2,3% и 0,0% пациентов, получавших плацебо / дексаметазон; см. раздел 4.8) Пациенты и врачи должны контролировать признаки и симптомы кровотечения, включая петехии и носовые кровотечения, особенно у пациентов одновременное лечение лекарственными средствами, которые могут вызвать кровотечение (см. раздел 4.8 «Нарушения свертываемости крови»).
• Миелодиспластические синдромы
У пациентов с миелодиспластическими синдромами лечение леналидомидом связано с более высокой частотой нейтропении и тромбоцитопении 3 и 4 степени, чем у пациентов, получавших плацебо (см. Раздел 4.8).
• Лимфома из клеток мантии.
У пациентов с лимфомой из мантийных клеток лечение леналидомидом связано с более высокой частотой нейтропении 3 и 4 степени, чем у пациентов контрольной группы (см. Раздел 4.8).
Инфекция с нейтропенией или без нее
Пациенты с множественной миеломой склонны к развитию инфекций, в том числе пневмонии. При лечении леналидомидом в сочетании с дексаметазоном наблюдалась более высокая частота инфекций, чем при лечении MPT. Инфекции ≥ 3 степени встречались на фоне нейтропении менее чем у трети пациентов. Пациенты с известными факторами риска инфекций должны находиться под тщательным наблюдением. Всем пациентам следует рекомендовать немедленно проконсультироваться со своим врачом при первых признаках инфекции (например, кашель, лихорадка и т. Д.), Чтобы можно было оперативно вмешаться для уменьшения тяжести.
Почечная недостаточность
Леналидомид в основном выводится через почки. Поэтому пациентам с почечной недостаточностью следует проявлять особую осторожность при выборе дозы и желательно контролировать функцию почек (см. Раздел 4.2).
Заболевания щитовидной железы
Наблюдались случаи гипотиреоза и гипертиреоза. Перед началом лечения рекомендуется оптимальный контроль сопутствующих заболеваний, влияющих на функцию щитовидной железы. Рекомендуется контролировать функцию щитовидной железы на исходном уровне и во время лечения.
Периферическая невропатия
Леналидомид структурно родственен талидомиду, который, как известно, вызывает тяжелую периферическую невропатию. При длительном применении леналидомида для лечения впервые диагностированной множественной миеломы не наблюдалось увеличения периферической нейропатии.
Реакция обострения опухоли и синдром лизиса опухоли
Поскольку леналидомид проявляет противоопухолевую активность, осложнения синдрома лизиса опухоли (Синдром лизиса опухоли, TLS). TLS и Реакция опухолевой вспышки (СКР) обычно наблюдались у пациентов с хроническим лимфолейкозом (ХЛЛ) и редко наблюдались у пациентов с лимфомами, получавших леналидомид. Сообщалось о случаях TLS с летальным исходом во время лечения леналидомидом.Пациенты с риском TLS и TFR - это пациенты с высокой опухолевой нагрузкой до лечения. Следует соблюдать осторожность при начале лечения леналидомидом у таких пациентов. Рекомендуется тщательно наблюдать за такими пациентами, особенно во время первого цикла или повышения дозы, и принимать соответствующие меры предосторожности. Были редкие сообщения о TLS у пациентов с ММ, получавших леналидомид, в то время как у пациентов с МДС лечили леналидомидом.
Масса опухоли
• Лимфома из клеток мантии.
Леналидомид не рекомендуется для лечения пациентов с высокой опухолевой нагрузкой, если доступны альтернативные варианты лечения.
Ранняя смерть
В исследовании MCL-002 наблюдалось общее очевидное увеличение ранней смерти (в течение 20 недель). Пациенты с высокой исходной опухолевой массой имеют более высокий риск ранней смерти: было 16/81 (20%) случаев ранней смерти в группе леналидомида и 2/28 (7%) случаев ранней смерти в группе контроля. К 52 неделям соответствующие цифры составили 32/81 (40%) и 6/28 (21%) (см. Раздел 5.1).
Неблагоприятные события
В исследовании MCL-002 во время цикла лечения 1 11/81 (14%) пациентов с высокой опухолевой нагрузкой были исключены из терапии леналидомидом по сравнению с 1/28 (4%) в контрольной группе. Основная причина прекращения лечения пациентов с высокой опухолевой нагрузкой во время цикла лечения 1 в группе леналидомида была связана с нежелательными явлениями, 7/11 (64%).
Поэтому пациентов с высокой опухолевой нагрузкой следует тщательно контролировать на предмет побочных реакций (см. Раздел 4.8), включая любые признаки Реакция опухолевой вспышки (СКР). Для корректировки дозы в случае СКР см. Раздел 4.2.
Повышенная масса опухоли определялась как минимум одно поражение диаметром ≥ 5 см или 3 поражения ≥ 3 см.
Реакция опухолевой вспышки
• Лимфома из клеток мантии.
Рекомендуется тщательный мониторинг и оценка СКР. Пациенты с повышенным MIPI (Международный прогностический индекс Mantel Cell Lymphoma) при диагнозе или заболевании, характеризующемся большими опухолевыми массами (по крайней мере, одно поражение с максимальным диаметром ≥ 7 см) на исходном уровне может иметь риск СКР. Там Реакция опухолевой вспышки может имитировать прогрессирование заболевания (PD). Пациенты в исследованиях MCL-002 и MCL-001, у которых наблюдалась СКР 1 и 2 степени, получали кортикостероиды, нестероидные противовоспалительные препараты (НПВП) и / или наркотические анальгетики для лечения симптомов СКР. Решение о применении терапевтических мер для СКР должно быть принято после «тщательной клинической оценки отдельного пациента (см. Раздел 4.2).
Аллергические реакции
Сообщалось о случаях аллергических реакций / реакций гиперчувствительности у пациентов, получавших леналидомид (см. Раздел 4.8). Рекомендуется тщательно контролировать пациентов, у которых в прошлом были аллергические реакции на талидомид, поскольку в литературе сообщалось о возможной перекрестной реакции между леналидомидом и талидомидом.
Тяжелые кожные реакции
Сообщалось о случаях SSJ и NET. Лечение леналидомидом следует прекратить в случае появления эксфолиативной или буллезной сыпи или при подозрении на SSJ или NET, и его не следует возобновлять после прекращения из-за этих реакций. Прерывание или прекращение приема леналидомида следует рассматривать при других формах кожных реакций в зависимости от их тяжести.Пациентам, у которых в анамнезе наблюдалась тяжелая сыпь, связанная с лечением талидомидом, не следует принимать леналидомид.
Непереносимость лактозы
Капсулы Ревлимид содержат лактозу. Пациентам с редкими наследственными проблемами непереносимости галактозы, дефицитом лактазы Лаппа или мальабсорбцией глюкозы-галактозы не следует принимать это лекарство.
Неиспользованные капсулы
Пациентам следует рекомендовать никогда не давать это лекарство другим людям и возвращать неиспользованные капсулы фармацевту по окончании лечения.
Вторая первичная опухоль
Увеличение вторичных первичных опухолей (Второе Начальное Злокачественность, SPM) у пациентов с миеломой, ранее получавших леналидомид / дексаметазон (3,98 на 100 человеко-лет), по сравнению с контрольной группой (1,38 на 100 человеко-лет). Неинвазивные SPM состоят из базальноклеточного или плоскоклеточного рака кожи.
Наиболее инвазивными ВПМ были солидные опухоли.
В клинических исследованиях у пациентов с впервые диагностированной множественной миеломой, не подходящих для трансплантации, у пациентов, получавших леналидомид в сочетании с мелфаланом и преднизоном до прогрессирования, наблюдалось 4,9-кратное увеличение частоты гематологического ПМС (случаи ОМЛ, МДС) (1,75 на 100 человеко-лет) по сравнению с мелфаланом в сочетании с преднизоном (0,36 на 100 человеко-лет).
У пациентов, получавших леналидомид (9 циклов) в сочетании с мелфаланом и преднизоном (1,57 на 100 человеко-лет), наблюдалось увеличение частоты встречаемости твердой SPM в 2,12 раза по сравнению с мелфаланом в сочетании с преднизоном (0,74 на 100 человеко-лет). человеко-лет).
У пациентов, получавших леналидомид в комбинации с дексаметазоном до прогрессирования или в течение 18 месяцев, частота гематологического ПМС (0,16 на 100 человеко-лет) не увеличивалась по сравнению с талидомидом в сочетании с мелфаланом и преднизоном (0,79 на 100 человеко-лет). .
У пациентов, получавших леналидомид в комбинации с дексаметазоном, до прогрессирования или в течение 18 месяцев (1,58 на 100 человеко-лет) наблюдалось повышение заболеваемости солидным ПМС в 1,3 раза по сравнению с талидомидом в комбинации с мелфаланом и преднизоном (1,19 на 100 человеко-лет). человеко-лет).
В клинических испытаниях у пациентов с впервые диагностированной множественной миеломой, подходящих для трансплантации, повышенная частота гематологического ПМС наблюдалась у пациентов, получавших леналидомид сразу после трансплантации высоких доз мелфалана и аутологичных стволовых клеток (Аутологичная трансплантация стволовых клеток, ASCT) по сравнению с пациентами, получавшими плацебо (1,27–1,56 и 0,46–0,53 на 100 человеко-лет, соответственно). Случаи злокачественных В-клеточных опухолей (включая лимфому Ходжкина), наблюдаемые в клинических испытаниях, были у пациентов, получавших леналидомид в условиях пост-ASCT.
Риск гематологического ПМС следует учитывать до начала лечения ревлимидом в сочетании с мелфаланом или в период сразу после приема высоких доз мелфалана и ASCT. Врачи должны тщательно обследовать пациентов до и во время лечения, используя стандартный скрининг рака на предмет ПМС, и назначать лечение в соответствии с указаниями.
Прогрессирование до острого миелоидного лейкоза (ОМЛ) при миелодиспластическом синдроме (МДС) в группе риска низкий или средний-1
• Кариотип
Исходные переменные, включая сложные цитогенетические аномалии, связаны с прогрессированием в ОМЛ у пациентов, зависимых от переливания крови, с изолированной аномалией делеции 5q. В объединенном анализе двух клинических исследований, проведенных с Ревлимидом при МДС с низким или промежуточным уровнем риска, у субъектов со сложными цитогенетическими аномалиями был самый высокий совокупный риск прогрессирования до ОМЛ, оцениваемый в 2 года (38,6%). Расчетная 2-летняя скорость прогрессирования к AML у пациентов с изолированной аномалией делеции 5q составило 13,8% по сравнению с 17,3% для пациентов с изолированной аномалией делеции 5q и одной «дополнительной цитогенетической аномалией».
Следовательно, соотношение польза / риск ревлимида неизвестно, когда МДС связан с изолированной аномалией делеции 5q и сложными цитогенетическими аномалиями.
• Статус TP53
Мутация TP53 присутствует у 20-25% пациентов с МДС с изолированной делеционной аномалией 5q низкого риска и связана с более высоким риском прогрессирования в ОМЛ. В "апостериорном анализе клинического исследования (MDS-004), проведенного с Revlimid при МДС низкого или среднего риска 1, расчетная 2-летняя скорость прогрессирования до AML составила 27,5% у пациентов с положительным IHC-p53 (1 % отсечения сильного ядерного окрашивания с использованием иммуногистохимической оценки белка p53 в качестве суррогата статуса мутации TP53) и 3,6% у пациентов с отрицательным IHC-p53 (p = 0,0038) (см. раздел 4.8).
Развитие других злокачественных новообразований при лимфоме из клеток мантии
При лимфоме из клеток мантии потенциальными рисками являются ОМЛ, злокачественные В-клеточные опухоли и немеланомный рак кожи (НМСК).
Заболевания печени
У пациентов, получавших леналидомид в составе комбинированной терапии, наблюдались случаи печеночной недостаточности, в том числе с летальным исходом: острая печеночная недостаточность, токсический гепатит, цитолитический гепатит, холестатический гепатит и смешанный цитолитический / холестатический гепатит. Механизмы тяжелой лекарственной гепатотоксичности остаются неизвестными, хотя в некоторых случаях факторами риска могут быть ранее существовавшие вирусные заболевания печени, повышенные исходные уровни ферментов печени и, возможно, лечение антибиотиками.
Обычно наблюдались аномалии функциональных тестов печени, которые обычно протекали бессимптомно и были обратимы при прекращении лечения. Как только параметры вернутся к исходному уровню, можно рассмотреть возможность возобновления лечения с более низкой дозой.
Леналидомид выводится через почки. Важно скорректировать дозу у пациентов с почечной недостаточностью, чтобы избежать достижения уровней в плазме, которые могут увеличить риск более серьезных гематологических побочных реакций или гепатотоксичности. Рекомендуется мониторинг функции печени, особенно в случае предшествующей или сопутствующей вирусной инфекции печени или когда леналидомид вводится в сочетании с лекарственными средствами, которые, как известно, связаны с нарушением функции печени.
Пациенты с впервые диагностированной множественной миеломой
Был более высокий уровень непереносимости (нежелательные явления 3 или 4 степени, серьезные нежелательные явления, прекращение лечения) у пациентов в возрасте> 75 лет, стадия ISS (Международная система постановки) III, рабочий статус (PS) ≤ 2, оцененный в соответствии с критериями ECOG (Восточная кооперативная онкологическая группа) или CLcr
Катаракта
Катаракта чаще наблюдалась у пациентов, получавших леналидомид в сочетании с дексаметазоном, особенно при длительном применении. Рекомендуется периодически контролировать зрительную способность.
04.5 Взаимодействие с другими лекарственными средствами и другие формы взаимодействия -
У пациентов с множественной миеломой, принимающих леналидомид и дексаметазон, следует с осторожностью применять эритропоэтические средства или другие средства, которые могут повышать риск тромбоза, такие как заместительная гормональная терапия (см. Разделы 4.4 и 4.8). прием леналидомида и дексаметазона (см. разделы 4.4 и 4.8).
Оральные контрацептивы
Исследования взаимодействия с пероральными контрацептивами не проводились. Леналидомид не является индуктором ферментов. В студии in vitro Леналидомид в различных концентрациях, проведенный с гепатоцитами человека, не индуцировал CYP1A2, CYP2B6, CYP2C9, CYP2C19 и CYP3A4 / 5.Следовательно, если леналидомид вводится отдельно, индукции, ведущей к снижению эффективности лекарственных средств, включая гормональные контрацептивы, не ожидается. Однако известно, что дексаметазон является индуктором CYP3A4 от слабого до умеренного и может влиять на другие ферменты и транспортные белки. Не исключено, что эффективность пероральных контрацептивов может снизиться во время лечения.
Необходимо принять эффективные меры, чтобы избежать беременности (см. Разделы 4.4 и 4.6).
Варфарин
Одновременное введение повторных доз 10 мг леналидомида не влияло на фармакокинетику разовой дозы R- и S-варфарина. Одновременный прием однократной дозы варфарина 25 мг не повлиял на фармакокинетику леналидомида. Однако неизвестно, существует ли «взаимодействие во время» клинического применения (сопутствующее лечение дексаметазоном). Дексаметазон является индуктором ферментов от слабого до умеренного, и его влияние на варфарин неизвестно. Во время лечения рекомендуется тщательный контроль концентрации варфарина.
Дигоксин
Одновременный прием 10 мг / день леналидомида увеличивал концентрацию дигоксина в плазме на 14% (0,5 мг, разовая доза) с доверительным интервалом 90% [0,52–28,2%]. Неизвестно, будет ли эффект отличаться в зависимости от терапевтической ситуации (более высокие дозы леналидомида и одновременное лечение дексаметазоном), поэтому во время лечения леналидомидом рекомендуется контролировать концентрацию дигоксина.
Статины
Когда статины назначаются с леналидомидом, существует повышенный риск рабдомиолиза, который может быть просто аддитивным. Необходим усиленный клинический и лабораторный мониторинг, особенно в первые недели лечения.
Дексаметазон
Одновременное введение однократных или многократных доз дексаметазона (40 мг / сут) не оказывает клинически значимого влияния на фармакокинетику многократных доз леналидомида (25 мг / сут).
Взаимодействие с ингибиторами P-гликопротеина (P-gp)
In vitro, Леналидомид является субстратом P-gp, но не ингибитором P-gp. Совместное введение нескольких доз мощного ингибитора P-gp, хинидина (600 мг, два раза в день) или ингибитора P-gp умеренного действия / субстрата темсиролимуса (25 мг) не оказывает клинически значимого влияния на фармакокинетику леналидомида (25). мг) Одновременный прием леналидомида не изменяет фармакокинетику темсиролимуса.
04.6 Беременность и кормление грудью -
Женщины детородного возраста / Противозачаточные средства у мужчин и женщин
Женщины детородного возраста должны использовать эффективные противозачаточные средства. Если беременность наступает во время лечения леналидомидом, терапию следует прекратить и пациентку следует обратиться к специалисту или опытному тератологу, который сможет оценить ситуацию и высказать свое мнение. Если партнер мужского пола, принимающего леналидомид, беременна, партнеру следует посоветовать обратиться к врачу-специалисту или врачу с опытом работы в тератологии, который может оценить ситуацию и высказать свое мнение.
Во время лечения леналидомид присутствует в сперме в крайне низких количествах и не обнаруживается в сперме здоровых людей через 3 дня после отмены препарата (см. Раздел 5.2). В качестве меры предосторожности и с учетом особых категорий пациентов с длительным периодом выведения, таких как пациенты с почечной недостаточностью, все пациенты мужского пола, принимающие леналидомид, должны использовать презервативы в течение всего периода лечения, во время приостановки дозы и в течение одной недели после прекращения терапии, если ваш партнер беременен или детороден и не использует никаких методов контрацепции.
Беременность
Леналидомид структурно родственен талидомиду, активному веществу с известным тератогенным эффектом у людей, вызывающим серьезные опасные для жизни врожденные дефекты.
Леналидомид вызывал пороки развития у обезьян, аналогичные описанным для талидомида (см. Раздел 5.3). Следовательно, ожидается тератогенный эффект леналидомида, и леналидомид противопоказан во время беременности (см. Раздел 4.3).
Время кормления
Поскольку неизвестно, выделяется ли леналидомид с грудным молоком человека, рекомендуется прекратить грудное вскармливание во время терапии леналидомидом.
Плодородие
Исследование фертильности, проведенное на крысах с дозами леналидомида до 500 мг / кг (примерно в 200-500 раз больше доз 25 мг и 10 мг, соответственно, используемых у людей и рассчитанных на основе площади поверхности тела), не показало никаких побочных эффектов на фертильность или материнская токсичность.
04.7 Влияние на способность управлять автомобилем и работать с механизмами -
Леналидомид оказывает слабое или умеренное влияние на способность управлять автомобилем и механизмами. Сообщалось об утомляемости, головокружении, сонливости, головокружении и нечеткости зрения во время лечения леналидомидом. Поэтому рекомендуется соблюдать осторожность при управлении транспортными средствами или механизмами.
04.8 Побочные эффекты -
Резюме профиля безопасности
Недавно диагностированная множественная миелома у пациентов, получавших леналидомид в сочетании с низкими дозами дексаметазона
Наиболее частыми (≥ 5%) серьезными побочными реакциями леналидомида в сочетании с низкими дозами дексаметазона (Rd и Rd18) по сравнению с мелфаланом, преднизоном и талидомидом (MPT) были:
• Пневмония (9,8%)
• Почечная недостаточность (включая острую) (6,3%).
Побочные реакции, наблюдаемые чаще при приеме Rd или Rd18, чем при MPT, были: диарея (45,5%), усталость (32,8%), боль в спине (32,0%), астения (28,2%), бессонница (27,6%), сыпь (24,3%). , снижение аппетита (23,1%), кашель (22,7%), гипертермия (21,4%) и мышечные спазмы (20,5%).
Пациенты с впервые диагностированной множественной миеломой, получавшие леналидомид в сочетании с мелфаланом и преднизоном
Наиболее часто наблюдаемые серьезные побочные реакции (≥ 5%) при приеме мелфалана, преднизона и леналидомида с последующей поддерживающей терапией леналидомидом (MPR + R) или мелфаланом, преднизоном и леналидомидом с последующим приемом плацебо (MPR + p) по сравнению с мелфаланом, преднизоном и плацебо, за которым следовало плацебо (MPp + p), составляли:
• Фебрильная нейтропения (6,0%)
• Анемия (5,3%)
Побочные реакции, которые наблюдались чаще с MPR + R или MPR + p, чем с MPp + p, были: нейтропения (83,3%), анемия (70,7%), тромбоцитопения (70,0%), лейкопения (38, 8%), запор (34,0%). %), диарея (33,3%), сыпь (28,9%), гипертермия (27,0%), периферические отеки (25,0%), кашель (24,0%), снижение аппетита (23,7%) и астения (22,0%).
Множественная миелома, по крайней мере, при одном предшествующем лечении
В двух плацебо-контролируемых исследованиях фазы III 353 пациента с множественной миеломой получали комбинированное лечение леналидомид / дексаметазон и 351 пациент - комбинированное лечение плацебо / дексаметазон.
Наиболее серьезными побочными реакциями, которые наблюдались чаще при использовании комбинации леналидомид / дексаметазон, чем при использовании комбинации плацебо / дексаметазон, были:
• Венозная тромбоэмболия (тромбоз глубоких вен, тромбоэмболия легочной артерии) (см. Раздел 4.4)
• Нейтропения 4 степени (см. Раздел 4.4).
Побочные реакции, которые чаще возникали при приеме леналидомида и дексаметазона по сравнению с плацебо и дексаметазоном при объединении клинических испытаний множественной миеломы (MM-009 и MM-010), включали усталость (43,9%), нейтропению (42,2%), запор ( 40,5%), диарея (38,5%), мышечные спазмы (33,4%), анемия (31,4%), тромбоцитопения (21,5%) и сыпь (21,2%).
Миелодиспластические синдромы
Общий профиль безопасности ревлимида у пациентов с миелодиспластическими синдромами основан на данных по 286 пациентам, включенным в исследования фазы II и фазы III (см. Раздел 5.1). Во второй фазе все 148 пациентов получали леналидомид. В исследовании III фазы 69 пациентов лечили леналидомидом 5 мг, 69 пациентов лечили леналидомидом 10 мг и 67 пациентов получали плацебо во время двойной слепой фазы исследования.
Большинство побочных реакций возникало в течение первых 16 недель терапии леналидомидом.
К серьезным побочным реакциям относятся:
• Венозная тромбоэмболия (тромбоз глубоких вен, тромбоэмболия легочной артерии) (см. Раздел 4.4)
• Нейтропения 3 или 4 степени, фебрильная нейтропения и тромбоцитопения 3 или 4 степени (см. Раздел 4.4).
Наиболее часто наблюдаемыми побочными реакциями, которые чаще возникали в группах леналидомида, чем в контрольной (плацебо) группе в исследовании фазы III, были нейтропения (76,8%), тромбоцитопения (46,4%), диарея (34,8%), запор ( 19,6%), тошнота (19,6%), зуд (25,4%), сыпь (18,1%), усталость (18,1%) и мышечные спазмы (16,7%).
Лимфома из клеток мантии
Общий профиль безопасности ревлимида у пациентов с лимфомой из мантийных клеток основан на данных 254 пациентов, включенных в рандомизированное контролируемое исследование фазы II MCL-002 (см. Раздел 5.1).
Кроме того, в Таблицу 3 были включены нежелательные лекарственные реакции (НЛР), наблюдаемые в дополнительном исследовании MCL-001.
Наиболее часто наблюдаемые серьезные побочные реакции в исследовании MCL-002 (с разницей не менее 2 процентных пунктов) в группе леналидомида по сравнению с контрольной группой были:
• Нейтропения (3,6%)
• Тромбоэмболия легочной артерии (3,6%)
• Диарея (3,6%)
Наиболее частыми побочными реакциями, которые чаще возникали в группе леналидомида, чем в контрольной группе в исследовании MCL-002, были нейтропения (50,9%), анемия (28,7%), диарея (22,8%), усталость (21,0%). , запор (17,4%), гипертермия (16,8%) и сыпь (включая аллергический дерматит) (16,2%).
В исследовании MCL-002 наблюдалось общее очевидное увеличение ранней смерти (в течение 20 недель). Пациенты с высокой исходной опухолевой массой имеют более высокий риск ранней смерти: 16/81 (20%) ранних смертей в группе леналидомида и 2/28 (7%) ранних смертей в контрольной группе. К 52 неделям соответствующие цифры составили 32/81 (39,5%) и 6/28 (21%) (см. Раздел 5.1).
Во время цикла лечения 1 11/81 (14%) пациента с высокой опухолевой нагрузкой были исключены из терапии леналидомидом по сравнению с 1/28 (4%) в контрольной группе. Основная причина прекращения лечения пациентов с высокой опухолевой нагрузкой во время цикла лечения 1 в группе леналидомида была связана с нежелательными явлениями, 7/11 (64%).
Повышенная масса опухоли определялась как минимум одно поражение диаметром ≥ 5 см или 3 поражения ≥ 3 см.
Сводный список побочных реакций
Сводная таблица для комбинированной терапии
Нежелательные реакции, наблюдаемые у пациентов, получавших лечение от множественной миеломы, перечислены ниже по системным классам органов и их частоте. В каждом частотном классе нежелательные реакции сообщаются в порядке уменьшения степени тяжести.Частоты определяются следующим образом: очень часто (≥ 1/10); общие (≥ 1/100,
Следующая таблица была составлена на основе данных, собранных в ходе исследований множественной миеломы с комбинированной терапией. Данные не обновлялись с учетом того, что лечение в группах, содержащих леналидомид, продолжалось до прогрессирования заболевания, по сравнению с группами сравнения в исследованиях основной множественной миеломы (см. Раздел 5.1).
Побочные реакции были помещены в соответствующую категорию в следующей таблице в соответствии с самой высокой частотой встречаемости, наблюдаемой в любом из основных клинических исследований.
Таблица 1: Побочные реакции, зарегистрированные в клинических испытаниях у пациентов с множественной миеломой, получавших леналидомид в сочетании с дексаметазоном или мелфаланом и преднизоном.
^ См. Раздел 4.8 Описание выбранных побочных реакций.
* Плоскоклеточный рак кожи наблюдался в клинических испытаниях у пациентов с миеломой, ранее получавших леналидомид / дексаметазон, по сравнению с контрольной группой.
** Плоскоклеточный рак кожи наблюдался в клиническом исследовании у пациентов с впервые выявленной миеломой, получавших леналидомид / дексаметазон, по сравнению с контрольной группой.
Сводная таблица для монотерапии
Побочные реакции, наблюдаемые у пациентов, получавших лечение по поводу миелодиспластических синдромов и лимфомы из мантийных клеток, перечислены ниже по системным классам органов и частоте.
В каждом классе частоты побочные реакции перечислены в порядке уменьшения степени тяжести. Частота определяется как: очень часто (≥ 1/10); часто (≥ 1/100,
Следующие таблицы составлены на основе данных, собранных в ходе основных исследований монотерапии миелодиспластических синдромов и лимфомы из клеток мантии.
Побочные реакции были помещены в соответствующую категорию в следующих таблицах в соответствии с наивысшей частотой встречаемости, наблюдаемой в любом из основных клинических исследований.
Таблица 2: Побочные реакции, о которых сообщалось в клинических испытаниях у пациентов с миелодиспластическими синдромами, получавших леналидомид
^ См. Раздел 4.8 Описание отдельных побочных реакций.
♦ Нежелательные явления, отмеченные как серьезные в клинических испытаниях миелодиспластических синдромов.
≈ Изменение настроения наблюдалось как частое серьезное нежелательное явление в исследовании миелодиспластических синдромов фазы III; о нежелательном явлении 3 или 4 степени не сообщалось.
Алгоритм, применяемый для включения в SmPC: Все нежелательные лекарственные реакции (НЛР), зафиксированные в алгоритме исследования фазы III, включены в европейский SmPC. Для этих нежелательных реакций был выполнен дополнительный контроль частоты нежелательных реакций, полученных с помощью алгоритма исследования фазы II, и, если частота нежелательных реакций в исследовании фазы II была выше, чем частота, зарегистрированная в исследовании фазы III, событие включали в Европейская СЛР с частотой, наблюдаемой в исследовании Фазы II.
Алгоритм, применяемый при миелодиспластических синдромах:
• Исследование фазы III миелодиспластических синдромов (двойная слепая популяция по безопасности, разница между леналидомидом 5/10 мг и плацебо для начального режима дозирования с появлением как минимум у 2 субъектов))
o Все нежелательные явления, возникающие во время лечения у ≥ 5% субъектов, получавших леналидомид, и разница не менее 2% в процентном отношении между леналидомидом и плацебо
o Все нежелательные явления 3 или 4 степени, возникающие во время лечения у 1% субъектов, получавших леналидомид, и разница не менее 1% в процентном соотношении между леналидомидом и плацебо
o Все серьезные побочные эффекты, возникающие во время лечения у 1% субъектов, получавших леналидомид, и разница не менее 1% в процентном отношении между леналидомидом и плацебо
• Фаза II исследования миелодиспластических синдромов
o Все нежелательные явления, возникающие во время лечения у ≥ 5% субъектов, получавших леналидомид o Все нежелательные явления 3 или 4 степени, возникающие во время лечения у 1% субъектов, получавших леналидомид o Все серьезные нежелательные явления, возникающие во время лечения у 1% субъектов, получавших леналидомид
Таблица 3: Побочные реакции, о которых сообщалось в клинических испытаниях у пациентов с лимфомой из мантийных клеток, получавших леналидомид
^ См. Раздел 4.8 Описание отдельных побочных реакций.
♦ Нежелательные явления, отмеченные как серьезные в клинических испытаниях лимфомы из клеток мантии.
Алгоритм, применяемый при лимфоме из клеток мантии:
• Фаза II контролируемого исследования лимфомы из клеток мантии.
o Все нежелательные явления, возникающие во время лечения у ≥ 5% пациентов в группе леналидомида, и разница не менее 2% в процентном отношении между леналидомидом и контрольной группой
o Все нежелательные явления 3 или 4 степени, возникающие во время лечения у ≥ 1% пациентов в группе леналидомида, и разница не менее 1,0% в процентном отношении между леналидомидом и контрольной группой
o Все серьезные побочные эффекты, возникающие во время лечения у ≥ 1% пациентов в группе леналидомида, и разница не менее 1,0% в процентном отношении между леналидомидом и контрольной группой
• Одноранговое исследование фазы II лимфомы из клеток мантии.
o Все нежелательные явления, возникающие во время лечения у ≥ 5% пациентов.
o Все нежелательные явления 3 или 4 степени, возникающие во время лечения, зарегистрированы у 2 или более субъектов.
Сводная таблица постмаркетинговых побочных реакций
В дополнение к вышеупомянутым побочным реакциям, выявленным в основных клинических исследованиях, следующая таблица была составлена на основе данных, собранных в ходе постмаркетинговых исследований.
Таблица 4: Побочные реакции, зарегистрированные при постмаркетинговом применении у пациентов, получавших леналидомид
^ См. Раздел 4.8 Описание отдельных побочных реакций.
Описание избранных побочных реакций
Тератогенность
Леналидомид структурно связан с талидомидом, активным веществом с известным тератогенным действием у людей, которое вызывает серьезные опасные для жизни врожденные пороки развития. Леналидомид вызывает пороки развития у обезьян, аналогичные тем, которые описаны для талидомида (см. Разделы 4.6 и 5.3). Тератогенный эффект леналидомида ожидается у людей во время беременности.
Нейтропения и тромбоцитопения
• Пациенты с впервые диагностированной множественной миеломой, получавшие леналидомид в сочетании с дексаметазоном в низких дозах
У пациентов с впервые выявленной множественной миеломой комбинация леналидомида с низкими дозами дексаметазона связана со снижением частоты нейтропении 4 степени (8,5% при Rd и Rd18 по сравнению с 15% при MPT). Фебрильная нейтропения 4 степени наблюдалась нечасто. (0,6% по сравнению с 0,7% в MPT).
У пациентов с впервые диагностированной множественной миеломой комбинация леналидомида с низкими дозами дексаметазона ассоциируется со снижением частоты тромбоцитопении 3 и 4 степени (8,1% для Rd и Rd18 по сравнению с 11% для MPT).
• Пациенты с впервые диагностированной множественной миеломой, получавшие леналидомид в сочетании с мелфаланом и преднизоном
У пациентов с впервые диагностированной множественной миеломой комбинация леналидомида с мелфаланом и преднизоном связана с более высокой частотой нейтропении 4 степени (34,1% для MMR + R / MPR + p по сравнению с 7,8% для MPp + p). фебрильной нейтропении 4 степени (1,7% в MPR + R / MPR + p по сравнению с 0,0% в MPp + p).
У пациентов с впервые диагностированной множественной миеломой комбинация леналидомида с мелфаланом и преднизоном связана с более высокой частотой тромбоцитопении 3 и 4 степени (40,4% у пациентов, получавших MMR + R / MMR + p, по сравнению с 13,7% у пациентов. обработанный MPp + p).
• Множественная миелома, по крайней мере, при одном предшествующем лечении
У пациентов с множественной миеломой комбинация леналидомида и дексаметазона связана с более высокой частотой нейтропении 4 степени (5,1% пациентов, получавших леналидомид / дексаметазон, по сравнению с 0,6% пациентов, получавших плацебо / дексаметазон. Эпизоды фебрильной нейтропении 4 степени наблюдались нечасто ( у 0,6% пациентов, получавших леналидомид / дексаметазон, по сравнению с 0,0% пациентов, получавших плацебо / дексаметазон).
У пациентов с множественной миеломой комбинация леналидомида и дексаметазона связана с более высокой частотой тромбоцитопении 3 и 4 степени (у 9,9% и 1,4% пациентов, получавших леналидомид / дексаметазон, соответственно. По сравнению с 2,3% и 0,0% из них). пациенты, получавшие плацебо / дексаметазон).
• Миелодиспластические синдромы
У пациентов с миелодиспластическими синдромами леналидомид ассоциирован с более высокой частотой нейтропении 3 или 4 степени (74,6% пациентов, получавших леналидомид, по сравнению с 14,9% пациентов, получавших плацебо, в исследовании фазы III). Эпизоды фебрильной нейтропении 3 или 4 степени наблюдались у 2,2% пациентов, получавших леналидомид, по сравнению с 0,0% пациентов, получавших плацебо. Леналидомид связан с более высокой частотой тромбоцитопении 3 или 4 степени (37% у пациентов, получавших леналидомид, по сравнению с 1,5% у пациентов, получавших плацебо, в исследовании фазы III).
• Лимфома из клеток мантии
У пациентов с лимфомой из мантийных клеток леналидомид ассоциирован с более высокой частотой нейтропении 3 или 4 степени (43,7% пациентов, получавших леналидомид, по сравнению с 33,7% пациентов в контрольной группе в исследовании фазы III). Эпизоды фебрильной нейтропении 3 или 4 степени наблюдались у 6,0% пациентов, получавших леналидомид, по сравнению с 2,4% пациентов в контрольной группе.
Венозная тромбоэмболия
Повышенный риск тромбоза глубоких вен (ТГВ) и тромбоэмболии легочной артерии (ТЭЛА) связан с использованием леналидомида и дексаметазона у пациентов с множественной миеломой и, в меньшей степени, у пациентов, получавших мелфалан и преднизон или в качестве монотерапии у пациентов с синдромы.Миелодиспластическая лимфома и лимфома из мантийных клеток, леченная леналидомидом (см. раздел 4.5) У этих пациентов одновременный прием эритропоэтических агентов или ТГВ в анамнезе также может увеличить риск тромбоза.
Инфаркт миокарда
Случаи инфаркта миокарда наблюдались у пациентов, получающих леналидомид, особенно у пациентов с известными факторами риска.
Нарушения свертываемости крови
Нарушения свертываемости перечислены в различных классификациях в зависимости от пораженного органа: патологии крови и лимфатической системы; патологии нервной системы (внутричерепное кровоизлияние); респираторные, грудные и средостенные патологии (носовое кровотечение); желудочно-кишечные патологии (десневые кровотечения, геморроидальные кровотечения, ректальное кровотечение); патологии почек и мочевыводящих путей (гематурия); травмы, отравления и процедурные осложнения (контузия); сосудистые патологии (экхимозы).
Аллергические реакции
Сообщалось о случаях аллергических реакций / реакций гиперчувствительности. В литературе сообщалось о возможной перекрестной реакции между леналидомидом и талидомидом.
Тяжелые кожные реакции
Сообщалось о случаях SSJ и NTE. Пациентам, у которых в анамнезе наблюдалась тяжелая сыпь, связанная с лечением талидомидом, не следует назначать леналидомид.
Вторая первичная опухоль
* В клинических испытаниях у пациентов с миеломой, ранее получавших леналидомид / дексаметазон, по сравнению с контрольной группой, состоящей в основном с базально-клеточным или плоскоклеточным раком кожи.
Острый миелоидный лейкоз
• Множественная миелома
В клинических испытаниях впервые выявленной множественной миеломы случаи ОМЛ наблюдались у пациентов, получавших леналидомид в сочетании с мелфаланом или вскоре после приема высоких доз мелфалана и ASCT (см. Раздел 4.4).Это увеличение не наблюдалось в клинических испытаниях у пациентов с впервые диагностированной множественной миеломой, получавших леналидомид в комбинации с дексаметазоном в низких дозах, по сравнению с талидомидом в комбинации с мелфаланом и преднизоном.
• Миелодиспластические синдромы
Исходные переменные, включая сложные цитогенетические аномалии и мутацию TP53, связаны с прогрессированием до AML у пациентов, зависимых от переливания крови, с изолированной аномалией делеции 5q (см. Раздел 4.4). Совокупный риск прогрессирования ОМЛ, оцененный через 2 года, составил 13,8% у пациентов с изолированной аномалией делеции 5q, по сравнению с 17,3% у пациентов с изолированной аномалией делеции 5q и одной дополнительной цитогенетической аномалией и 38,6% у пациентов со сложным кариотипом.
В ретроспективном анализе клинического исследования, проведенного с Ревлимидом при миелодиспластических синдромах, предполагаемое 2-летнее прогрессирование до ОМЛ составило 27,5% у IHC-p53-позитивных пациентов и 3,6% у IHC-p53-позитивных пациентов. IHC-p53 -отрицательный (p = 0,0038). У IHC-p53-положительных пациентов наблюдалась более низкая скорость прогрессирования ОМЛ среди тех, кто достиг независимого ответа от переливания крови (11,1%), по сравнению с пациентами, не ответившими на лечение (34,8%).
Заболевания печени
Наблюдались следующие постмаркетинговые побочные реакции (частота неизвестна): острая печеночная недостаточность и холестаз (оба опасны для жизни), токсический гепатит, цитолитический гепатит, смешанный цитолитический / холестатический гепатит.
Рабдомиолиз
Наблюдались редкие случаи рабдомиолиза, некоторые из них при назначении леналидомида со статинами.
Заболевания щитовидной железы
Наблюдались случаи гипотиреоза и гипертиреоза (см. Раздел 4.4 Заболевания щитовидной железы).
Реакция обострения опухоли и синдром лизиса опухоли
В исследовании MCL-002 примерно у 10% пациентов, получавших леналидомид, наблюдался СКР, по сравнению с 0% в контрольной группе. Большинство событий произошло в цикле 1, все они были расценены как связанные с лечением, и большинство сообщений относились к степени 1 или 2. Пациенты с высоким MIPI на момент постановки диагноза и заболеванием, характеризующимся большими опухолевыми массами (по крайней мере, одно поражение с максимальным диаметром ≥ 7 см. ) на исходном уровне может иметь риск СКР. В исследовании MCL-002 TLS был зарегистрирован у одного пациента в каждой из двух лечебных групп. В исследовании поддержки MCL-001 примерно 10% субъектов испытали СКР; все отчеты были 1 или 2 степени тяжести, и все были расценены как связанные с лечением. Большинство событий произошло в цикле 1. В исследовании MCL-001 не было сообщений о TLS (см. Раздел 4.4).
Желудочно-кишечные расстройства
Во время лечения леналидомидом наблюдались перфорации желудочно-кишечного тракта, которые могут привести к септическим осложнениям и могут быть связаны с летальным исходом.
Сообщение о предполагаемых побочных реакциях
Отчетность о предполагаемых побочных реакциях, возникающих после получения разрешения на лекарственный препарат, важна, поскольку позволяет осуществлять непрерывный мониторинг баланса пользы / риска лекарственного средства. Медицинских работников просят сообщать о любых предполагаемых побочных реакциях через национальную систему отчетности. В «Приложении V». .
04.9 Передозировка -
Нет особого опыта в лечении передозировки леналидомида у пациентов, хотя в исследованиях по установлению доз некоторые пациенты подвергались дозам до 150 мг, а в исследованиях однократных доз некоторые пациенты получали дозы до 400 мг. В этих исследованиях ограничивающая дозу токсичность была в основном гематологической по своей природе. В случае передозировки рекомендуется поддерживающая терапия.
05.0 ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА -
05.1 «Фармакодинамические свойства -
Фармакотерапевтическая группа: другие иммунодепрессанты.
Код УВД: L04 AX04.
Механизм действия
Механизм действия леналидомида включает противоопухолевые, антиангиогенные, проэритропоэтические и иммуномодулирующие свойства. В частности, леналидомид подавляет пролиферацию определенных гематопоэтических опухолевых клеток (включая раковые плазматические клетки ММ и клетки с делецией хромосомы 5). усиливает опосредованный Т-клетками иммунитет и естественные киллеры (NK) и увеличивает количество NKT-клеток; подавляет ангиогенез, блокируя миграцию и адгезию эндотелиальных клеток и образование микрососудов; увеличивает продукцию гемоглобина плода CD34 + гемопоэтическими стволовыми клетками и подавляет продукцию провоспалительных цитокинов (например, TNF-α и IL-6) моноцитами.
Было показано, что при МДС с изолированной аномалией делеции 5q леналидомид избирательно ингибирует аномальный клон, увеличивая апоптоз клеток Del (5q).
Леналидомид связывается непосредственно с церблоном, компонентом ферментного комплекса убиквитин-лигаза cullin-RING E3, который включает белок 1, связывающий повреждение дезоксирибонуклеиновой кислоты (ДНК) (DDB1,Белок-1, связывающий повреждения ДНК), cullin 4 (CUL4) и регулятор выбраковки 1 (Roc1). В присутствии леналидомида церблон связывается с белками-субстратами Aiolos и Ikaros, которые являются факторами лимфоидной транскрипции, вызывая их убиквитинирование и последующую деградацию с последующим цитотоксическим и иммуномодулирующим действием.
Клиническая эффективность и безопасность
Леналидомид оценивался в двух исследованиях фазы III при впервые выявленной множественной миеломе и в двух исследованиях фазы III при рецидивирующей рефрактерной множественной миеломе, как описано ниже.
Мне А также L или м недавно диагностированный множественный
Леналидомид в комбинации с дексаметазоном у пациентов, которым не требуется трансплантация стволовых клеток
Эффективность и безопасность леналидомида оценивалась в многоцентровом рандомизированном открытом трехуровневом исследовании III фазы (MM-020) у пациентов в возрасте 65 лет и старше или, если возраст моложе 65 лет, у пациентов старше 65 лет. не соответствовали критериям трансплантации стволовых клеток из-за решения пациента или недоступности трансплантации стволовых клеток по причине стоимости или по другим причинам. В исследовании (MM-020) сравнивали леналидомид и дексаметазон (Rd), вводимые в течение 2 различных периодов лечения (например, до прогрессирования заболевания [Rd группа] или до восемнадцати 28-дневных циклов [72 недели, Rd18 группа]) с мелфаланом, преднизоном и талидомид (MPT) до двенадцати 42-дневных (72-недельных) циклов. Пациенты были рандомизированы (1: 1: 1) в одну из 3 групп лечения. При рандомизации пациенты были стратифицированы по возрасту (≤ 75 лет против> 75 лет), стадии (стадии I и II по шкале ISS против стадии III) и стране.
Пациенты в группах Rd и Rd18 получали леналидомид 25 мг один раз в день в дни с 1 по 21 28-дневного цикла в соответствии с протоколом группы. Дексаметазон 40 мг вводили один раз в день на 1, 8, 15 и 22 дни каждого 28-дневного цикла лечения. Начальная доза и режим приема Rd и Rd18 были скорректированы с учетом возраста и функции почек (см. Раздел 4.2). Пациенты старше 75 лет получали дексаметазон в дозе 20 мг один раз в день на 1, 8, 15 и 22 дни каждого 28-го дня. Цикл лечения Всем пациентам во время исследования проводилась профилактика антикоагулянтами (низкомолекулярный гепарин, варфарин, гепарин, низкие дозы аспирина).
Первичной конечной точкой эффективности в исследовании была выживаемость без прогрессирования заболевания (Прогресс Бесплатное выживание, PFS). Всего в исследование было включено 1623 пациента: 535 пациентов, рандомизированных в Rd, 541 пациент, рандомизированных в Rd18, и 547 пациентов, рандомизированных в MPT. Демографические характеристики пациентов и характеристики, связанные с заболеванием, на исходном уровне были хорошо сбалансированы во всех трех группах. В целом, у испытуемых было запущенное заболевание: из общей популяции исследования 41% находились на стадии III по шкале ISS, 9% имели тяжелую почечную недостаточность (клиренс креатинина [CLcr]
В обновленном анализе PFS, PFS2 и общей выживаемости (OS) с использованием крайнего срока 3 марта 2014 г., когда среднее время наблюдения для всех выживших субъектов составляло 45,5 месяцев, результаты исследования представлены в Таблица 5.
Таблица 5: Сводка данных об общей эффективности
AMT = противомиеломная терапия; ДИ = доверительный интервал; CR = полный ответ; d = дексаметазон в низких дозах; HR = коэффициент опасности; IMWG = Международная рабочая группа по миеломе; IRAC = Независимый комитет по рассмотрению жалоб; М = мелфалан; max = максимум; min = минимум; NS = не подлежит оценке; ОС = общая выживаемость; P = преднизон; ВБП = выживаемость без прогрессирования заболевания; PR = частичный ответ; R = леналидомид; Rd = Rd вводят до документированного прогрессирования заболевания; Rd18 = Rd вводили в течение ≥ 18 циклов; SE = стандартная ошибка; Т = талидомид; VGPR = оптимальный частичный ответ; vs = против.
a Среднее значение основано на оценке Каплана-Мейера.
b 95% ДИ о медиане.
c На основе модели пропорциональных рисков Кокса, сравнивающей функции риска, связанные с указанными группами лечения.
d Значение p основано на нестратифицированном логарифмическом ранговом тесте различий в кривых Каплана-Мейера между указанными группами лечения.
e Исследовательская конечная точка (PFS2)
f Медиана - это одномерная статистика без поправки на усечение.
g Улучшенная оценка согласованного ответа на этапе лечения исследования (для определений каждой категории ответа Дата отсечения данных = 24 мая 2013 г.).
h Дата окончания = 24 мая 2013 г.
Леналидомид в комбинации с мелфаланом и преднизоном с последующей поддерживающей монотерапией при пациенты, не подходящие для трансплантации
Безопасность и эффективность леналидомида (MPR) оценивались в многоцентровом рандомизированном двойном слепом исследовании III фазы (MM-015) с участием пациентов в возрасте 65 лет и старше и с креатинином в сыворотке 75 лет) и стадии (I и II этапы МКС против III этапа).
В этом исследовании изучалось использование комбинированной терапии MMR (мелфалан 0,18 мг / кг перорально в дни 1-4 повторных 28-дневных циклов; преднизон 2 мг / кг перорально в дни 1-4 повторных 28-дневных циклов; и леналидомид 10 мг. в день перорально в дни 1-21 повторных 28-дневных циклов), для индукционной терапии, максимум до 9 циклов.Пациенты, которые завершили 9 циклов или которые не смогли завершить 9 циклов из-за непереносимости, перешли на поддерживающую монотерапию, начав с леналидомида 10 мг перорально в дни 1-21 повторных 28 циклов. Дней, до прогрессирования заболевания.
Первичной конечной точкой эффективности в исследовании была выживаемость без прогрессирования заболевания (ВБП). Всего в исследование было включено 459 пациентов: 152 пациента, рандомизированных для MMR + R, 153 пациента, рандомизированных для MMR + p и 154 пациента, рандомизированных для MPp + p. Демографические характеристики пациентов и связанные с заболеванием характеристики на исходном уровне были хорошо сбалансированы во всех трех группах; в частности, примерно 50% пациентов, включенных в каждую группу, имели следующие характеристики: стадия III по ISS и клиренс креатинина.
В «анализе PFS, PFS2 и OS с использованием крайнего срока апрель 2013 г., для которого среднее время наблюдения для всех выживших субъектов составляло 62,4 месяца, результаты исследования представлены в таблице 6.».
Таблица 6: Сводка данных об общей эффективности
ДИ = доверительный интервал; CR = полный ответ; HR = коэффициент опасности; М = мелфалан; NS = не подлежит оценке; ОС = общая выживаемость; р = плацебо; P = преднизон;
PD = прогрессирующее заболевание; PR = частичный ответ; R = леналидомид; SD = стабильное заболевание; VGPR = оптимальный частичный ответ.
a Среднее значение основано на оценке Каплана-Мейера.
¤ PFS2 (исследовательская конечная точка) была определена для всех пациентов (ITT) как время от рандомизации до начала противомиеломной терапии третьей линии или смерти от любой причины для всех рандомизированных пациентов.
Поддерживающие исследования при впервые выявленной множественной миеломе
Открытое рандомизированное многоцентровое исследование III фазы (ECOG E4A03) было проведено с участием 445 пациентов с впервые диагностированной множественной миеломой; 222 пациента были рандомизированы в группу леналидомид / дексаметазон в низких дозах, а 223 - в группу леналидомид / дексаметазон в стандартной дозе. Пациенты, рандомизированные в группу леналидомид / дексаметазон в стандартной дозе, получали леналидомид 25 мг / день с 1 по 21 дни каждые 28 дней, плюс дексаметазон 40 мг / день в дни с 1 по 4, с 9 по 12 и 17 в 20, каждые 28 дней. для первых четырех циклов. Пациенты, рандомизированные в группу леналидомид / низкие дозы дексаметазона, получали леналидомид 25 мг / день с 1 по 21 дни каждые 28 дней, плюс низкие дозы дексаметазона 40 мг / день в дни 1, 8, 15 и 22 каждые 28 дней. . В группе леналидомида / низких доз дексаметазона 20 пациентов (9,1%) испытали по крайней мере одно прерывание приема по сравнению с 65 пациентами (29,3%) в группе леналидомид / дексаметазон стандартной дозы.
В ретроспективном анализе самая низкая смертность наблюдалась в группе леналидомид / низкие дозы дексаметазона 6,8% (15/220) по сравнению с группой леналидомид / стандартной дозой дексаметазона 19,3% (43/223) в группе вновь диагностированных множественных заболеваний. популяция пациентов с миеломой со средним периодом наблюдения 72,3 недели.
Однако при длительном наблюдении разница в общей выживаемости в пользу низких доз леналидомида / дексаметазона имеет тенденцию к уменьшению.
Множественная миелома, по крайней мере, при одном предшествующем лечении
Эффективность и безопасность леналидомида оценивалась в двух многоцентровых, рандомизированных, двойных слепых, плацебо-контролируемых, параллельных группах (MM-009 и MM-010) исследований фазы III леналидомида в сочетании с дексаметазоном по сравнению с монотерапией дексаметазоном у ранее леченных пациентов с множественная миелома. Из 353 пациентов, включенных в исследования MM-009 и MM-010, получавших леналидомид / дексаметазон, 45,6% были в возрасте 65 лет и старше. Из 704 пациентов, прошедших оценку в исследованиях MM-009 и MM-010, 44,6% были 65 лет и старше.
В обоих исследованиях пациенты из группы леналидомид / дексаметазон (лен / дез) получали леналидомид 25 мг перорально один раз в день с 1 по 21 день и идентично выглядящую капсулу плацебо один раз в день. Группа плацебо / дексаметазон (плацебо / дез) принимала по 1 капсуле плацебо с 1 по 28 дни каждого 28-дневного цикла. Пациенты обеих групп принимали 40 мг дексаметазона перорально один раз в день в дни с 1 по 4, с 9 по 12 и
От 17 до 20 каждого 28-дневного цикла в течение первых 4 циклов терапии. После первых 4 курсов терапии доза дексаметазона была снижена до 40 мг перорально один раз в день в дни с 1 по 4 каждого 28-дневного цикла. В обоих исследованиях лечение продолжалось до прогрессирования заболевания. В обоих исследованиях разрешалась корректировка дозировки. на основании клинических и лабораторных данных.
Первичной конечной точкой эффективности в обоих исследованиях было время до прогрессирования заболевания (ВДП, время прогрессировать). Всего в исследовании MM-009 обследовано 353 пациента: 177 в группе леналидомид / дексаметазон и 176 в группе плацебо / дексаметазон. Всего в исследовании MM-010 обследовали 351 пациента: 176 в группе леналидомид / дексаметазон и 175 в группе плацебо / дексаметазон.
В обоих исследованиях группы леналидомид / дексаметазон и плацебо / дексаметазон имели сопоставимые начальные демографические характеристики и характеристики, связанные с заболеванием. Обе группы пациентов имели средний возраст 63 года с сопоставимым соотношением между пациентами мужского и женского пола.Восточная кооперативная онкологическая группа), количество и тип предшествующих терапий были сопоставимы в обеих группах.
Анализирует промежуточный предварительно запланированные для обоих исследований показали, что комбинированная терапия леналидомид / дексаметазон показала статистически значимое улучшение (p
Был проведен анализ эффективности расширенного наблюдения в течение медианы 130,7 недель. Таблица 7 показывает результаты анализа эффективности последующего наблюдения - совместных исследований MM-009 и MM-010.
В этом объединенном расширенном последующем анализе медиана ВДП составила 60,1 недели (95% ДИ: 44,3, 73,1) у пациентов, получавших леналидомид / дексаметазон (N = 353), по сравнению со средним значением 20, 1 неделя (95% ДИ: 17.7, 20.3) у пациентов, получавших плацебо / дексаметазон (N = 351). Медиана выживаемости без прогрессирования составила 48,1 недели (95% ДИ: 36,4, 62,1) у пациентов, получавших леналидомид / дексаметазон, по сравнению со средним временем 20,0 недель (95% ДИ: 16, 1, 20,1) у пациентов, получавших плацебо / дексаметазон. . Средняя продолжительность лечения составляла 44,0 недели (минимум: 0,1, максимум: 254,9) для леналидомида / дексаметазона и 23,1 недели (минимум: 0,3, максимум: 238,1) для плацебо / дексаметазона. В обоих исследованиях полные ответы (CR, полный ответ), частичный ответ (PR, частичный ответ) и общий ответ (CR + PR) в группе леналидомид / дексаметазон оставались значительно выше, чем в группе дексаметазон / плацебо. Медиана общей выживаемости в расширенном последующем анализе совместных исследований составляет 164,3 недели (95% ДИ: 145,1, 192,6) у пациентов, получавших леналидомид / дексаметазон, по сравнению с 136,4 неделями (95% ДИ: 113,1, 161,7) у пациентов, получавших плацебо / дексаметазон. Несмотря на то, что 170 из 351 пациента, рандомизированного для лечения плацебо / дексаметазоном, получали терапию леналидомидом после прогрессирования заболевания или после слепоты, объединенный анализ общей выживаемости продемонстрировал статистически значимое преимущество в выживаемости для группы леналидомид / дексаметазон по сравнению с плацебо. / дексаметазоновая группа (коэффициент опасности = 0,833, 95% ДИ = [0,687, 1,009], p = 0,045).
Таблица 7: Сводка результатов анализа эффективности на дату окончания для расширенного наблюдения - совместные исследования MM-009 и MM-010 (соответствующие даты окончания: 23 июля 2008 г. и 2 марта 2008 г.)
a: Двусторонний одномерный анализ, сравнивающий кривые выживаемости между группами лечения. b: Двусторонний критерий хи-квадрат с поправкой на непрерывность.
Миелодиспластические синдромы
Эффективность и безопасность леналидомида оценивалась у пациентов с трансфузионно-зависимой анемией из-за миелодиспластических синдромов низкого или промежуточного риска, связанных с цитогенетической аномалией делеции 5q, с другими цитогенетическими аномалиями или без них, в двух основных исследованиях.: Фаза III, многоцентровая. , рандомизированное, двойное слепое, плацебо-контролируемое, трехгрупповое, двухдозовое пероральное леналидомид (10 мг и 5 мг) по сравнению с плацебо-исследование (MDS-004); и Фаза II, многоцентровое, одноранговое, открытое, на леналидомид (10 мг) (MDS-003).
Приведенные ниже результаты представляют популяцию намеренных лечиться, изученную в MDS-003 и MDS-004; результаты для субпопуляции с изолированной делецией 5q показаны отдельно (утвержденные показания см. в разделе 4.1).
В исследовании MDS-004, в котором 205 пациентов были в равной степени рандомизированы для лечения леналидомидом 10 мг, 5 мг или плацебо, первичный анализ эффективности заключался в сравнении показателей независимого ответа на переливание крови в группах леналидомида 10 мг и 5 мг по сравнению с плацебо. группе (двойная слепая фаза от 16 до 52 недель и открытая фаза до 156 недель). У пациентов, у которых не было хотя бы легкой эритроидной реакции через 16 недель, лечение было прекращено. По крайней мере, умеренный эритроидный ответ позволяет продолжать терапию до рецидива эритроида, прогрессирования заболевания или неприемлемой токсичности.Пациентам, которые первоначально получали плацебо или леналидомид 5 мг и не достигали хотя бы легкой эритроидной реакции через 16 недель лечения, разрешалось перейти с плацебо на леналидомид 5 мг или продолжить лечение леналидомидом в более высокой дозе (с 5 мг на 10 мг. ).
В исследовании MDS-003, в котором 148 пациентов получали леналидомид в дозе 10 мг, первичный анализ эффективности состоял из оценки эффективности лечения леналидомидом в достижении улучшения кроветворения у субъектов с миелодиспластическими синдромами. Низкий или средний риск - 1.
Таблица 8: Сводка результатов эффективности - MDS-004 (двойная слепая фаза) и MDS-003, популяция, планирующая лечение
† Субъекты, получавшие леналидомид 10 мг на 21 день 28-дневного цикла
†† Субъекты, получавшие леналидомид в дозе 5 мг 28 дней 28-дневного цикла.
* Большинство пациентов в группе плацебо прекратили двойное слепое лечение из-за отсутствия эффективности после 16 недель лечения, прежде чем перейти к открытой фазе.
# Связано с увеличением Hgb на ≥ 1 г / дл
∞ Не достигнуто (медиана не достигнута)
В исследовании MDS-004 значительно более высокий процент пациентов с миелодиспластическими синдромами достиг первичной конечной точки трансфузионной независимости (> 182 дней) с леналидомидом 10 мг по сравнению с плацебо (55,1% против 6,0%) среди 47 пациентов с цитогенетической аномалией. .
Del (5q) изолировал и лечил 10 мг леналидомида, 27 пациентов (57,4%) добились независимости от переливаний эритроцитов.
Среднее время независимости от переливания в группе леналидомида 10 мг составляло 4,6 недели. Средняя продолжительность независимости от переливания не была достигнута ни в одной из групп лечения, но ожидается, что она превысит 2 года для субъектов, получавших леналидомид. гемоглобин (Hgb) от исходного уровня в группе 10 мг составлял 6,4 г / дл.
Дополнительные конечные точки исследования включали цитогенетический ответ (основной и второстепенный цитогенетические ответы в группе 10 мг наблюдались у 30,0% и 24,0% пациентов соответственно), оценку качества жизни, связанного со здоровьем (HRQoL), и прогрессирование до острого миелоидного лейкоза. Результаты цитогенетического ответа и HRQoL соответствовали результатам первичной конечной точки и в пользу лечения леналидомидом по сравнению с плацебо.
В исследовании MDS-003 высокий процент пациентов с миелодиспластическими синдромами достиг трансфузионной независимости (> 182 дней) с леналидомидом 10 мг (58,1%). Среднее время независимости от трансфузии составляло 4,1 недели. Средняя продолжительность независимости от трансфузии составляла 114,4 недели. Среднее увеличение гемоглобина (Hgb) составляло 5,6 г / дл.
Основные и второстепенные цитогенетические ответы наблюдались у 40,9% и 30,7% испытуемых соответственно.
Большой процент субъектов, включенных в MDS-003 (72,9%) и MDS-004 (52,7%), ранее получали препараты, стимулирующие эритропоэз.
Лимфома из клеток мантии
Эффективность и безопасность леналидомида у пациентов с лимфомой из клеток мантии оценивалась в многоцентровом рандомизированном открытом исследовании фазы II в сравнении с выбранной исследователем монотерапией у пациентов, которые были невосприимчивы к последней схеме лечения или у которых было от одного до трех рецидивов ( Изучите MCL-002).
В исследование были включены пациенты в возрасте от 18 лет с гистологически подтвержденной лимфомой из мантийных клеток и заболеванием, поддающимся измерению на КТ. Пациенты должны были получить адекватное предварительное лечение по крайней мере с одним предварительным режимом комбинированной химиотерапии. Кроме того, пациенты не должны были проходить интенсивную химиотерапию и / или трансплантацию на момент включения в исследование. Пациенты были рандомизированы 2: 1 в группу леналидомида или в контрольную группу. Выбор лечения исследователем был принят ранее. Рандомизации и состоял из монотерапии с хлорамбуцил, цитарабин, ритуксимаб, флударабин или гемцитабин.
Леналидомид вводили перорально в дозе 25 мг один раз в день в течение первых 21 дня (от G1 до G21) повторных 28-дневных циклов до прогрессирования или неприемлемой токсичности. Пациенты с умеренной почечной недостаточностью должны были получать более низкую начальную дозу леналидомида (10 мг в день) по тому же графику.
Исходные демографические данные в группах леналидомида и контрольной группы были сопоставимы. Обе популяции пациентов имели средний возраст 68,5 лет при сопоставимом соотношении пациентов мужского и женского пола.И статус эффективности, оцененный по критериям ECOG, и количество предшествующих терапий были сопоставимы в обеих группах.
Первичной конечной точкой эффективности MCL-002 была выживаемость без прогрессирования заболевания (ВБП).
Результаты эффективности для популяции, получавшей лечение (ITT), были оценены Независимой контрольной комиссией (Независимый контрольный комитет, IRC) и представлены в таблице ниже.
Таблица 9: Сводка результатов эффективности - исследование MCL-002, популяция, планирующая лечение
ДИ = доверительный интервал; CRR = полный ответ; CR = полный ответ; CRu = полный ответ не подтвержден; DMC = комитет по мониторингу данных; ITT = намерение лечить; HR = коэффициент опасности; КМ = Каплан-Мейер; MIPI = Международный прогностический индекс лимфомы из клеток мантии; NP = не актуально; ORR = общая скорость ответа; PD = прогрессирующее заболевание; ВБП = выживаемость без прогрессирования заболевания; PR = частичный ответ; SCT = трансплантат стволовых клеток; SD = стабильное заболевание; SE = стандартная ошибка.
a Медиана основана на оценке КМ.
b Диапазон рассчитан как 95% доверительный интервал относительно среднего времени выживания.
e Среднее значение и медиана являются одномерной статистикой без поправки на усечение.
d Переменные стратификации включали время от постановки диагноза до первой дозы (
e Последовательное тестирование было основано на средневзвешенном значении статистики логарифмического рангового теста с использованием нестратифицированного логарифмического рангового теста для увеличения размера выборки и нестратифицированного логарифмического рангового теста из первичного анализа. Веса основаны на событиях, наблюдавшихся на дату третьего заседания RCD, и основаны на разнице между наблюдаемыми событиями и событиями, ожидаемыми во время первичного анализа.
Представлены связанный последовательный HR и соответствующий 95% CI.
В исследовании MCL-002 в популяции ITT было общее очевидное увеличение смертности в течение 20 недель в группе леналидомида, 22/170 (13%), по сравнению с 6/84 (7%) в контрольной группе. У пациентов с высокой опухолевой нагрузкой соответствующие показатели составили 16/81 (20%) и 2/28 (7%) (см. Раздел 4.4).
Педиатрическая популяция
Европейское агентство по лекарственным средствам отказалось от обязательства предоставлять результаты исследований ревлимида во всех подгруппах педиатрической популяции по поводу множественной миеломы, миелодиспластических синдромов и лимфомы из мантийных клеток (информацию о «применении в педиатрии» см. В разделе 4.2).
05.2 «Фармакокинетические свойства -
Леналидомид имеет асимметричный атом углерода; поэтому его молекула существует в оптически активных формах S (-) и R (+). Леналидомид выпускается в виде рацемической смеси. Леналидомид обычно более растворим в органических растворителях, но наиболее растворим в 0,1 н. Растворе HCl.
Абсорбция
Леналидомид быстро всасывается после перорального приема у здоровых добровольцев в условиях голодания, достигая максимальной концентрации в плазме через 0,5–2 часа после приема дозы. У пациентов и здоровых добровольцев максимальная концентрация (Cmax) и площадь 1 дюйм под кривой зависимости концентрации от времени ( AUC) увеличивается пропорционально с увеличением дозы. Повторные дозы не вызывают значительного накопления лекарства. В плазме относительная концентрация S- и R-энантиомеров леналидомида составляет примерно 56% и 44% соответственно.
Одновременный прием высококалорийной пищи с высоким содержанием жиров у здоровых добровольцев снижает степень абсорбции, что приводит к уменьшению площади ниже AUC примерно на 20% и снижению Cmax в плазме на 50%. Однако в регистрационных исследованиях основной множественной миеломы и миелодиспластических синдромов, в которых была установлена безопасность и эффективность леналидомида, лекарство вводили без учета приема пищи. Следовательно, леналидомид можно вводить с пищей или без нее.
Популяционный фармакокинетический анализ показывает, что скорость всасывания перорального леналидомида одинакова у пациентов с множественной миеломой, пациентов с миелодиспластическими синдромами и пациентов с лимфомой из клеток мантии.
Распределение
In vitro, Леналидомид, меченный 14С, плохо связывается с белками плазмы, со средним значением 23% и 29%, соответственно, у пациентов с множественной миеломой и здоровых добровольцев.
Леналидомид присутствует в сперме (
Биотрансформация и устранение
Результаты проведенных исследований метаболизма человека. in vitro указывают на то, что леналидомид не метаболизируется ферментами цитохрома P450, что позволяет предположить, что введение леналидомида вместе с лекарственными препаратами, ингибирующими ферменты цитохрома P450, вряд ли вызовет метаболические лекарственные взаимодействия у людей. in vitro указывают на то, что леналидомид не оказывает ингибирующего действия на CYP1A2, CYP2C9, CYP2C19, CYP2D6, CYP2E1, CYP3A или UGT1A1. Таким образом, маловероятно, что леналидомид вызовет клинически значимые лекарственные взаимодействия при одновременном применении с субстратами этих ферментов.
Образование in vitro указывают на то, что леналидомид не является субстратом белков устойчивости к раку молочной железы человека (BCRP), переносчиков белков множественной лекарственной устойчивости (MRP) MRP1, MRP2 или MRP3, переносчиков органических анионов (OAT) OAT1 и OAT3, переносчиков полипептидных органических анионов (OATP) OATP1B1, органических переносчики катионов (OCT) OCT1 и OCT2, белок экструзии лекарств и токсинов (MATE) MATE1 и новые переносчики органических катионов (OCTN) OCTN1 и OCTN2.
Образование in vitro указывают на то, что леналидомид не оказывает ингибирующего действия на насос экспорта солей желчи человека (BSEP), BCRP, MRP2, OAT1, OAT3, OATP1B1, OATP1B3 и OCT2.
Большая часть леналидомида выводится с мочой. Вклад почечной экскреции в общий клиренс у субъектов с нормальной функцией почек составлял 90%, в то время как 4% леналидомида выводилось с фекалиями.
Леналидомид плохо метаболизируется, поэтому 82% дозы выводится в неизмененном виде с мочой. Гидроксиленалидомид и N-ацетил-леналидомид составляют 4,59% и 1,83% выведенной дозы соответственно. Почечный клиренс леналидомида превышает скорость клубочковой фильтрации, поэтому, по крайней мере, до некоторой степени он активно секретируется.
При дозах от 5 до 25 мг / день период полувыведения из плазмы составляет приблизительно 3 часа у здоровых добровольцев и колеблется от 3 до 5 часов у пациентов с множественной миеломой, миелодиспластическими синдромами или лимфомой из клеток мантии.
Пожилые пациенты
Специфических клинических исследований для оценки фармакокинетики леналидомида у пожилых пациентов не проводилось. Популяционный фармакокинетический анализ включал пациентов в возрасте от 39 до 85 лет и показал, что возраст не влияет на клиренс (концентрацию в плазме) леналидомида. Поскольку у пожилых пациентов более вероятно снижение функции почек, рекомендуется соблюдать осторожность при выборе доз и В качестве меры предосторожности рекомендуется мониторинг функции почек.
Почечная недостаточность
Фармакокинетика леналидомида изучалась у пациентов с почечной недостаточностью, вызванной доброкачественными заболеваниями. В этом исследовании для классификации функции почек использовались два метода: клиренс креатинина в моче, измеренный в течение 24 часов, и клиренс креатинина, рассчитанный по формуле Кокрофта-Голта. Результаты показывают, что по мере снижения функции почек (период полувыведения леналидомида увеличивается с примерно 3,5 часа у субъектов с клиренсом креатинина> 50 мл / мин до более 9 часов у субъектов с нарушением функции почек
Печеночная недостаточность
Популяционный фармакокинетический анализ включал пациентов с легкой печеночной недостаточностью (N = 16, общий билирубин от> 1 до ≤ 1,5 x ULN (верхний предел нормы) или AST> ULN) и показал, что «легкая печеночная недостаточность не влияет на клиренс (концентрацию в плазме). леналидомида Нет данных у пациентов с умеренной и тяжелой печеночной недостаточностью.
Другие внутренние факторы
Фармакокинетический анализ населения показывает, что масса тела (33–135 кг), пол, раса и тип гематологического злокачественного новообразования (MM, MDS или MCL) не имеют клинически значимого влияния на клиренс леналидомида у взрослых пациентов.
05.3 Доклинические данные по безопасности -
Исследование развития эмбриона и плода было проведено на обезьянах, получавших леналидомид в дозах от 0,5 до 4 мг / кг / день. Результаты этого исследования показали, что леналидомид вызывает внешние пороки развития, включая непатентное анальное отверстие и пороки развития верхних и нижних конечностей (искривленные, укороченные, деформированные, деформированные и / или отсутствующие части конечностей, олиго и / или полидактилия) у потомства самок обезьян, получивших препарат во время беременности.
У отдельных плодов также наблюдались различные висцеральные эффекты (изменение цвета, красные очаги в различных органах, небольшая бесцветная масса над атриовентрикулярным клапаном, маленький желчный пузырь, деформированная диафрагма).
Леналидомид показывает потенциальный риск острой токсичности; у грызунов минимальные смертельные дозы после перорального приема составили> 2000 мг / кг / день. Повторное пероральное введение 75, 150 и 300 мг / кг / день в течение до 26 недель приводило к обратимому, связанному с лечением, увеличению минерализации лоханки почек у крыс, в основном самок, при всех уровнях доз. Уровень отсутствия наблюдаемых побочных эффектов (NOAEL, отсутствие наблюдаемого уровня побочных эффектов) считается менее 75 мг / кг / день, что примерно в 25 раз превышает дневное воздействие на человека на основе значений AUC. У обезьян повторное пероральное введение 4 и 6 мг / кг / день в течение периодов до 20 недель приводило к значительной смертности и токсичности (заметная потеря веса, снижение количества лейкоцитов, эритроцитов и тромбоцитов, кровотечения в нескольких органах, воспаление желудочно-кишечный тракт, атрофия лимфатической ткани и костного мозга). Также у обезьян повторное пероральное введение 1 и 2 мг / кг / день в течение периода до 1 года вызывало обратимые изменения клеточности костного мозга, небольшое снижение соотношения миелоэритроидных клеток и атрофию тимуса. На основании сравнения AUC наблюдалось небольшое снижение количества лейкоцитов до 1 мг / кг / день, что соответствует примерно такой же дозе для людей.
Проведены исследования мутагенности in vitro (бактериальная мутация, лимфоциты человека, лимфома мыши, трансформация в эмбриональные клетки сирийского хомяка) и in vivo (тест на микроядер на крысах) не выявил каких-либо эффектов, связанных с наркотиками, ни на уровне генов, ни на уровне хромосом. Исследования канцерогенности леналидомида не проводились.
Токсичность для развития ранее изучалась на кроликах. В этих исследованиях кроликам давали перорально 3, 10 и 20 мг / кг / день леналидомида. Отсутствие промежуточной доли легкого наблюдалось при дозе 10 и 20 мг / кг / сут, с корреляцией с дозой, и эктопической почки при дозе 20 мг / кг / сут. Хотя эти условия наблюдались. в дозах, токсичных для матери, они могут быть связаны с прямым эффектом. При дозах 10 и 20 мг / кг / день у плода также наблюдались изменения мягких тканей и скелета.
06.0 ФАРМАЦЕВТИЧЕСКАЯ ИНФОРМАЦИЯ -
06.1 Вспомогательные вещества -
Содержимое капсулы
Безводная лактоза
Микрокристаллическая целлюлоза
Кроскармеллоза натрия
Стеарат магния
Оболочка капсулы
Желе
Диоксид титана (E171)
Индигокармин (E132)
Желтый оксид железа (E172)
Чернила формулировки
Шеллак
Пропиленгликоль
Оксид железа черный (E172)
Гидроксид калия
06.2 Несовместимость »-
Не имеет значения.
06.3 Срок действия »-
3 года.
06.4 Особые меры предосторожности при хранении -
Это лекарство не требует особых условий хранения.
06.5 Тип непосредственной упаковки и содержимое упаковки -
Поливинилхлорид (ПВХ) / полихлортрифторэтилен (PCTFE) / блистер из алюминиевой фольги, содержащий 7 твердых капсул.
В упаковке 21 капсула.
06.6 Инструкции по эксплуатации и обращению -
Неиспользованные лекарства и отходы, полученные от этого лекарства, необходимо утилизировать в соответствии с местными правилами.
07.0 ДЕРЖАТЕЛЬ «МАРКЕТИНГОВОГО РАЗРЕШЕНИЯ» -
Celgene Europe Limited
1 Longwalk Road
Stockley Park
Аксбридж
UB11 1DB
Соединенное Королевство
08.0 НОМЕР РАЗРЕШЕНИЯ НА МАРКЕТИНГ -
EU / 1/07/391/002
038016022
09.0 ДАТА ПЕРВОГО РАЗРЕШЕНИЯ ИЛИ ПРОДЛЕНИЯ РАЗРЕШЕНИЯ -
Дата первого разрешения: 14 июня 2007 г.
Дата последнего обновления: 14 июня 2012 г.
10.0 ДАТА ПЕРЕСМОТРА ТЕКСТА -
D.CCE сентябрь 2016 г.
11.0 ДЛЯ РАДИОПРЕПАРАТОВ: ПОЛНЫЕ ДАННЫЕ ПО ДОЗИМЕТРИИ ВНУТРЕННЕГО ИЗЛУЧЕНИЯ -
12.0 ДЛЯ РАДИОПРЕПАРАТОВ, ДОПОЛНИТЕЛЬНЫЕ ИНСТРУКЦИИ ПО ЭКСПЕРИМЕНТАЛЬНОЙ ПОДГОТОВКЕ И КОНТРОЛЮ КАЧЕСТВА -


















-cos-cause-e-disturbi-associati.jpg)