Теперь мы проиллюстрируем типы реакций, которые происходят между токсичным сайтом и целевым сайтом.
Типы реакций могут быть:
- ОБРАТНЫЙ (нековалентные связи между токсичной и биологической мишенью);
- НЕОБРАТИМЫЙ (ковалентные связи между токсичной и биологической мишенью);
- ПЕРЕНОС ЭЛЕКТРОНОВ (РЕДОКС-реакции);
- ФЕРМЕНТИЧЕСКИЕ (реакции гидролиза токсичными, такими как змеиный яд, образованные различными опасными веществами, такими как:
- Ацетилхолинэстераза, которая гидролизует нейромедиатор ацетилхолин;
- Коллагеназы, разрушающие коллаген;
- Фосфолипаза А2, ферменты, которые находятся в фосфолипидной мембране и отвечают за производство арахидоновой кислоты, следовательно, простагландинов и тромбоксана;
- Фосфодиэстеразы, которые являются ферментами, ответственными за деградацию всех этих вторичных мессенджеров, таких как цГМФ и цАМФ.
- Ферменты, разрушающие нити гена, затем ДНК (дезоксирибонуклеаза) и РНК (рибонуклеаза).
ПОСЛЕДСТВИЯ
До сих пор мы видели различные типы целей, различные связи, которые образуются между токсичным веществом и целью. Вопрос, который мы задаем себе сейчас: «а какие последствия будут иметь такие ссылки?».
Основных последствий пять:
- ВЗАИМОДЕЙСТВИЕ С ФУНКЦИЯМИ ВОЗБУЖДАЕМЫХ МЕМБРАН КЛЕТКИ;
- ВМЕШАТЕЛЬСТВО В ПРОИЗВОДСТВО ЭНЕРГИИ ЭЛЕКТРОЭНЕРГИИ;
- ИЗМЕНЕНИЕ ГОМЕОСТАЗА ИОНА КАЛЬЦИЯ;
- СМЕРТЬ КОНКРЕТНЫХ ГРУПП КЛЕТОК;
- БЕСМЕРТНОЕ ИЗМЕНЕНИЕ ГЕНОВ В СОМАТИЧЕСКИХ КЛЕТКАХ (КАНЦЕРОГЕНЕЗ).
1) ВЗАИМОДЕЙСТВИЕ С ФУНКЦИЯМИ ВОЗБУЖДАЕМЫХ МЕМБРАН КЛЕТКИ.
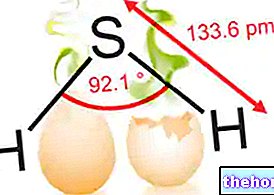
Одним из первых последствий является изменение возбудимости клеточной мембраны. Из-за взаимодействия токсического вещества с мишенью происходит изменение в распределении ионов, находящихся на двух сторонах мембраны, которые ответственны за явления. деполяризации и гиперполяризации клетки. Хлорорганические соединения, токсин, вырабатываемый рыбой (тетродотоксин), и органические растворители, такие как этанол, изменяют ионную проницаемость мембраны, делая клетку более возбудимой или менее чувствительной к возбуждению благодаря действию открытия или закрытия различных ионных каналов. присутствует на клеточной мембране.
Натриевой канал можно разделить на три стадии: закрытый, открытый и, наконец, неактивный или десенсибилизированный. Как мы помним, существует несколько веществ разного происхождения, способных воздействовать на эти натриевые каналы. Тетродотоксин (ТТХ), вырабатываемый фугу, блокирует прохождение натрия по различным специализированным каналам; таким образом не происходит деполяризации мембраны, что предотвращает передачу внутриклеточных сигналов.
Что касается органических растворителей, их влияние не на ионные каналы, а из-за того, что они очень жирорастворимы и вызывают неспецифическое «действие с дезорганизацией фосфолипидной мембраны. Наконец, хлорорганические соединения, такие как ДДТ (дихлордифенилтрихлорэтан), мешают с закрытием каналов с ионами натрия, вызывающими проблемы с возбудимостью клеток.
2) ВМЕШАТЕЛЬСТВО В ПРОИЗВОДСТВО ЭНЕРГИИ КЛЕТКОЙ.
Второй тип последствий - это вмешательство в выработку АТФ клеткой. Различные токсичные вещества действуют на разные точки окислительного фосфорилирования, препятствуя выработке аденозинтрифосфата; поэтому клетка остается без энергии. Токсичные вещества, которые действуют, подавляя образование АТФ являются:
- Синильная кислота, которая ингибирует последнюю стадию реакций цепи переноса электронов. В частности, она инактивирует фермент цитохром С-оксидазу, уменьшая количество выбрасываемых ионов H + и изменяя разность потенциалов на сторонах митохондриальной мембраны.
- Разобщающие вещества (например, хлорфенолы) увеличивают проницаемость внутренней мембраны митохондрий для ионов H +. Таким образом, проникновение ионов H + происходит с уменьшением разности потенциалов на двух сторонах мембраны с последующим уменьшением АТФ.
- Вещества, которые уменьшают поступление кислорода к митохондриям, в результате чего синтез АТФ замедляется или блокируется.
НИЗКОЕ ПРОИЗВОДСТВО АТФ означает ИЗМЕНЕНИЕ ФУНКЦИОНАЛЬНОСТИ МЕМБРАНЫ, ИОННЫХ НАСОСОВ И СИНТЕЗА БЕЛКОВ.
3) ИЗМЕНЕНИЕ ГОМЕОСТАЗА ИОНА КАЛЬЦИЯ.
Из всех ионов кальций является одним из основных вторичных мессенджеров, обеспечивающих передачу сигналов извне внутрь клетки. Все вещества, которые изменяют вход, выход, высвобождение и / или повторное поступление кальция из внутриклеточных отложений, тем или иным образом приводят к «изменению» гомеостаза кальция.
Кальций внутри клетки, в условиях покоя, всегда должен быть в определенной концентрации. Концентрация поддерживается стабильной благодаря особым механизмам регуляции кальция, которые позволяют его устранять или интегрировать. Ca2 + вне клетки, в условиях покоя он имеет концентрация 1 мМ = 10–3, а внутри 0,1 мкМ = 10–7, так что с "разница в 10 000 раз между внутренней и внешней частью.
Кальций очень важен для нашего организма, так как он очень полезен для сокращения мышц и выработки гормонов.
Как клетка поддерживает этот баланс? Ячейка имеет механизмы включения-выключения. Механизм ON увеличивает концентрацию кальция в клетке, в то время как механизм OFF действует противоположным образом, уменьшая концентрацию иона. Эти механизмы всегда должны активироваться адекватными стимулами.
- ВКЛ = + [конц.]
- ВЫКЛ = - [конц.]
Ca2 +, попадающий в клетку, может активно вытесняться определенными насосами, или он может быть изолирован и откладываться в определенных местах внутриклеточного хранения. Очень важно то, что весь гомеостатический механизм требует ЭНЕРГЕТИЧЕСКИХ РАСХОДОВ. Следовательно, все патологические состояния, такие как церебральная и / или сердечная ишемия, или все токсические вещества, которые снижают доступный клетке АТФ, определяют «изменение гомеостаза кальция». Неспособность клетки восстановить баланс этого иона. повышенная возбудимость (ЭКСИТОТОКСИЧНОСТЬ) или, что еще хуже, гибель клеток из-за некроза или апоптоза. Эксайтотоксичность вызывается глутаминовой кислотой, которая является одним из основных возбуждающих нейротрансмиттеров нашей ЦНС. Глутаминовая кислота фактически воздействует на каналы кальция ион, позволяя иону проникать и тем самым вызывая опасные эффекты для клетки. Помимо высокой возбудимости, он привлекает свободные радикалы кислорода, которые начинают реагировать с мембранными липидами, нуклеиновыми кислотами и белками. Таким образом, в нормальных условиях глутаминовая кислота действует как нейротрансмиттер, но при определенных нейродегенеративных патологиях оказывается очень опасным. или для нашего тела.
4) СМЕРТЬ КОНКРЕТНЫХ ГРУПП КЛЕТОК.
Есть токсины, вызывающие избирательную гибель групп клеток; например, йод 131 для щитовидной железы и талидомид для первичных клеток эмбриона.
Мы можем говорить об избирательной дегенерации клеток, например, в случае дегенерации дофаминовых нейронов, которые расположены в области ЦНС, ответственной за контроль движений. Эти нейроны разрушаются нейродегенеративным заболеванием, известным как БОЛЕЗНЬ ПАРКИНСОНА. Другими веществами, которые действуют на определенную популяцию нейронов, являются производные олова олова, такие как триметилолово. Эти вещества, присутствующие в пестицидах, влияют на нейроны других ограниченных областей ЦНС, таких как лимбическая система и все сенсорные области коры головного мозга.
В случае избирательного накопления в качестве примера взят йод 131, который накапливается в клетках щитовидной железы, вызывая их разрушение. Второй пример избирательного накопления - это действие талидомида в период эмбрионального развития, которое разрушает клетки, ответственные за развитие нижних и верхних конечностей, вызывая так называемую ФОКОМЕЛИЮ.
Как и в случае с талидомидом, некоторые токсины могут вызывать дегенерацию эмбриональных клеток, что приводит к выкидышу или порокам развития. Другие токсиканты, с другой стороны, могут иметь несколько механизмов, таких как цианид (связывается с цитохромоксидазой, снижает энергетические резервы клетки, определяет окислительный стресс, изменяет гомеостаз кальция) или триметилолово (изменяет гомеостаз кальция)., Снижает синтез АТФ, увеличивает высвобождение глутаминовой кислоты). Знание того, как действует токсикант, помогает предотвратить или предотвратить эффект, который это вещество может оказывать на наш организм.
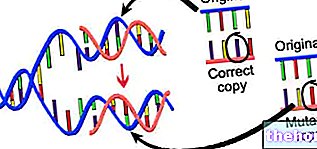
5) НЕ СМЕРТНОЕ ИЗМЕНЕНИЕ ГЕНОВ В СОМАТИЧЕСКИХ КЛЕТКАХ (КАНЦЕРОГЕНЕЗ)
Есть токсины, основная деятельность которых - вызывать модификации генов. Все эти соединения классифицируются как канцерогены. Этот момент будет более подробно рассмотрен позже в статьях о канцерогенезе.
Еще статьи на тему «Реакции между токсичной и биологической мишенью»
- Целевые молекулы токсичных веществ
- Токсичность и токсикология
- Сотовый ремонт